
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2008年全国高等院校招生统一考试
化学试卷(江苏)
一、单项选择题:(本题包括8小题,每题3分,共24分。每小题只有一个选项符合题意)
1.化学与生活、社会密切相关。下列说法不正确的是
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
2.下列文字表述与反应方程式对应且正确的是
A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓
B.用醋酸除去水垢:CaCO3+2H+==Ca2++H2O+CO2↑
C.利用腐蚀法制作印刷线路板:Fe3++Cu==Fe2++Cu2+
D.实验室用液溴和苯在催化剂作用下制溴苯:![]()
3.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA
B.标准状况下,22.4L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32-
4.下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.氯水和活性炭使红墨水褪色
C.漂白粉和水玻璃长期暴露在空气中变质
D.乙炔和乙烯使溴的四氯化炭溶液褪色
5.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O![]() Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2-e—+OH-==NiOOH+H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
6.下列装置或操作能达到实验目的的是 ( C)
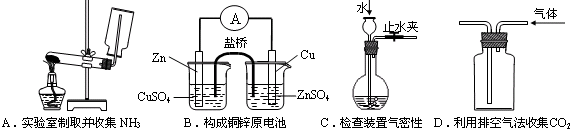
7.下列排列顺序正确的是
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4④结合质子能力:OH->CH3COO->Cl-
A.①③B.②④C.①④D.②③
8.在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
C.c(H+)=10-12mol·L-1的溶液:K+、Ba2+、Cl-、Br-
D.碳酸氢钠溶液:K+、SO42-、Cl-、H+
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
9.以下实验或操作不能达到目的的是
A.用溴水鉴别苯、乙醇、四氯化碳
B.准确称取0.4000g的NaOH固体配成1000mL浓度为0.01000mol·L-1的溶液
C.为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤
D.用激光笔检验淀粉溶液的丁达尔现象
10.下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2Cl-+2H+![]()
![]() H2↑+Cl2↑
H2↑+Cl2↑
B.用银氨溶液检验乙醛中的醛基:
CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+3Ag↓+H2O
CH3COO-+NH4++3NH3+3Ag↓+H2O
C.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-![]() 2C6H5OH+2CO32-
2C6H5OH+2CO32-
D.Na2SO3溶液使酸性KMnO4溶液褪色:
5SO32-+6H++2MnO4-==5SO42-+2Mn2+3H2O
11.香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
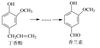
有关上述两种化合物的说法正确的是
A.常温下,1mol丁香酚只能与1molBr2反应
B.丁香酚不能与FeCl3溶液发生显色反应
C.1mol香兰素最多能与3mol氢气发生加成反应
D.香兰素分子中至少有12个原子共平面
12.下列溶液中有关物质的量浓度关系正确的是
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+) + c(M+) == c(OH-) + c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) +2c(OH-) == 2c(H+) + c(CH3COOH)
D.0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
13.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物:
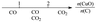
B.Fe在Cl2中的燃烧产物:

C.AlCl3溶液中滴加NaOH后铝的存在形式:

D.氨水与SO2反应后溶液中的铵盐:

14.某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀。该有机样品可能是
A.乙二醇B.乙醇C.乙醛D.甲醇和丙三醇的混合物
第二卷(非选择题 共72分)
三、(本题包括1小题,共10分)
 15.(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN-和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
15.(10分)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN-和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
Ag++2CN- == [Ag(CN)2]-
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
⑴水样预处理的目的是 。
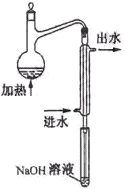
⑵水样预处理的装置如右图,细导管插入吸收液中是为了
。
⑶蒸馏瓶比吸收液面要高出很多,其目的是 。
⑷如果用盐酸代替磷酸进行预处理,实验结果将 (填“偏高”、“无影响”或“偏低”)。
⑸准确移取某工厂污水100mL,经处理后用浓度为0.01000mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00mL。此水样中含氰化合物的含量为mg·L-1(以CN-计,计算结果保留一位小数)。
15.⑴将含氰化合物全部转化为CN-⑵完全吸收HCN,防止气体放空
⑶防止倒吸 ⑷偏高 ⑸109.2
四、(本题包括2小题,共18分)
16.(8分)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
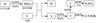
⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
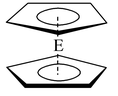 ⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:![]() 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
16.⑴Cu+H2O2+H2SO4==CuSO4+2H2O
⑵4Fe2++O2+4H+==4Fe3++2H2O2Fe3++2I—==2Fe2++I2
⑶10KOH+3Cl2+2Fe(OH)3==2K2FeO4+6KCl+8H2O
⑷13
17.(10分)工业上制备BaCl2的工艺流程图如下:
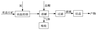
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)![]() 4CO(g) + BaS(s) △H1=571.2kJ·mol-1①
4CO(g) + BaS(s) △H1=571.2kJ·mol-1①
BaSO4(s) + 2C(s)![]() 2CO2(g) + BaS(s) △H2=226.2kJ·mol-1②
2CO2(g) + BaS(s) △H2=226.2kJ·mol-1②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,![]() = 。
= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g)![]() 2CO(g)的△H=kJ·mol-1。
2CO(g)的△H=kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是
, 。
17.⑴S2-+H2O![]() HS-+OH-HS-+H2O
HS-+OH-HS-+H2O![]() H2S+OH-(可不写)
H2S+OH-(可不写)
⑵2.7×10-3⑶172.5
⑷使BaSO4得到充分的还原(或提高BaS的产量)
①②为吸热反应,炭和氧气反应放热维持反应所需高温
五、(本题包括1小题,共10分)
18.(10分)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
⑴下列措施中,有利于降低大气中CO2浓度的有: 。(填字母)
a.减少化石燃料的使用b.植树造林,增大植被面积
c.采用节能技术d.利用太阳能、风能
⑵将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2+6H2O![]() C6H12O6+6O2b.CO2+3H2
C6H12O6+6O2b.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
c.CO2+CH4![]() CH3COOHd.2CO2+6H2
CH3COOHd.2CO2+6H2![]() CH2==CH2+4H2O
CH2==CH2+4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
⑶文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:
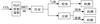
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。
CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):
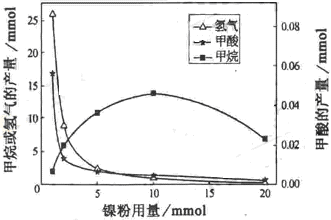 研究人员根据实验结果得出结论:
研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,
即:CO2![]() HCOOH
HCOOH![]() CH4
CH4
①写出产生H2的反应方程式
。
②由图可知,镍粉是 。(填字母)
a.反应Ⅰ的催化剂
b.反应Ⅱ的催化剂
c.反应Ⅰ、Ⅱ的催化剂
d.不是催化剂
③当镍粉用量从1mmol增加到10mmol,反应速率的变化情况是 。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应ⅠⅡ的速率均不变
d.反应ⅠⅡ的速率均增加,且反应Ⅰ的速率增加得快
e.反应ⅠⅡ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
18.⑴abcd⑵ac
⑶①3Fe+4H2O![]() Fe3O4+2H2②c③e
Fe3O4+2H2②c③e
六、(本题包括1小题,共12分)
19.(12分)苯噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
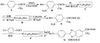
请回答下列问题:
⑴A长期暴露在空气中会变质,其原因是 。
⑵由A到B的反应通常在低温进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 。(填字母)
a.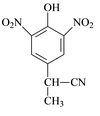 b.
b.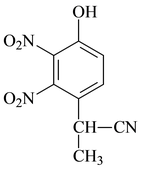 c.
c.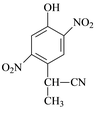 d.
d.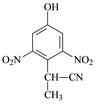
⑶在E的下列同分异构体中,含有手性碳原子的分子是 。(填字母)
a.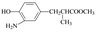 b.
b.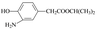
c.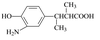 d.
d.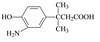
⑷F的结构简式 。
⑸D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是 。高聚物L由H通过肽键连接而成,L的结构简式是 。
19.⑴酚类化合物易被空气中的O2氧化 ⑵a⑶ac
⑷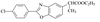
⑸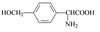
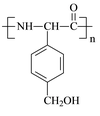 或
或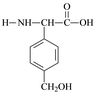
七、(本题包括1小题,共10分)
20.(10分)将一定量的SO和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2![]() 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是 。(填字母)
a.SO2和SO3浓度相等b.SO2百分含量保持不变
c.容器中气体的压强不变d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是 。(填字母)
a.向装置中再充入N2b.向装置中再充入O2
c.改变反应的催化剂d.升高温度
(3)求该反应达到平衡时SO2的转化率(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?
20.(10分)
(1)bc(2)b
(3)消耗的O2物质的量:![]()
生成的SO3物质的量:![]()
SO2和SO3的物质的量和:![]()
反应前的SO2物质的量:![]()
SO2的转化率:![]()
(4)在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量是:![]()
八、(本题包括1小题,共12分)
下列两题分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,请你选择其中一题作答,如果两题全做,则按A题评分。
21.(12分)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)B的氢化物的分子空间构型是 。其中心原子采取 杂化。
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)E的核外电子排布式是 ,ECl3形成的配合物的化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4![]() HBr+NaHSO4①
HBr+NaHSO4①
R-OH+HBr![]() R-Br+H2O②
R-Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答下列问题:
(1)在溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是 。(填字母)
a.圆底烧瓶b.量筒c.锥形瓶d.布氏漏斗
(2)溴代烃的水溶性 (填“大于”、“等于”或“小于”)相应的醇;其原因是
。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在 (填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,起目的是 。(填字母)
a.减少副产物烯和醚的生成b.减少Br2的生成
c.减少HBr的挥发d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是 。(填字母)
a.NaIb.NaOHc.NaHSO3d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于 ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是 。
21.A.(12分)
(1)C<O<N(2)三角锥形sp3
(3)![]() N2O
N2O
(4)1s22s22p63s23p63d54s1(或[Ar]3d54s1) [Cr(NH3)4(H2O)2]Cl3
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
B.(12分)
(1)d
(2)小于;醇分子可与水分子形成氢键,溴代烃分子不能与水分子形成氢键。
(3)下层
(4)abc
(5)c
(6)平衡向生成溴乙烷的方向移动(或反应②向右移动)
1-溴丁烷与正丁醇的沸点较小,若边反应边蒸馏,会有较多的正丁醇被蒸出。