
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2014年高考化学试题(江苏卷)
一、单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
 水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图像,模型如图。下列关于水的说法正确的是( )
水是生命之源,2014年我国科学家首次拍摄到水分子团簇的空间取向图像,模型如图。下列关于水的说法正确的是( )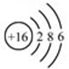
| 物质 组别 | 甲 | 乙 | 丙 |
| A | |||
| B | |||
| C | |||
| D |
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
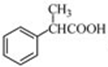 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: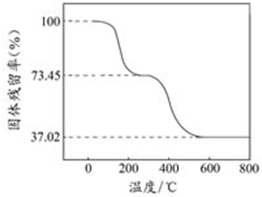 ①准确称取3.390g样品与足量稀盐酸充分反应,生成
①准确称取3.390g样品与足量稀盐酸充分反应,生成
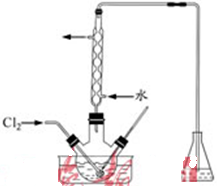 (1)向含碘废液中加入稍过量的
(1)向含碘废液中加入稍过量的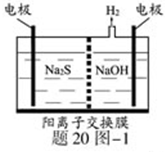 (1)将烧碱吸收
(1)将烧碱吸收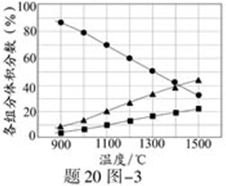 ②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成__________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成__________________。 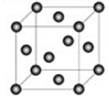 (5)
(5)【解析】水极微弱电离,是弱电解质;可燃冰的主要成分是甲烷;冰的密度小于液态水;氢氧还可以组成双氧水;正确选项是A。
【知识点】物质的分类; 常见物质的性质及用途
2.B
【解析】过氧化钠是离子化合物,A错误;C画的是硫原子的结构示意图;D是对二甲苯。B正确。 【知识点】原子结构与元素周期律
3.C
【解析】
PH=1酸性环境中不能大量存在![]() ;c(
;c(![]() )=1×10-13mol/L的碱性溶液中不能大量存在Mg2+、Cu2+;
)=1×10-13mol/L的碱性溶液中不能大量存在Mg2+、Cu2+;![]() 溶液中不能大量存在
溶液中不能大量存在![]() 。ABD均不正确,
。ABD均不正确,![]() 溶液近中性,K+、Na+、NO3-、Cl-相互不影响,可以大量共存。
溶液近中性,K+、Na+、NO3-、Cl-相互不影响,可以大量共存。
【知识点】离子共存
4. B
【解析】晶体硅用于制作半导体材料,因为其导电性,和其硬度熔点无关;漂白粉用于漂白纸,因为其强氧化性,和在空气中不稳定易变质无关;氧化铁用于制作红色涂料,是利用其颜色是红色,和他的碱性氧化物能和酸反应没关系;ACD都是错误的,.氢氧化铝具有弱碱性,可用于中和胃酸(盐酸)过多,B正确。 【知识点】常见物质的性质及用途;生活中的材料
5. C
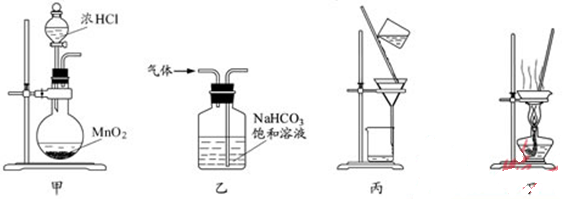
【解析】甲无加热装置,A错误;乙中的吸收液,可以吸收氯气,B错误;丁装置的操作不能蒸干,得不到MnCl2·4H2O晶体;D也是错误的;C操作中二氧化锰不溶于水,而氯化锰可溶,可以用过滤的方法分离,图示也没有问题,C正确。 【知识点】化学实验基础知识
6. A
【解析】氧原子摩尔质量是16g/mol,所以,1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA,A 正确;丙烯酸分子中除含有碳碳双键外,还有碳氧双键,B错误;标况下,苯不是气体,C错误;水的反应中,每生成0.1mol氧气,转移电子的数目为0.2NA,D错误。
【知识点】阿伏伽德罗常数
7. D
【解析】A反应的产物是NO,B中NH4+也参加离子反应,C中醋酸不能拆开,三个选项都是错误的,D正确。 【知识点】离子方程式的书写及正误判断
8.B
【解析】
B选项中,O2和稀HNO3不反应,气体选项近符合题意。
【知识点】其他非金属及其化合物; 氮、磷及其化合物
9.D
【解析】
由题干所给信息,可推知X、Y、Z、W四种元素,分别是:碳、氧、镁、硅,原子半径应是r(Z)>r(W)>r(X)>r(Y),A错误;氧化镁是离子键,二氧化硅是共价键,化学键不同,B错误;碳酸酸性比硅酸强,C错误;水的稳定性比硅烷强,D正确,选项D。 【知识点】无机推断
10. C
【解析】除第二反应是吸热外,其余三个都是放热反应,AB都错误;由盖斯定律,C正确,D系数不对,错误,选项是 C
【知识点】化学反应与能量变化; 盖斯定律; 焓变与键能
二、不定项选择题
11. C
【解析】铜比铁稳定,应附着比铁活泼的锌,A错误;反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的体积减小,若在常温下能自发进行,则该反应的△H<0;B 错误;水解是吸热反应,所以C正确;D选项速率增大,平衡常数减小,错误。
【知识点】金属的化学腐蚀与防护; 化学反应与能量变化; 水的电离和溶液酸碱性; 影响化学反应速率的因素
12. B D
【解析】由甲肾上腺素的结构简式可知:酚羟基是两个,手性碳原子1个(连醇羟基者),1mol去甲肾上腺素最多能与3molBr2发生取代反应(酚羟基临、对位),它既能和盐酸反应(碱性氨基),又能和氢氧化钠溶液反应(酸性的酚羟基),选项是BD
【知识点】有机物的结构; 有机物官能团及性质; 有机反应的类型
13. D
【解析】向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,主要是Cl2的氧化性,D错误,其他三个选项都是正确的。
【知识点】实验探究; 氯及其化合物;无机推断
14. AC
【解析】
A中二者恰好反应,生成弱电解质醋酸,离子浓度大小关系正确;B选项中NH3·H2O的电离大于NH4+的水解,其大小关系是:c(NH4+)>c(Cl-)>c(NH3·H2O)>c(OH-),0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合,物料守恒2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],C正确;D选项的关系中无Cl-,电荷不守恒,错误。正确选项是AC。
【知识点】离子浓度
15. AD
【解析】对比反应Ⅰ、Ⅲ,温度高CH3OCH3(g)的含量低,该反应的正方应为放热反应,A正确;反应的气体体积前后不变,相同条件下,增加CH3OH(g)的量,平衡不移动,体积分数相同,B错误;温度高,速率快,Ⅲ比Ⅰ的时间短,C错误;由表格所给数据,利用“三段式”,可计算出该反应387°C时的平衡常数是K=4,若按D项投料,K1=1.5<4,故反应向正向进行。D正确。
【知识点】化学反应与能量变化; 化学反应速率; 化学反应速率
三、非选择题
16.
(1)![]()
![]()
(2)![]()
![]()
(3)溶液中的部分![]() 被氧化为
被氧化为![]() 减小
减小
【解析】
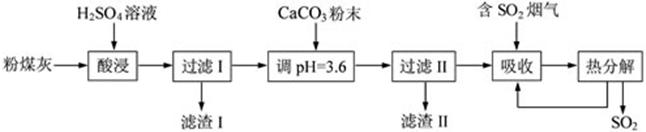
(1)粉煤灰含有![]() 、
、![]() ,加硫酸
,加硫酸![]() 不反应,成为滤渣,和
不反应,成为滤渣,和![]() 的反应方程式为:
的反应方程式为:![]()
(2)加![]() 使
使![]() 转化为
转化为![]() ,同时必然生成微溶的
,同时必然生成微溶的![]() ;若溶液的pH偏高,碱性较强,会生成氢氧化铝的沉淀,导致溶液中铝元素的含量降低。其离子方程式为:
;若溶液的pH偏高,碱性较强,会生成氢氧化铝的沉淀,导致溶液中铝元素的含量降低。其离子方程式为:![]()
(3)在上述流程中,溶液中的![]() 会-部分被氧化为
会-部分被氧化为![]() ,所以,分解放出的
,所以,分解放出的![]() 量总是小于吸收的
量总是小于吸收的![]() 量。同时导致溶液的酸性增强,PH减小。
量。同时导致溶液的酸性增强,PH减小。
【知识点】化学方程式书写;无机推断; 离子方程式的书写及正误判断; 水的电离和溶液酸碱性
17.
(1)醚键羧基
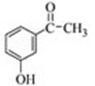
(2)
(3)①③④
(4)![]()
(5)
【解析】
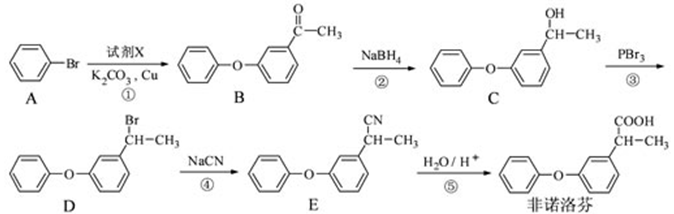
(1)从非诺洛芬的分子结构可看出,含氧官能团有羧基和醚键
(2)明显反应①是卤代烃和酚羟基的取代反应,所以X的结构简式为 
(3)在所进行的五部反应中,可清楚看出属于取代反应的有①、③、④
(4)又B的组成,根据题意要求,可发生银镜反应,必有醛基;可水解应有酯基;且水解后产生酚羟基,结合分子中含有两个苯环,有6种不同化学环境的氢,其结构简式只能是:![]()
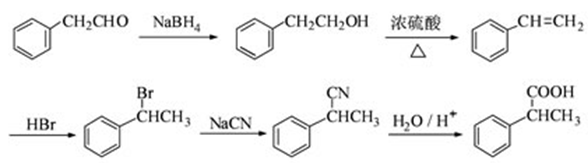
(5)由题意要求,结合所给信息,合成路线如【答案】。
【知识点】有机物官能团及性质; 有机物的结构; 有机反应的类型; 同分异构体; 有机合成与推断
18.
(1)生成的产物具有阻燃作用
(2)2a+3b=c+2d
(3)![]()
![]()
在270~600°C之间,失去结晶水后的样品进一步热分解放出![]() 和
和![]()
![]()
![]()
![]()
![]()
![]()
【解析】
(1)从碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]组成上看,在受热时发生分解反应,吸收热量,同时,其分解产物也有阻燃作用,所以,可以作塑料阻燃剂。
(2)由化合价代数和等于0可知,四者相互关系是:2a+3b=c+2d。
(3)样品中的n(OH-): n(CO32-)及计算过程见【答案】。
【知识点】分子结构;化学计算
19.
(1)![]() 使
使![]() 中的碘进入水层。
中的碘进入水层。
(2)分液
(3)使氯气在溶液中有较大溶解度(或防止碘的升华或防止碘进一步被氧化等) 氢氧化钠溶液
(4)从水层去少量溶液,加入1~2ml淀粉溶液,加盐酸酸化,滴加![]() 溶液,若溶液变蓝色,说明废水中含有
溶液,若溶液变蓝色,说明废水中含有![]() ,若溶液不变蓝,说明废水中不含有
,若溶液不变蓝,说明废水中不含有![]() 。
。
另从水层取少量原溶液,加入1~2ml淀粉溶液,加盐酸酸化,滴加![]() 溶液,若溶液变蓝色,说明废水中含有
溶液,若溶液变蓝色,说明废水中含有![]() ,若溶液不变蓝,说明废水中不含有
,若溶液不变蓝,说明废水中不含有![]() 。
。
【解析】
(1)![]() 具有氧化性,可以氧化
具有氧化性,可以氧化![]() ,
,![]() ,其目的是将易溶于
,其目的是将易溶于![]() 的
的![]() 变成
变成![]() 后,易进入水中。
后,易进入水中。
(2)不相溶解的液体间分离,应采用分液方法。
(3)温度高氯气在水中的溶解度减小,所以,该实验控制在低温下进行。为吸收有毒的氯气,锥形瓶里盛放氢氧化钠溶液。
(4)对于含碘废水中可能存在![]() 、
、![]() 的检验,见【答案】。
的检验,见【答案】。
【知识点】离子方程式的书写及正误判断; 化学实验基础知识; 化学实验的设计与评价
20.
(1)①![]() ②
②![]()
(2)①Cu、H、Cl ②0.5mol ③提高混合气体中空气的比例
(3)![]()
【解析】
(1)电解时,阴极发生阳离子的还原反应,放电的只能是![]() ,电极反应式是:
,电极反应式是:![]() ,阳极区的
,阳极区的![]() 酸化失电子得S,必然的电子生成
酸化失电子得S,必然的电子生成![]() ,方程式为:
,方程式为:![]()
(2)图示中变价元素是铁和氧,不变的是Cu、H、Cl。电子守恒,反应中当有1mol![]() 转化为硫单质时,需要消耗
转化为硫单质时,需要消耗![]() 0.5mol。在工艺要求前提下,要生成S而不生成-2价的CuS,当然需要提高混合气体中空气的含量即增加氧气的量。
0.5mol。在工艺要求前提下,要生成S而不生成-2价的CuS,当然需要提高混合气体中空气的含量即增加氧气的量。
(3)由图示,在高温下,硫化氢分解的氢气是另一成分的二倍,所以,其分解的方程式为: ![]()
【知识点】电解池;化学方程式书写;离子方程式的书写及正误判断;化学计算;基本概念的知识
21.
A.[物质结构与性质]
(1)[Ar]![]() 或
或![]()
(2)HF
(3)sp2 6mol,(或6![]() 个、6×6.02×
个、6×6.02×![]() 个)
个)
(4)2Cu(OH)2+CH3CHO+NaOHCH3COONa+Cu2O↓+3H2O
(5)12
【解析】
(1)铜是29号元素,故Cu+基态核外电子排布式为: [Ar]![]() 或
或![]() 。
。
(2)OH-是两原子10电子离子,所以,其等电子体的一种分子是HF
(3)醛基中含C=O,所以碳原子的轨道杂化类型是sp2。由乙醛结构简式![]() ,分子中含有的δ键数是6mol。
,分子中含有的δ键数是6mol。
(4)NaOH的![]() 悬浊液与乙醛反应方程式比较简单,见【答案】。
悬浊液与乙醛反应方程式比较简单,见【答案】。
(5)由铜晶胞结构图示,可计算出每个铜原子周围距离最近的铜原子数目是12个(顶点和面心点,3×4=12)。
【知识点】原子结构与元素周期律; 化学键与分子间作用力; 化学方程式书写; 晶体结构与性质
B.[实验化学]
(1)加快铁和稀硫酸的反应速率
(2)①用蒸馏水洗净 用![]() 标准溶液润洗2~3次 ②
标准溶液润洗2~3次 ②![]() ③AB
③AB
(3)氢氧化铁
【解析】
(1)实验中,为加快铁和稀硫酸的反应速率,需要在搅拌的情况下,同时加热。
(2)滴定实验中,滴定管在注入7标准溶液前,需要需要检漏、用蒸馏水洗净、用标准溶液润洗2~3次;由电子守恒,利用方程式可计算出![]() ;
;![]() 升高温度易分解,且该反应是在酸性条件下进行,要使滤液中的
升高温度易分解,且该反应是在酸性条件下进行,要使滤液中的![]() 完全被
完全被![]() 氧化,选AB条件下进行,CD不行。
氧化,选AB条件下进行,CD不行。
(3)因 ![]() 溶液显碱性,加入含有
溶液显碱性,加入含有![]() 的溶液中,很可能生成氢氧化铁杂质。
的溶液中,很可能生成氢氧化铁杂质。