
最新!2022湖南物理高考真题及答案解析出炉
06月11日
双流中学2016--2017学年届高三(下)2月月考
理科综合
物理部分
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共4页,满分110分.
第Ⅰ卷(选择题,共42分)
选择题(本题共7小题.其中1—5题为单项选择题;6—7题为多项选择题,每题全部选对的得6分,选对但不全的得3分,有选错的得0分.)
 1.如图,电源电动势为E,线圈L的直流电阻不计.则以下判断正确的是
1.如图,电源电动势为E,线圈L的直流电阻不计.则以下判断正确的是
A.闭合S,稳定后,电容器两端电压为E
B.闭合S,稳定后,电容器的a极带正电
C.断开S瞬间,电容器的a极将带正电
 D.断开S瞬间,电容器的a极将带负电
D.断开S瞬间,电容器的a极将带负电
2.如图所示,半径为R的圆形区域内有垂直于纸面向里的匀强磁场;重力不计、电荷量一定的带电粒子以速度v正对着圆心O射入磁场,若粒子射入、射出磁场点间的距离为R,则粒子在磁场中的运动时间为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
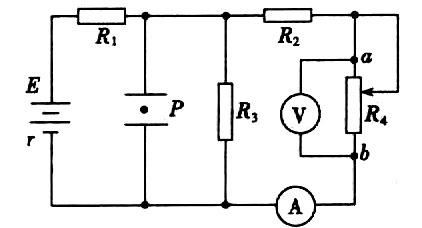 3.如图所示,位于平行金属板中央的带电质点P处于静止状态,不考虑电流表和电压表对电路的影响,当滑动变阻器R4的滑片向b端移动时,则
3.如图所示,位于平行金属板中央的带电质点P处于静止状态,不考虑电流表和电压表对电路的影响,当滑动变阻器R4的滑片向b端移动时,则
A.质点P将向上运动 B.R3上消耗的功率逐渐增大
C.电流表读数减小 D.电压表读数减小
4.假设月球半径为R,月球表面的重力加速度为g0.如图所示,“嫦娥三号”飞船沿距月球表面高度为3R的圆形轨道Ⅰ运动,到达轨道的A点,点火变轨进入椭圆轨道Ⅱ,到达轨道Ⅱ的近月B点再次点火进入近月轨道Ⅲ绕月球做圆周运动.下列判断正确的是
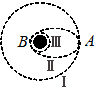 A.飞船在A点点火变轨前后相比较,变轨后动能减小
A.飞船在A点点火变轨前后相比较,变轨后动能减小
B.飞船在Ⅱ轨道上由A点运动到B点的过程中,动能减小
C.飞船在轨道Ⅲ跟轨道Ⅰ的线速度大小之比为1:2
D.飞船在轨道Ⅰ绕月球运动一周所需的时间为![]()
5.电磁流量计广泛应用于测量可导电流体(如污水)在管中的流量(在单位时间内通过管内横截面的流体的体积).为了简化,假设流量计是如图所示的横截面为长方形的一段管道,其中空部分的长、宽、高分别为图中的a、b、c.流量计的两端与输送流体的管道相连接(图中虚线).图中流量计的上下两面是金属材料,前后两面是绝缘材料.现于流量计所在处加磁感强度为B的匀强磁场,磁场方向垂直于前后两面.当导电流体稳定地流经流量计时,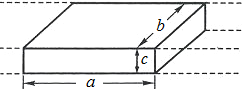 在管外将流量计上、下两表面分别与一串接了电阻R的电流表的两端连接,I表示测得的电流值.已知流体的电阻率为ρ,不计电流表的内阻,则可求得流量为
在管外将流量计上、下两表面分别与一串接了电阻R的电流表的两端连接,I表示测得的电流值.已知流体的电阻率为ρ,不计电流表的内阻,则可求得流量为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
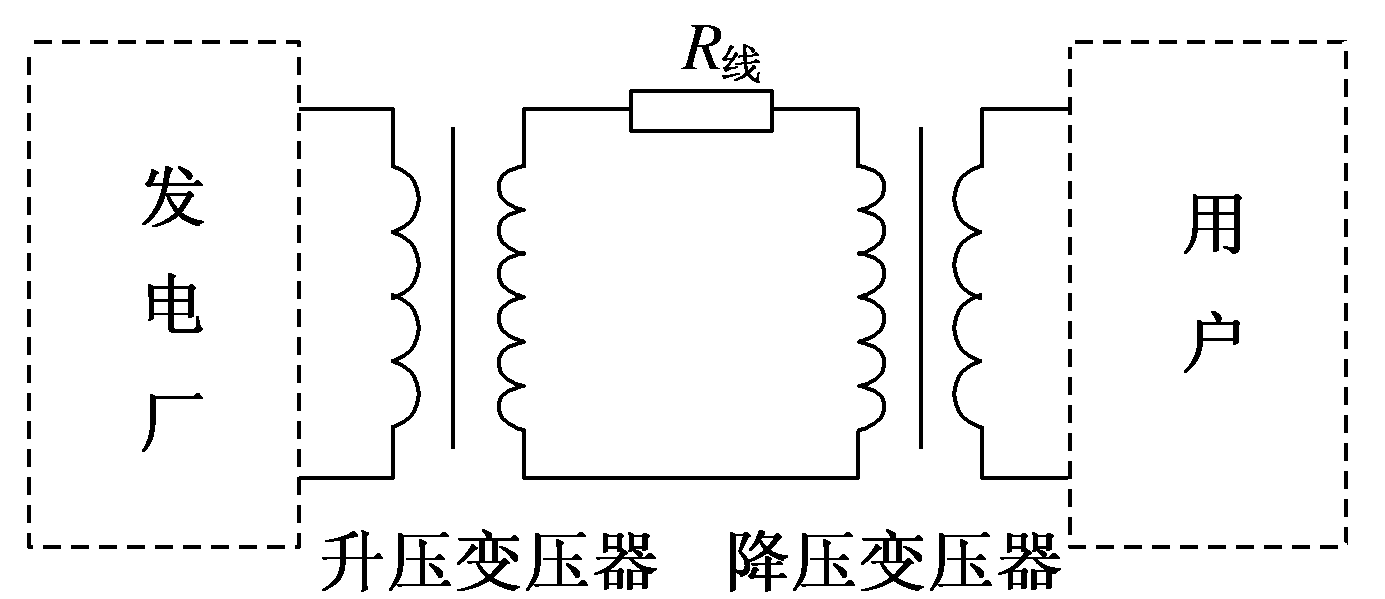 6.在如图所示的远距离输电电路图中,升压变压器和降压变压器均为理想变压器,发电厂的输出电压和输电线的电阻均不变,随着用户用电量的增加,发电厂输出功率的增大,下列说法中正确的有
6.在如图所示的远距离输电电路图中,升压变压器和降压变压器均为理想变压器,发电厂的输出电压和输电线的电阻均不变,随着用户用电量的增加,发电厂输出功率的增大,下列说法中正确的有
A.升压变压器的输出电压增大
B.降压变压器的输出电压增大
C.输电线上损耗的功率增大
D.输电线上损耗的功率占总功率的比例增大
7.如图甲所示,质量m=2kg的物块放在光滑水平面上,在P点的左方始终受到水平恒力F1的作用,在P点的右方除受F1外还受到与F1在同一直线上的水平恒力F2的作用.物块从A点由静止开始运动,在0~5s内运动的v—t图象如图乙所示,由图可知
 A.t=2.5s时,小球经过P点
A.t=2.5s时,小球经过P点
B.t=2.5s时,小球距P点距离最远
C.t=3.0时,恒力F2的功率P为10W
D.在1~3s的过程中,F1与F2做功之和为8J
第Ⅱ卷(非选择题,共68分)
8.(1)(6分)为判断线圈绕向,可将灵敏电流计G与线圈L连接,如图所示.已知线圈由a端开始绕至b端;当电流从电流计G左端流入时,指针向左偏转.
 ①将磁铁N极向下从线圈上方竖直插入L时,发现指针向左偏转.俯视线圈,其绕向为_____________(填“顺时针”或“逆时针”).
①将磁铁N极向下从线圈上方竖直插入L时,发现指针向左偏转.俯视线圈,其绕向为_____________(填“顺时针”或“逆时针”).
②当条形磁铁从图中虚线位置向右远离L时,指针向右偏转.俯视线圈,其绕向为_____________(填“顺时针”或“逆时针”).
(2)(10分)现仅有以下器材:
电流表A1(量程0.2A,内阻约为1Ω) 电流表A2(量程0.02A,内阻约为10Ω)
电压表V1(量程3V,内阻约为3kΩ) 电压表V2(量程10V,内阻约为10kΩ)
滑线变阻器R(0~10Ω,额定电流1A) 电阻箱R0(0~9999.9Ω,额定电流0.1A)
蓄电池组E(电动势6V,内阻r=0.1Ω) 电键S及导线若干
为较准确地测定一电阻值Rx约1.2Ω的电阻丝的阻值,已有甲、乙两位同学分别设计了甲、乙两个电路图来测量Rx.但甲、乙两电路设计均有不合理之处,请指出存在的问题(各图分别指出两处即得满分).
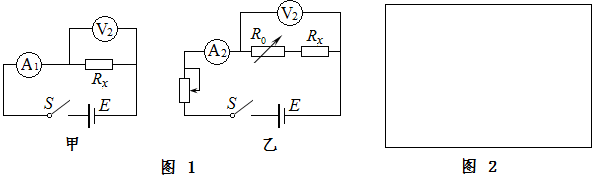
①甲图不合理之处: , .(2分)
②乙图不合理之处: , .(2分)
③请设计一个实用的较合理的电路图,画在规定方框内;(画电路图2分)
并写出Rx的计算公式:Rx= ;(2分)
说明公式中各物理量的意义是: .(2分)
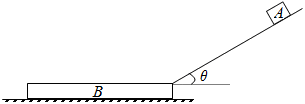
9.(15分)如图所示,一质量为mB=2kg的木板B静止在光滑的水平面上,其右端上表面紧靠一固定斜面轨道的底端(斜面底端与木板B右端的上表面之间有一段小圆弧平滑连接),轨道与水平面的夹角θ=37°.一质量也为mA=2kg的物块A由斜面轨道上距轨道底端x0=8m处静止释放,物块A刚好没有从木板B的左端滑出.已知物块A与斜面轨道间的动摩擦因数为μ1=0.25,与木板B上表面间的动摩擦因数为μ2=0.2,sin370=0.6,cos370=0.8,g取10m/s2,物块A可看作质点,求:
(1)物块A刚滑上木板B时的速度为多大?
(2)物块A从刚滑上木板B到相对木板静止共经历了多长时间?木板B有多长?
10.(17分)如图所示,BCPC′D是螺旋轨道,半径为R的圆O与半径为2R的BCD圆弧相切于最低点C,与水平面夹角都是37°的倾斜轨道AB、ED分别与BC、C′D圆弧相切于B、D点(C、C′均为竖直圆的最底点),将一劲度系数为k的轻质弹簧的一端固定在AB轨道的有孔固定板上,平行于斜面的细线穿过有孔固定板和弹簧跨过定滑轮将小球和大球连接,小球与弹簧接触但不相连,小球质量为m,大球质量为![]() ,ED轨道上固定一同样轻质弹簧,弹簧下端与D点距离为L2,初始两球静止,小球与B点的距离是L1,L1>L2,现小球与细线突然断开.一切摩擦不计,重力加速度为g,sin370=0.6,cos370=0.8.
,ED轨道上固定一同样轻质弹簧,弹簧下端与D点距离为L2,初始两球静止,小球与B点的距离是L1,L1>L2,现小球与细线突然断开.一切摩擦不计,重力加速度为g,sin370=0.6,cos370=0.8.
(1)细线刚断时,小球的加速度大小;
(2)小球恰好能完成竖直圆周运动这种情况下,小球过C点前后瞬间有压力突变,求压力改变量为多少?
(3)小球冲上左侧轨道获得与初始线断相同的加速度时,小球的速度.

11.(20分)如图,质量为M的足够长金属导轨abcd放在光滑的绝缘水平面上.一电阻不计,质量为m的导体棒PQ放置在导轨上,始终与导轨接触良好,PQbc构成矩形.棒与导轨间动摩擦因数为μ,棒左侧有两个固定于水平面的立柱.导轨bc段长为L,开始时PQ左侧导轨的总电阻为R,右侧导轨单位长度的电阻为R0.以ef为界,其左侧匀强磁场方向竖直向上,右侧匀强磁场水平向左,磁感应强度大小均为B.在t=0时,一水平向左的拉力F垂直作用在导轨的bc边上,使导轨由静止开始做匀加速直线运动,加速度为a.
(1)求回路中感应电动势及感应电流随时间变化的表达式;
(2)经过多长时间拉力F达到最大值,拉力F的最大值为多少?
 (3)某过程中回路产生的焦耳热为Q,导轨克服摩擦力做功为W,求导轨动能的增加量.
(3)某过程中回路产生的焦耳热为Q,导轨克服摩擦力做功为W,求导轨动能的增加量.
双流县中学高2016届高三2月月考理科综合能力测试
化学试题
命 题:杨华敏 审 题:廖泽君
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 Cu-64
第I卷(选择题,共42分)
本卷共7题,每题6分,共42分。在每题给出的四个选项中,只有一项最符合题目要求。
1、化学与生产、生活密切相关,下列叙述错误的是
A.饱和Na2SO4溶液可以使蛋白质变性
B.大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染
C.从海带中提取碘单质的过程涉及氧化还原反应
D.镀锌铁桶镀层破损后铁仍不易被腐蚀
2、下列离子在给定条件下,可能大量共存的是
B.溶解有AlCl3的溶液中:Na+、K+、SO42—、S2—
C.25℃时,水电离出的c(H+)=1×l0-l3mol/L的溶液中:K+、Ba2+、NO3—、I—
D.离子浓度均为0.1 mol/L的溶液中:Na+、Fe3+、CH3COO—、NO3—
3、设NA为阿伏加德罗常数的值。下列说法中正确的是
A.46 g C2H6O中含有的C-H键数一定为5 NA
B.常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA
C.将15.6 g Na2O2投入到足量水中,反应后溶液中的氧原子数为0.4NA
D.2 mol SO2和1 mol O2混合,所得气体的分子数为2NA
4、下列实验“操作和现象”与“结论”都正确的是
| 操作和现象 | 结 论 | |
| A | 向盛有2mL 0.1mol/L AgNO3溶液的试管中,先滴几滴0.1mol/L KCl溶液,再滴加0.1mol/L KI溶液。试管中先出现白色沉淀,后出现淡黄色沉淀 | Ksp(AgCl)< Ksp(AgI) |
| B | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| C | 在分液漏斗中加入碘水后再加入CCl4,充分振荡,分层,下层溶液呈紫色 | CCl4可作为碘的萃取剂 |
| D | 测定饱和NaClO溶液、CH3COONa溶液的pH, pH(NaClO)>pH(CH3COONa) | 弱酸的酸性:HClO< CH3COOH |
5、现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,吸收有毒的硫化氢气体。工艺原理如下图所示。下列说法中正确的是
A.电解池中OH—从右槽迁移到左槽
B.H+在右槽发生氧化反应
C.左槽中发生的反应是:4OH—-4e—=O2↑ + 2H2O
D.常温常压下,反应中每转移1mol电子生成1g氢气
 6、电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点。右图是某同学用0.1mol/L KOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计)。下列有关判断不正确的是
6、电导率是衡量电解质溶液导电能力大小的物理量,据溶液电导率变化可以确定滴定反应的终点。右图是某同学用0.1mol/L KOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的HCl和CH3COOH溶液滴定曲线示意图(混合溶液体积变化忽略不计)。下列有关判断不正确的是
A.曲线①代表0.1 mol/L KOH溶液滴定CH3COOH溶液的滴定曲 线,曲线②代表0.1 mol/L KOH溶液滴定HCl溶液的滴定曲线
B.在相同温度下,C点水电离的c(H+)大于A点水电离的c(H+)
C.在A点的溶液中有:c(CH3COO—)+ c(OH—)﹣c(H+)= 0.05 mol/L
D.在B点的溶液中有:c(K+)> c(OH—)> c(CH3COO—)> c(H+)
7、工业上用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)。反应的平衡常数如下表:
CH3OH(g)。反应的平衡常数如下表:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
下列说法正确的是
A.该反应的△H >0
B.加压、增大H2浓度和加入催化剂都能提高CO的转化率
C.工业上采用5 ×103kPa和250℃的条件,其原因是原料气的转化率高
D. t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100
第II卷(非选择题,共58分)
8、(14分)A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
(1)元素D在周期表中的位置是
(2)G的基态原子电子排布式为 。
(3)B、C、D原子的第一电离能由小到大的顺序为 (用元素符号回答)
(4)CA3中心原子C的杂化类型是 ,分子的立体构型是 。
(5)向GSO4(aq)中逐滴加入氨水至过量,会观察到 现象。后一步反应的离子反应方程式为: 。
(6)某电池放电时的总反应为:Fe+F2O3+3H2O = Fe(OH)2+2F(OH)2(注:F2O3和F(OH)2为上面F元素对应的化合物),写出该电池放电时的正极反应式 。
9、(15分)ClO2是一种国际上公认的安全无毒的绿色水处理剂。回答下列问题:
(1)工业废水的处理:
 某实验兴趣小组通过下图装置,利用稀硫酸、KClO3和草酸溶液制备ClO2,并用它来处理含Mn2+的工业废水。
某实验兴趣小组通过下图装置,利用稀硫酸、KClO3和草酸溶液制备ClO2,并用它来处理含Mn2+的工业废水。
(2)ClO2易溶于水。用水吸收ClO2得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用cmol·L—1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL。
(已知2 Na2S2O3+ I2 = Na2S4O6+ 2NaI)
①滴定终点的判断依据是 。
②原ClO2溶液的浓度为 g / L(用步骤中的字母代数式表示)。
③若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果 (填“偏高”、“偏低”或“无影响”)
10、(14分)菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如下:

已知:
(1)A的结构简式为_________________,A中所含官能团的名称是_________。
(2)由A生成B的反应类型是______________,E的某同分异构体只有一种相同化学环境的氢,该同分异构体的结构简式为_________________。
(3)写出D和E反应生成F的化学方程式________________________。
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试剂任选)。
合成路线流程图示例:![]()
11、(15分)辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质。一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如下:

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
回答下列问题:
(1)浸取后得到的浸出液中含有CuSO4、MnSO4。写出浸取时产生CuSO4、MnSO4反应的化学方程式 。
(2)调节pH的目的是 ,pH的调节范围为 .
(3)生成MnCO3沉淀的离子方程式为 。
(4)操作A为 。
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═ 2Cu2O(s)+ 2SO2(g)△H=﹣768.2kJ/mol
2Cu2O(s)+ Cu2S(s)═ 6Cu(s)+ SO2(g)△H= +116.0 kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为 。
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损失Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6 kg这样的辉铜矿最多能制备
mol无水Cu(NO3)2。(计算结果精确到小数点后1位)
生物试卷
第I卷选择题
选择题:包括7小题,每小题6分,共42分。每小题只有一个选项符合题意。
1、下列相关叙述正确的是( )
A、性激素、叶绿素、生长素中含有N元素的一定是生长素
B、绿藻、黑藻、颤藻中没有叶绿体的一定是颤藻
C、线粒体、酵母菌、噬菌体中遗传物质是RNA的一定是线粒体
D、核糖体、质粒、酶中没有核糖参与组成的一定是酶
2、下列物质或者结构不是依赖离心法分离得到的是 ( )
A、较纯净的细胞膜 B、一些细胞器
C、噬菌体外壳和大肠杆菌 D、叶绿体中各种色素
3、一个以投饵养殖肉食性鱼类为主的鱼塘,由于管理不当,藻类爆发,引起沉水植物死亡,随后大量浮游动物和鱼类死亡,导致水体发臭。下列相关叙述错误的是( )
A、投放以浮游植物为食的鱼类可防止藻类的爆发
B、导致沉水植物死亡的最主要非生物因素是光照
C、流经该鱼塘的总能量是生产者所固定的太阳能总量
D、水生生物死亡加重了水体的污染,属于正反馈调节
4、如图为细胞中多聚核糖体合成分泌蛋白的示意图,已知分泌蛋白的新生肽链上有一段可以引导其进入内质网的特殊序列(图中P肽段)。下列相关说法正确的是 ( )

A、若P肽段功能缺失,可继续合成新生肽链但无法将蛋白质分泌到细胞外
B、合成①的场所在细胞核,⑥的合成与核仁无关
C、多个核糖体结合的①是相同的,但最终合成的肽链②③④⑤在结构上各不相同
D、若①中有一个碱基发生改变,则合成的多肽链结构一定会发生改变
 5、右图表示黄化燕麦幼苗中生长素相对含量的分布,根据所学知识和图中信息判断,下列叙述错误的是( )
5、右图表示黄化燕麦幼苗中生长素相对含量的分布,根据所学知识和图中信息判断,下列叙述错误的是( )
A.生长素主要在生长活跃的部位合成
B.a点生长素浓度相对较高是由于b、c点对应的细胞合成的生长素运输到a点所致
C.b点所对应的幼苗部位的细胞体积比a点所对应的幼苗部位的细胞体积大
D.如将a点对应浓度的生长素作用于d点细胞,可能会抑制d点细胞的生长
6、下图表示血糖调节的部分过程。a~d表示化学物质,E~K表示生理过程。有关叙述不正确的是( )
A、据图调节胰岛B细胞分泌的信号分子有a、c和葡萄糖
B、②可以是非糖物质转变为葡萄糖,过程K所起的作用是促进或者抑制
C、肝细胞和肌细胞都有激素c的受体
D、过程F、J传递物质a、d的载体分别是传出神经和体液
 7、如图为某动物细胞分裂示意图,则该细胞( )
7、如图为某动物细胞分裂示意图,则该细胞( )
A、一定发生过基因突变
B、只分裂产生一种生殖细胞
C、含有的6条染色体组成三个染色体组
D、G所在的染色体和g所在的染色体在遗传中遵循基因分离规律
第II卷(非选择题)本部分包括4小题,共计48 分。
8、(12分)如图所示,图l为某绿色植物细胞内部分代谢活动图解,其中①~⑤表示代谢过程,A~F表示代谢过程中产生的物质;图2为某植物在适宜的光照、CO2浓度环境中,在不同温度条件下的净光合作用速率和呼吸作用速率曲线。回答有关问题:
(1)图1中,F代表的物质是 ,物质B的移动方向是 。
(2)图1中,代表有氧呼吸中释放能量最多的过程 (填序号);图1中消耗【H】的生理过程有 (填序号)。
(3)光合作用和呼吸作用都受温度的影响,其中与 作用有关酶的最适温度更高,光合速率与呼吸速率相等时对应的温度是 ℃。
(4)若在20℃与37℃积累的有机物量相等,则37℃光反应产生的[H] (填“大于”“等于”或“小于”)20℃。当环境温度处于55℃~60℃时,与光合作用和呼吸作用两者相关的酶的活性情况是 。试分析高温抑制光合速率的原因(要求答对两点): 。
9、(11分)甲、乙、丙三个生物兴趣小组分别按如下三个流程进行课外探究活动,据此结合所学知识回答下列问题。
(1)甲组同学生产的果酒中带有一股醋酸味,可能的原因是: 。
(2)乙组同学欲按此原理生产蝴蝶兰组培苗,在愈伤组织形成的基础上要让其分化出根,应适当 (用升高或降低)培养基中细胞分裂素/生长素的比值。
(3)生物兴趣小组丙欲按上流程统计被原油污染的土壤中高效降解原油的某菌株的数量。其流程中对土壤液稀释的作用是: ;土壤样品稀释后应该采用 方法接种于以原油为唯一碳源的选择培养基上。)
(4)分析甲、乙、丙三组中“控制杂菌污染”最粗放仍能成功的是哪一组实验?
原因是什么? 。
10、(11分)肝细胞能将甲醛转化成甲酸而具有解除甲醛毒害的功能,研究人员为验证肝脏的这种解毒功能而进行了相关实验,实验分组设计如下表所示(“?”表示还没完成的实验步骤),右图为实验结果。

| 组别 | 培养环境 | 肝脏小块 (数目相同) |
| A组 | 含1.0mmol/L甲醛的肝脏培养液 | 有 |
| B组 | 含1.0mmol/L甲醛的肝脏培养液 | ? |
| C组 | 不含甲醛的肝脏培养液 | ? |
(1)表中,除A组外,还需放置肝脏小块的是 组。
(2)右上图中曲线 是C组实验的结果,说明肝细胞在代谢过程中会 。
(3)右上图中曲线乙是 组实验的结果,这说明 。
(4)研究发现一定浓度的甲醛可诱发染色体断裂,为进一步验证肝脏的解毒功能,研究人员同时进行了如下实验。方法步骤如下:
①取新培养的具有分裂能力的正常淋巴细胞悬液3等份,备用。
②按上表的实验设计培养肝脏15分钟后,取三组装置中的 ,分别加入备用的等量淋巴细胞悬液中继续培养一段时间。再分别取淋巴细胞染色、制片。然后在显微镜下观察 ,并对比分析。
③实验结果:添加了 组中的肝脏培养液的淋巴细胞出现异常,而其他两组的淋巴细胞正常。
 11、(14分)小鼠的体色黑色和白色是一对相对性状,由两对独立遗传的等位基因E和e、F和f控制,其体色与基因关系如图1。现用两只纯合小鼠杂交,结果如图2。请回答问题:
11、(14分)小鼠的体色黑色和白色是一对相对性状,由两对独立遗传的等位基因E和e、F和f控制,其体色与基因关系如图1。现用两只纯合小鼠杂交,结果如图2。请回答问题:
(1)通过图1说明基因与体色性状之间的关系是_____ 。
(2)根据图1和图2的杂交实验结果可判断E(e)基因位于__________(填“常”或“性”)染色体上。由图2杂交实验可判断出母本的基因型是__________。
(3)为进一步确定父本的基因型,让F1中的雌雄小鼠相互交配,观察并统计F2中黑色和白色的个体数量。预测实验结果及结论:
①若F2代中黑色 :白色约为________________,则基因型为_________________。
②若F2代中黑色 :白色约为________________,则基因型为_________________。
物理参考答案
选择题(本题共7小题.其中1—5题为单项选择题;6—7题为多项选择题,每题全部选对的得6分,选对但不全的得3分,有选错的得0分.)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 答案 | C | A | D | A | B | CD | BC |
8.(1)(每空3分)①顺时针,②逆时针
(2)①Ⅰ.不能多次测量;Ⅱ.超过电流表量程;Ⅲ.电压表量程太大,读数误差较大.
②Ⅰ.电流表量程太小;Ⅱ.②电压表量程太大;Ⅲ.变阻器调节作用太小.
③电路图见下图;
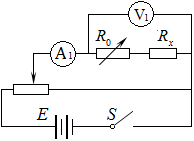
![]() ;UV是电压表V1示数,IA是电流表A1示数,R0是电阻箱示数.
;UV是电压表V1示数,IA是电流表A1示数,R0是电阻箱示数.
9.解:(1)物块沿斜面下滑的加速度为a,则有:
![]() (2分)
(2分)
∴![]() (2分)
(2分)
物块A刚滑上木板B时的速度
![]() (2分)
(2分)
(2)物块A在B上滑动时,
对A:![]() (1分)
(1分)
对B:![]() (1分)
(1分)
物块A刚好没有从木板B左端滑出,即:物块A在木板B左端时两者速度相等;
设经历时间t两者速度相等,速度关系:![]() (2分)
(2分)
物块A刚好没有从木板B左端滑出,位移关系:![]() (3分)
(3分)
解得:L=8m;t=2s; 2分
10.解:(1)线未断时,小球m处于平衡状态;
对小球m:![]() (2分)
(2分)
细线刚断时,小球的加速度![]() (2分)
(2分)
(2)小球恰好能完成竖直圆周运动,在P点:![]() (1分)
(1分)
又小球从C点到P点过程中,机械能守恒,则得:![]() (2分)
(2分)
∴![]()
小球在经过C点时,在C点左右两边相当于分别在半径为2R和R的两个圆周上过最低点;
过C点前:![]()
∴![]() (2分)
(2分)
过C点后:![]()
∴![]() (2分)
(2分)
则小球对轨道的压力之差为![]() (1分)
(1分)
(3)小球滑上左侧斜面轨道,压缩弹簧获得与初始线断时相同大小的加速度,弹簧弹力为
![]()
即弹簧压缩量与右侧初始弹簧压缩量相同,均为![]() (2分)
(2分)
弹簧的弹性势能相等;整个过程机械能守恒:![]()
解得![]() (3分)
(3分)
11.解:(1)回路中感应电动势E=BLv1分
导轨做初速度为零的匀加速运动v=at1分
回路中感应电动势随时间变化的表达式E=BLat1分
![]() 1分
1分
回路中总电阻![]() 1分
1分
回路中感应电流随时间变化的表达式![]() 2分
2分
(2)导轨受到外力F,安培力FA,摩擦力f;
![]() 1分
1分
![]() 1分
1分
由牛顿第二定律![]() 1分
1分
解得 1分
1分
上式中,当![]() ,即
,即![]() 时外力F取最大值 1分
时外力F取最大值 1分
所以![]() 2分
2分
(3)设此过程中导轨运动距离S由动能定理,W合=△Ek,W合=Mas1分
由于摩擦力Ff=μ(mg+FA),则摩擦力做功W=μmgS+μWA=μmgS+μQ2分
所以![]() 1分
1分
导轨动能的增加量![]() 2分
2分
化学试题答案
1—7: A C B C D B D
8、(14分)
(1)第二周期,VIA族(2分) (2)[Ar]3d104s1(2分)
(3)C<O<N(2分); (4)SP3(2分);三角锥形(2分);
(5)先产生蓝色沉淀,后沉淀消失,生成深蓝色透明溶液(2分)。
Cu(OH)2+4NH3·H2O = [Cu(NH3)4]2++2OH—+4H2O 或者Cu(OH)2+4NH3= [Cu(NH3)4]2++2OH—(2分);
(6)Ni2O3+3H2O+2e—=2Ni(OH)2+2OH—(2分)
9、(15分)
(1)①分液漏斗(1分),防倒吸(1分)
② H2C2O4+ H2SO4+2KClO3═ K2SO4+ 2CO2↑+ 2C1O2↑+ 2H2O(3分)
③ 2ClO2+5 Mn2++ 6H2O = 5 MnO2↓+ 2 Cl—+ 12H+(3分)
(2)①锥形瓶内溶液颜色由蓝色变为无色,且半分钟内无变化(2分)②135cV2/V1(3分)③偏高(2分)
10、(14分)
(1)![]() (2分),碳碳双键、醛基(2分)。
(2分),碳碳双键、醛基(2分)。
(2)加成(或还原)反应(2分);CH3![]() CH3(2分)
CH3(2分)
(3)![]() (3分)
(3分)
(4)CH3CH2Br![]() CH3CH2MgBr
CH3CH2MgBr CH3CH2CH2CH2OH(3分)
CH3CH2CH2CH2OH(3分)
11、(15分)
(1)2MnO2+ Cu2S + 4H2SO4= S↓+ 2CuSO4+ 2MnSO4+ 4H2O(3分)
(2)铁离子转化成氢氧化铁完全沉淀(1分) 3.2 ≤ pH <4.4 (1分)
(3)Mn2++ NH3+ HCO3﹣= MnCO3↓ + NH4+(2分)
(4)蒸发浓缩、冷却结晶(过滤)(2分)
(5)Cu2S(s)+ O2(g)═ 2Cu(s)+ SO2(g)△H=﹣217.4 kJ/mol(3分)
(6)14.3(3分)
生物参考答案
1、B 2、D 3、C 4、A 5、B 6、C 7、B
8、(1)丙酮酸 从叶绿体基质到类囊体薄膜
(2)③ ②③
(3)呼吸 40
(4)大于(2分) 光合作用相关的酶失活,呼吸作用相关的酶活性降低(2分) 在高温时避免水分减少,气孔关闭;酶在高温时活性降低甚至变性失活;高温破坏了叶绿体膜结构(2分)
9、(1)酒精发酵后期进入了空(氧)气,反应温度过高达到了30--35℃,导致醋酸杆菌大量生长产酸(满分2分,任意答出“进入了空(氧)气”“反应温度过高”其中的一条原因即给2分,其中温度这一项答出过高即可,不要求答出具体的范围;只答醋酸杆菌大量生长产酸给1分)
(2)降低(满分2分)
(3)使接种后能形成单菌落,便于后面计数(2分,答出单菌落即给2分)稀释涂布平板法(2分,填平板划线或其它方法均不给分)
(4)甲组(1分) 在缺氧,呈酸性的发酵液中绝大多数微生物因无法适应这一环境而受抑制(2分)
10、(1)C
(2)丙 产生(少量)甲醛(2分)
(3)A 肝脏具有解除甲醛毒害的功能(2分)
(4)等量肝脏培养液 染色体形态和数目 B(2分)
11、(1)基因通过控制酶的合成影响细胞代谢控制生物性状
(2)常 EEXfXf
(3)① 1:1 EEXFY ② 3:5 eeXFY