
最新!2022湖南物理高考真题及答案解析出炉
06月11日
2018届贵州省遵义市第四中学高三3月月考理科综合试题
可能用到的相对原子质量:H:1 Li:7 C:12 N:14 O:16 Mg:24 Si:28
第I卷
一、选择题:本题共13小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
1、下列关于细胞中物质和结构的叙述,正确的是
A、细胞中各种糖类可以为细胞的生命活动提供能量
B、脂质中的性激素进入细胞需要借助载体蛋白
C、细胞质基质呈胶质状态,其中含有将葡萄糖分解为丙酮酸的酶
D、真核细胞中溶酶体合成的多种水解酶能分解衰老、损伤的细胞器
2、下列关于细胞分裂及相关实验的说法,不正确的是
A、“低温诱导染色体加倍”实验的原理是低温能够抑制染色体着丝点分裂
B、植物有丝分裂末期,细胞板由细胞的中央向四周扩散,逐渐形成细胞壁
C、观察洋葱根尖细胞有丝分裂解离液能够使组织细胞分散开
D、进行有性生殖的生物,减数第一次分裂前期DNA分子数目和有丝分裂前期DNA分子数目相同
3、2017年的诺贝尔生理学或医学奖得主分离出了能够控制昼夜节律的period基因,它能够编码PER蛋白。另外发现,doubletime基因编码的DBT蛋白能够减缓PER蛋白在细胞中的积累,timeless基因编码的TIM蛋白与PER蛋白结合后进入细胞核,能够调节period基因的表达。下列叙述正确的是
A、同一生物体内,上述基因只存在于特定的细胞中
B、根据题干信息可推测,基因与生物性状之间存在一一对应关系
C、Period基因编码合成的PER蛋白直接从细胞核穿过核孔进入细胞质
D、PER蛋白在细胞核中积累从而抑制period基因的表达属于负反馈调节
4、植物激素对植物生命活动的调节起重要作用,下列关于植物激素的说法错误的是
A、横放植物的根向地生长体现了生长素的两重性
B、脱落酸和赤霉素对种子的萌发作用表现为相互拮抗
C、乙烯具有促进果实成熟的功能,植物各个部位可以合成乙烯
D、不同浓度的α—萘乙酸,吲哚丁酸等植物激素对植物的生长作用可能相同
5、下列关于种群和群落的叙述,正确的有几项
①种群内常因争夺食物而形成竞争关系 ②年龄组成能够对种群密度变化进行预测 ③种群“S”型曲线中,K/2时种群增长率最大 ④物种组成是区分群落的重要特征 ⑤植物的垂直结构为动物的分层现象提供了资源基础 ⑥初生演替中草本阶段比灌木阶段的群落自我调节能力弱
A、3项 B、4项 C、5项 D、6项
6、下列关于科学事实的叙述,错误的是
A、T2噬菌体侵染大肠杆菌实验中,理想条件下,35S标记组沉淀物不应该有放射性
B、罗伯特森通过电镜下观察细胞膜,提出了暗—亮—暗三层结构这个观点
C、摩尔根通过类比推理的方法得到了基因在染色体上的推论
D、萨克斯把绿叶半遮光半曝光处理,得出了光合作用产物有淀粉这一结论
7.化学与生活密切相关,下列说法错误的是( )
A.鲜花运输中保鲜可利用浸泡过高锰酸钾的硅土
B.压敏胶能牢固黏贴物品是利用了分子间作用力
C.“侯德榜制碱法”利用了强碱制备弱碱的原理
D.工厂静电除尘利用了某些胶体粒子的带电性
8.下列关于有机物的说法不正确的是( )
A.蔗糖在一定条件下能发生水解反应、氧化反应
B.苯丙氨酸和谷氨酸缩合最多可以形成3种二肽
C.蛋白质的颜色反应是指浓硝酸能使蛋白质变黄
D.油脂中的碳链含碳碳双键时主要是低沸点的植物油
9.有关海水资源的开发利用中各工业的某项操作叙述错误的是( )
| 工业体系 | 操作 | |
| A. | 镁工业:制备单质镁 | 用提纯得到的MgO加热熔融、电解得单质镁 |
| B. | 溴工业:制备单质溴 | 用SO2作吸收剂将Br2转化为HBr达到富集的目的 |
| C. | 淡水工业:制备蒸馏水 | 用太阳能将海水蒸发再液化得到初步的淡水 |
| D. | 氯碱工业:氢气、烧碱和含氯产品 | 用电解得到的Cl2和石灰水混合加工得到漂白粉 |
10.NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标况下11.2L 甲醇所含共价键数为5NA
B.1L 1mol/L葡萄糖溶液含有氧原子数为6NA
C.46g乙醇在金属铜催化下完全反应生成乙醛转移电子数为2NA
D.0.1L 12mol/L 浓硫酸与足量Zn完全反应标况下生成气体1.2NA
11.镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。放电时总反应为LiAO2+ nC = Li1-xAO2+ LixCn(0<x<1),工作原理如下图所示,则以下说法错误的是( )
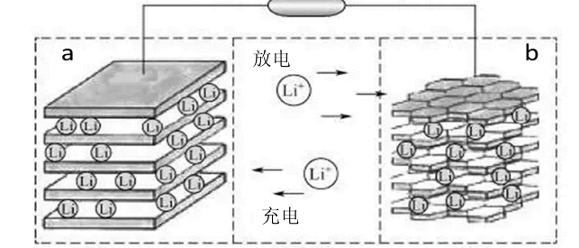
A.放电时Ni元素最先失去电子
B.放电时电子从a电极由导线移向b电极
C.充电时的阳极反应式为LiAO2-xe-= Li1-xAO2+xLi+
D.充电时转移1mol电子,理论上阴极材料质量增加7g
12.X、Y、Z、W为前20号依次递增的四种元素,X与Y能形成X2Y和X2Y2两种常温下呈液态的化合物,Z原子的原子序数为最外层电子数的3倍,等物质的量的单质W所含电子数为化合物X2Y电子数的两倍,则以下说法错误的是( )
A.氢化物的稳定性比Y>Z B.X2Y2的电子式为![]()
C.WY2 中既含有共价键又含有离子键 D.WX2能与X2Y反应生成X2
13.常温下,用0.100mol/L 的AgNO3溶液滴定50.0ml,0.0500mol/L KCl溶液,以K2CrO4为指示剂,测得溶液中pCl=-lgC(Cl-)、pAg=-lgC(Ag+)随加入AgNO3的体积变化如图所示,已知溶液中离子浓度小于等于1.0×10-5mol/L则沉淀完全,Ksp(Ag2CrO4)=2.0×10-12,Ksp(Ag2SO4)=1.4×10-5,下列说法错误的是( )

A.AgCl的沉淀溶解平衡常数Ksp数量级为10-10
B.为防止指示剂失效,溶液应维持中性或弱碱性
C.滴定中指示剂的有效浓度应维持在2.0×10-2mol/L
D.滴定完后加入1ml 0.01mol/L H2SO4会产生新的沉淀
二、选择题:本大题共8小题,每小题6分。在每题给出的四个选项中,第14~18题只有一项符合题目要求;第19~21题有多项符合题目要求,全部选对的得6分,选对但不全的得3分,有选错或不选的得0分。
 14. 如图所示,“伦敦眼”(The London Eye)是世界著名的观景摩天轮,它总高度135米(443英尺),屹立于伦敦泰晤士河南畔的兰贝斯区。现假设摩天轮正绕中间的固定轴做匀速圆周运动,则对于坐在座椅上观光的游客来说,正确的说法是( )
14. 如图所示,“伦敦眼”(The London Eye)是世界著名的观景摩天轮,它总高度135米(443英尺),屹立于伦敦泰晤士河南畔的兰贝斯区。现假设摩天轮正绕中间的固定轴做匀速圆周运动,则对于坐在座椅上观光的游客来说,正确的说法是( )
A.因为摩天轮做匀速转动,所以游客受力平衡
B.当摩天轮转到最高点时,游客处于失重状态
C.因为摩天轮做匀速转动,所以游客的机械能守恒
D.当摩天轮转到最低点时,座椅对游客的支持力小于所受的重力
15. 2016年“蛟龙”再探深海,前往太平洋、印度洋执行实验性应用航次。假设深海探测器在执行下潜任务中,探测器最后达到某一恒定的收尾速度。若探测器质量为m,由于重力作用下潜,探测器的收尾速度为v,探测器受到恒定的浮力F,重力加速度为g,下列说法正确的是( )
A.探测器达到收尾速度后,合力为向下
B.无论是达到收尾速度前,还是达到收尾速度后,探测器受到的合力都不能是零
C.探测器达到收尾速度前,受到的合力可能为零
D.探测器达到收尾速度后,探测器受到的水的阻力为mg-F
16. 如图所示为氢原子能级示意图,现有大量的氢原子处于n=4的激发态,当向低能级跃迁时辐射出若干不同频率的光,下列说法正确的是 ( )
 A.这些氢原子总共可辐射出3种不同频率的光
A.这些氢原子总共可辐射出3种不同频率的光
B.由n=2能级跃迁到n=1能级产生的光频率最小
C.用n=2能级跃迁到n=1能级辐射出的光照射逸出功为6.34 eV的金属铂能发生光电效应
D. 由n=4能级跃迁到n=1能级产生的光最容易表现出衍射现象
17. 2017年6月19日,我国在西昌卫星发射中心发射“中星9A”广播电视直播卫星,按预定计划,“中星9A”应该首先被送入近地点约为200公里,远地点约为3.6万公里的转移轨道Ⅱ(椭圆),然后通过在远地点变轨,最终进入地球同步轨道Ⅲ(圆形)。但是由于火箭故障,卫星实际入轨后初始轨道Ⅰ远地点只有1.6万公里。科技人员没有放弃,通过精心操作,利用卫星自带燃料在近地点点火,尽量抬高远地点的高度,经过10次轨道调整,终于在7月5日成功定点于预定轨道.下列说法正确的是( )
A.失利原因可能是发射速度没有达到7.9km/s
B.卫星从轨道Ⅰ的P点进入轨道Ⅱ后机械能增加
C. 卫星在轨道Ⅲ经过Q点时和在轨道Ⅱ经过Q点时的速度相同
D.卫星在轨道Ⅱ由P点向Q点运行时处于超重状态
18、两个点电荷Q1,Q2固定于x轴上,其中Q2位于坐标原点0.将一带正电的试探电荷从足够远处沿x轴方向移近Q2(位于坐标原点O),在移动过程中,试探电荷的电势能随位置的变化关系如图所示,曲线与x轴的交点为M,曲线的最低点为N,则下列判断正确的是( )
A.M点电势为零,N点场强不为零
B.M点场强为零,N点电势为零
C. Q1带正电,Q2带负电,且Q2电荷量较小
D. Q1带负电,Q2带正电,且Q2电荷量较小
19、如图所示,M是一小型理想变压器,接线柱a、b接在电压u=311sin314t(V)的正弦交流电源上,变压器右侧部分为一火警报警系统原理图,其中R2为用半导体热敏材料制成的传感器,其阻值随温度的升高而减小.电流表A2为值班室的显示器,显示通过R1的电流,电压表V2显示加在报警器上的电压(报警器未画出),R3为一定值电阻.当传感器R2所在处出现火警时,以下说法中正确的是( )
A.变压器的输入功率增大
B. 变压器的输入功率不变
C. V1的示数不变,A1的示数增大
D.V2,A2的示数都减小
20、如图所示,在光滑绝缘水平面上有一半径为R的圆,AB是一条直径,
空间有匀强电场场强大小为E,方向与水平面平行.在圆上A点有一发
射器,以相同的动能平行于水平面沿不同方向发射带电量为+q的小球,
小球会经过圆周上不同的点,在这些点中,经过C点的小球的动能最大.
由于发射时刻不同时,小球间无相互作用.且∠α=30°,下列说法正
确的是( )
21、如图在x轴上方存在垂直纸面向里的磁感应强度为B的匀强磁场,x轴下方存在垂直纸面向外的磁感应强度为![]() 的匀强磁场.一带负电的粒子从原点0以与x轴成30°角斜向上射入磁场,且在上方运动半径为R则( )
的匀强磁场.一带负电的粒子从原点0以与x轴成30°角斜向上射入磁场,且在上方运动半径为R则( )
A.粒子经偏转一定能回到原点O
B.粒子完在成一次周期性运动的时间为![]()
C.![]()
D.粒子第二次射入x轴上方磁场时,沿x轴前进了3R
第Ⅱ卷
三、非选择题:包括必考题和选考题两部分。第22题~第32题为必考题,每个考题考生都必须作答,第33~38为选考题,考生根据要求作答。
22.(5分, 每空1分)某实验小组用如图1所示的装置探究动能定理,并测量当地的重力加速度.将小钢球从固定轨道倾斜部分某处由静止释放,经轨道末端水平飞出,落到铺着白纸和复写纸的水平地面上,在白纸上留下点迹.为了使问题简化,小钢球在轨道倾斜部分下滑的距离分别为L、2L、3L、4L…,这样在轨道倾斜部分合外力对小钢球做的功就可以分别记为W0、2W0、3W0、4W0…
(1)为了探究动能定理,除了测量小钢球离开轨道后的下落高度h和水平位移s外,还需测量________.
A.L、2L、3L、4L…的具体数值
B.轨道与小钢球之间的动摩擦因数μ
C.小钢球的质量m
(2)请用上述必要的物理量写出探究动能定理的关系式:
W=________;
 (3)为了减小实验误差必须进行多次测量,在L、2L、3L、4L…处的每个释放点都要让小钢球重复释放多次,在白纸上留下多个点迹.那么,确定在同一位置释放的小钢球在白纸上的平均落点位置的方法是________________________;
(3)为了减小实验误差必须进行多次测量,在L、2L、3L、4L…处的每个释放点都要让小钢球重复释放多次,在白纸上留下多个点迹.那么,确定在同一位置释放的小钢球在白纸上的平均落点位置的方法是________________________;
图2
(4)该实验小组利用实验数据得到了如图2所示的图象,则图象的横坐标表示________(填“s”或“s2”).若该图线的斜率为k,则当地的重力加速度g=________(用题中相关的物理量表示).23.(10分,每空2分)某同学要测量一个改装后的电压表Vx的量程和内阻,实验过程如下:
(1)先用多用电表粗测电压表的内阻和量程,实验中多用电表红表笔应与电压表_____(填“正”或“负”)接线柱相连;若已知多用电表内电源电动势为9V,所用档位为“×1K”档,调零后测量,指针位置如图所示.此时电压表指针指在表盘的四分之三刻度处.则所测电压表内阻约为___________,量程为____________.

(2)若电压表量程为(1)问中所测数值,则为了精确测量其内阻,现提供以下器材:
待测电压表Vx
电流表A(量程0.6A,内阻约为3Ω)
电压表V(量程l0V,内阻约为30kΩ)
定值电阻R0(阻值为10kΩ)
滑动变阻器R1(最大阻值为5Ω,额定电流为1A)
滑动变阻器R2(最大阻值为100Ω,额定电流为lA)
电源E(电动势为15V,内阻约为1Ω)
开关和导线若干
①为了较精确的测量电压表内阻,则测量电路应该选择如下电路中的________.

②写出电压表内阻测量值的表达式Rv=_________.
24.(12分)光滑水平面上有一足够长的木板质量为M,另一质量为m的滑块,以速度![]() 从左端滑上木板,足够小滑块与木板间的动摩擦因数为
从左端滑上木板,足够小滑块与木板间的动摩擦因数为![]() 。求:
。求:
⑴木板最终的速度;
⑵滑块相对木板运动的时间。
25.(20分)如图25-1所示,平行金属轨道![]() 、
、![]() 所在的平面与水平面的夹角
所在的平面与水平面的夹角![]() ,轨道宽度
,轨道宽度![]() 。轨道处在垂直轨道平面向下的匀强磁场中,磁感应强度随时间变化的关系如图25-2所示。轨道底端接有电阻
。轨道处在垂直轨道平面向下的匀强磁场中,磁感应强度随时间变化的关系如图25-2所示。轨道底端接有电阻![]() ,轨道电阻不计。放在轨道上距底端
,轨道电阻不计。放在轨道上距底端![]() 处,垂直于轨道一金属棒
处,垂直于轨道一金属棒![]() ,其质量
,其质量![]() ,电阻
,电阻![]() 。从
。从![]() 时释放金属棒,在前
时释放金属棒,在前![]() 的时间内,金属棒在1s末恰好保持静止。
的时间内,金属棒在1s末恰好保持静止。
(![]() ).
).
求:⑴ 在前![]() 的时间内金属棒中的电流大小及方向;
的时间内金属棒中的电流大小及方向;
⑵ 金属棒与轨道间的动摩擦因数(最大静摩擦力等于滑动摩擦力);
⑶ 如果金属棒滑到底端时恰好达到最大速度,从![]() 开始到金属棒滑到底端的全过程中,电阻
开始到金属棒滑到底端的全过程中,电阻![]() 产生的热量及流过电阻
产生的热量及流过电阻![]() 的电荷量。
的电荷量。
26.(13分)某课外活动小组根据镁与CO2的反应设计实验探究镁与NO2的反应。
甲同学推测产物是MgO和N2;
乙同学推测产物除了MgO和N2外,固体中还可能含有Y。
该小组同学设计了以下装置探究镁与NO2反应的固体产物,并测定其组成。
 (1)实验开始时,先关闭止水夹后打开弹簧夹,再打开分液漏斗活塞,当硬质玻璃管充满红综色气体后,打开止水夹,关闭弹簧夹,最后点燃酒精灯。这样做的目的是
(1)实验开始时,先关闭止水夹后打开弹簧夹,再打开分液漏斗活塞,当硬质玻璃管充满红综色气体后,打开止水夹,关闭弹簧夹,最后点燃酒精灯。这样做的目的是
(2)装置B中的试剂可以选用
A、浓硫酸 B、无水氯化钙 C、五氧化二磷 D、碱石灰
(3)装置C中盛装氢氧化钠溶液的作用是:
(4)为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是①气体恢复至室温再读数;② ;③ 。
(5)实验结束后,同学们将固体产物取出与水反应,发现有刺激性气味的气体产生,该气体能使湿润的石蕊试纸变蓝。说明乙组同学推测正确,请写出Y与水反应的化学方程式
(6)若初始加入镁粉质量为3.6 g,在足量的NO2中充分反应后 ,收集到N2体积为448ml (标准状况),则产物中MgO的质量是
27.(15分)硅是最理想的太阳能电池材料,高性能晶硅电池是建立在高质量晶硅材料基础上的。工业上可以用如图所示的流程制取高纯硅。
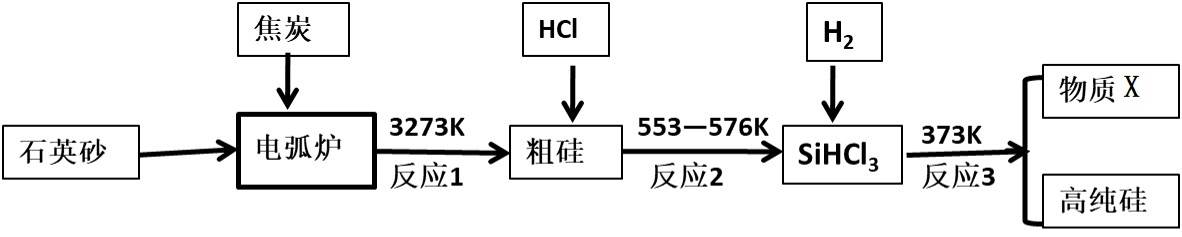
(1)硅在周期表中的位置是 ,反应1中氧化剂与还原剂的物质的量之比为:
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点31.8℃)中含有少量SiCl4(沸点57.6℃)和SiH2Cl2(沸点8.2℃)、SiH3Cl(沸点-30.4℃)提纯SiHCl3采用的方法为 ,整个过程中可以循环利用的物质X是: (填化学式)
(3)提纯粗硅的过程中必须严格控制无水无氧,原因之一是硅的卤化物极易水解,写出SiCl4遇水剧烈反应的化学方程式
(4)硅在有HNO3存在的条件下,可以与HF生成H2SiF6,同时有不溶于水的气体生成,该气体遇空气变为红棕色,硅单质发生的化学方程式为
(5)某工厂用100吨纯度为75%的石英砂为原料经第一步反应制得的粗硅中含硅28吨,则该过程中硅的产率是: (精确到小数点后两位)
28.(15分)I用CO2和氢气制备甲醇是解决能源危机的方向之一。
已知:2H2(g)+CO(g) ⇌ CH3OH(g) △H1= -90.7kJ/mol
2CH3OH(g) ⇌ CH3OCH3(g)+H2O(g) △H2= -23.5 kJ/mol
3CO(g)+3H2(g) ⇌ CH3OCH3(g)+CO2(g) △H3= -246.4 kJ/mol
⑴则CO2与氢气合成甲醇的热化学方程式为:
T℃时,将4molCO2与10mol H2通入1L密闭容器中,时间t与甲醇物质的量的关系见下表
| 时间t/h | 0 | 2 | 4 | 6 | 8 | 10 |
| n(甲醇)/mol | 0 | 1.4 | 2.3 | 2.8 | 3.0 | 3.0 |
回答下列问题:
⑵欲提高氢气的平衡转化率,应采取的措施为 (任意写两种)
⑶该温度下,反应的平衡常数K=
II 采用如下装置电解亚硫酸钠亦可制备硫酸与氯碱工业的一种产物

⑷A、B池中的电解质溶液应该是 、 ,a为 离子交换膜。
⑸写出B池发生的电极反应式
(6)Na2SO3溶液中离子浓度由大到小的排列顺序为
29、在适宜温度和光照条件下,把小球藻培养在一定浓度的NaHCO3溶液和一定量的葡萄糖溶液中。在实验过程中按图示顺序在d、e点依次向培养液中加入适量的线粒体和酵母菌个体,对应时间内测定整个装置中氧气浓度的变化,结果如图所示。请回答下列问题:

30、某种新型病毒感染人体后,人体可以出现发热、打喷嚏、食欲不振等症状。请回答下列问题:
(1)病毒进入人体后,作为_________可诱导B淋巴细胞增殖分化为_______和记忆细胞。
(2)人体之所以会发热是因为当机体感知到致病细菌侵入后,一方面病人的骨骼肌战栗加大产热,一方面引起__________激素分泌增多,促进细胞代谢加快,体温升高。该激素在人体内的分泌存在_________和________调节机制。
(3)病毒刺激人的鼻粘膜人会打喷嚏。人的鼻粘膜参与的免疫属于______________免疫,其特点是_____________________________。
(4)感染该病毒后,人体内分泌系统、神经系统、免疫系统都努力工作,以维持机体的稳态。人体内的激素和神经递质在作用过程中所具有的共同特点_________________________(答出一点)。
31、下图为某鱼塘能量流动图(能量单位是J·m-2·a-1),其中c,d,f为不同鱼种。请回答下列问题:

(1)图中各生物间能量流动的数据是在 层次上进行研究得到的。小鱼c和中鱼d的关系是 。
(2)图中各生物的同化量的共同最终去向是 。第一营养级到第二营养级的能量传递效率是 。
(3)大鱼f排出的粪便中所含的能量 (填“包含”或“不包含”)在从中鱼d流入大鱼f的126J·m-2·a-1中。如果市场行情有较大变化,中鱼d经济价值剧增,该鱼塘应如何获得较大的经济价值? 。
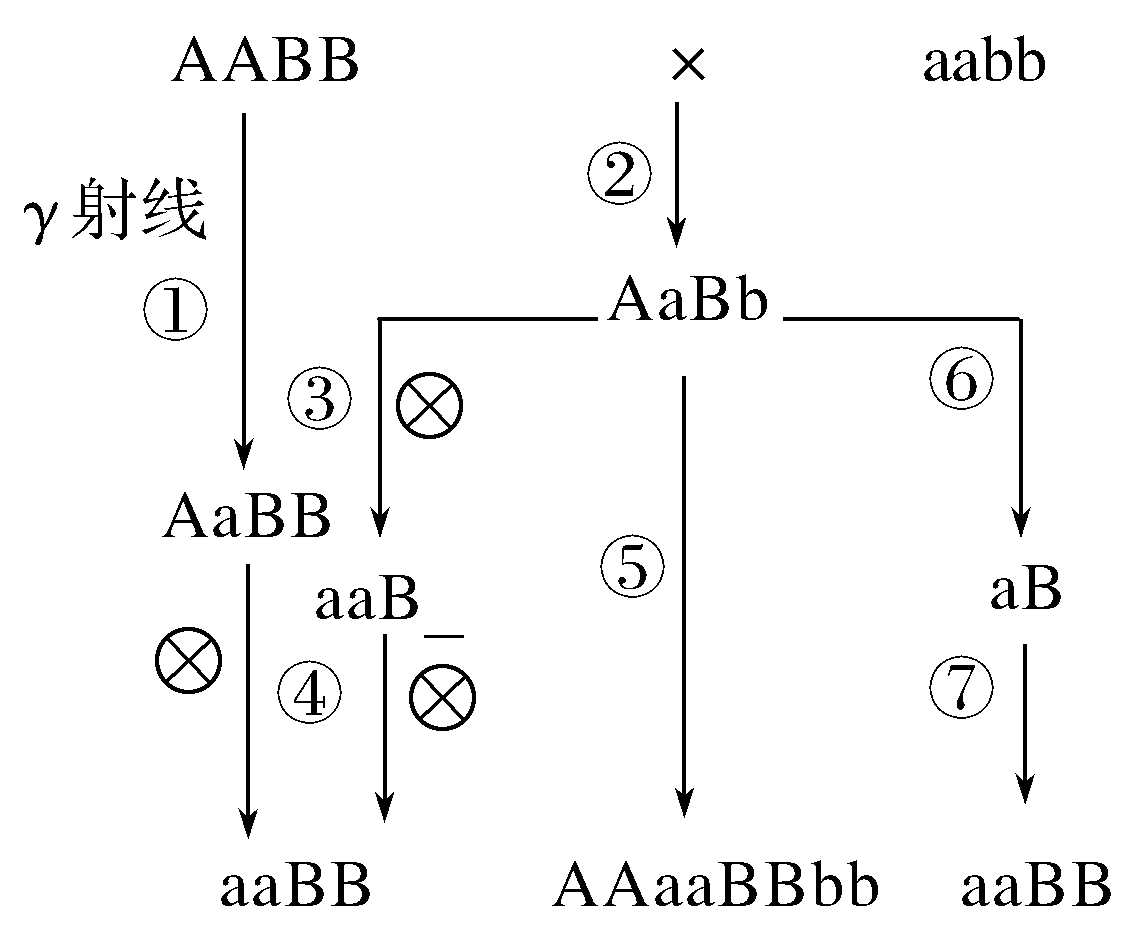
32、假设a、B为玉米的优良基因,现有AABB、aabb两个品种,控制两对相对性状的基因位于两对同源染色体上,实验小组用不同方法进行了实验(如图)。
 (5分)分子力F、分子势能Ep与分子间距离r的关系图线如图所示(取无穷远处分子势能Ep=0)。若甲分子固定于坐标原点O,乙分子从某处(分子间的距离大于r0小于10r0)静止释放,在分子力的作用下沿r正半轴靠近甲。(填正确答案标号。选对1个得2分,选对2个得4分,选对3个得5分。每选错1个扣3分,最低得分为0分)
(5分)分子力F、分子势能Ep与分子间距离r的关系图线如图所示(取无穷远处分子势能Ep=0)。若甲分子固定于坐标原点O,乙分子从某处(分子间的距离大于r0小于10r0)静止释放,在分子力的作用下沿r正半轴靠近甲。(填正确答案标号。选对1个得2分,选对2个得4分,选对3个得5分。每选错1个扣3分,最低得分为0分) (2) (10分) 如图所示,汽缸A和B的活塞用硬杆相连,活塞的横截面积SA=2SB,两活塞距离底部均为h,汽缸壁用导热材料做成,此时环境温度为300 K,外界大气压为p0,汽缸B内的压强p2=0.5p0.问:
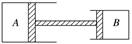 (I)此时汽缸A内气体的压强为多少?
(I)此时汽缸A内气体的压强为多少?
(II)若保持汽缸B中的气体温度不变,把汽缸A缓慢加热,加热至温度多高活塞才移动![]() h?
h?
(1)(5分)一简谐横波沿x轴正向传播,t=0时刻的波形如图(a)示,x=0.10m处的质点的振动图线如图(b)所示,已知该波的波长大于0.10m。下列正确的是(选对1个的2分,选对2个的4分,选对3个的5分。每选错没错1个扣3分,最低得分为0分)
A x=0.10m处质点在t=0时刻向上振动。
B 波长为0.30m。
C 波速为0.125m/s。
D 波的频率为2.4HZ。
E 若该波遇到宽为0.33m障碍物,不能发生明显的衍射现象。
(2)如图所示,一柱形玻璃的横截面是半径为R的![]() 圆,圆心为O,以O为原点建立直角坐标系Oxy.一单色光平行于x轴射入玻璃,入射点的坐标为(0,d),单色光在玻璃中的折射率为
圆,圆心为O,以O为原点建立直角坐标系Oxy.一单色光平行于x轴射入玻璃,入射点的坐标为(0,d),单色光在玻璃中的折射率为![]() ,不考虑单色光经圆弧面反射后的情况.
,不考虑单色光经圆弧面反射后的情况.
①当d多大时,该单色光在圆弧面上刚好发生全反射?
②当d→0时,求该单色光照射到x轴上的坐标.(θ很小时,![]() ,)
,)

35.(物质结构 15分)氮及其化合物广泛存在于自然界中,回答下列问题:
⑴基态氮原子核外有种不同运动状态的电子 ,其价层电子排布图为
⑵NH4NO3中元素的第一电离能大小关系:N O,NO3-的空间构型为 ,NH4+中氮原子的杂化类型为
⑶HCN分子中含 个σ和个π键。与CN-互为等电子体的分子和离子分别为和(各举一例,填化学式)
⑷NH3极易溶于水,其主要原因是
⑸立方氮化硼的结构与金刚石相似,其晶胞如图所示,B原子周围最近的N原子所构成的立体图形为,一个晶胞中N原子数目为

36.(有机化学 15分)席夫碱类化合物G有机合成、药物、新材料等方面有广泛应用。合成G的一种路线如下:
C8H17Cl
![]()
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
![]()
回答下列问题:
⑴B的化学名称 ,A生成B的化学方程式
⑵A 生成B , E 生成F的反应类型分别是 ,
C+F 生成G的化学方程式
⑶E的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的共有 种,其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为 (任意写一种)
⑷已知![]() 请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线
请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线
(1)培养基中的乳糖可以为大肠杆菌提供 。为了方便大肠杆菌的鉴定,需要在培养基中添加成分X ,在该培养基表面,大肠杆菌的菌落呈现 (填颜色)。为了完成步骤二,该培养基中的成分Y通常是 。
(2)完善步骤三,①是 ,②是 。
(3)若该小组在空白对照组的平板上检测到少许菌落,请分析可能的原因: 。
(4)将1mL冰块水样稀释100倍,在3个平板上用涂布法分别接入0.1mL稀释液;经适当培养后,3个平板上的菌落数分别为39、38和37,据此可得出每升水样中的活菌数为 。
38.【生物——选修3:现代生物科技专题】(15分)
转基因抗病香蕉的培育过程如图1所示,图2表示PstⅠ、SmaⅠ、EcoRⅠ和ApaⅠ四种限制酶的识别序列及酶切位点。请据图回答下列问题:
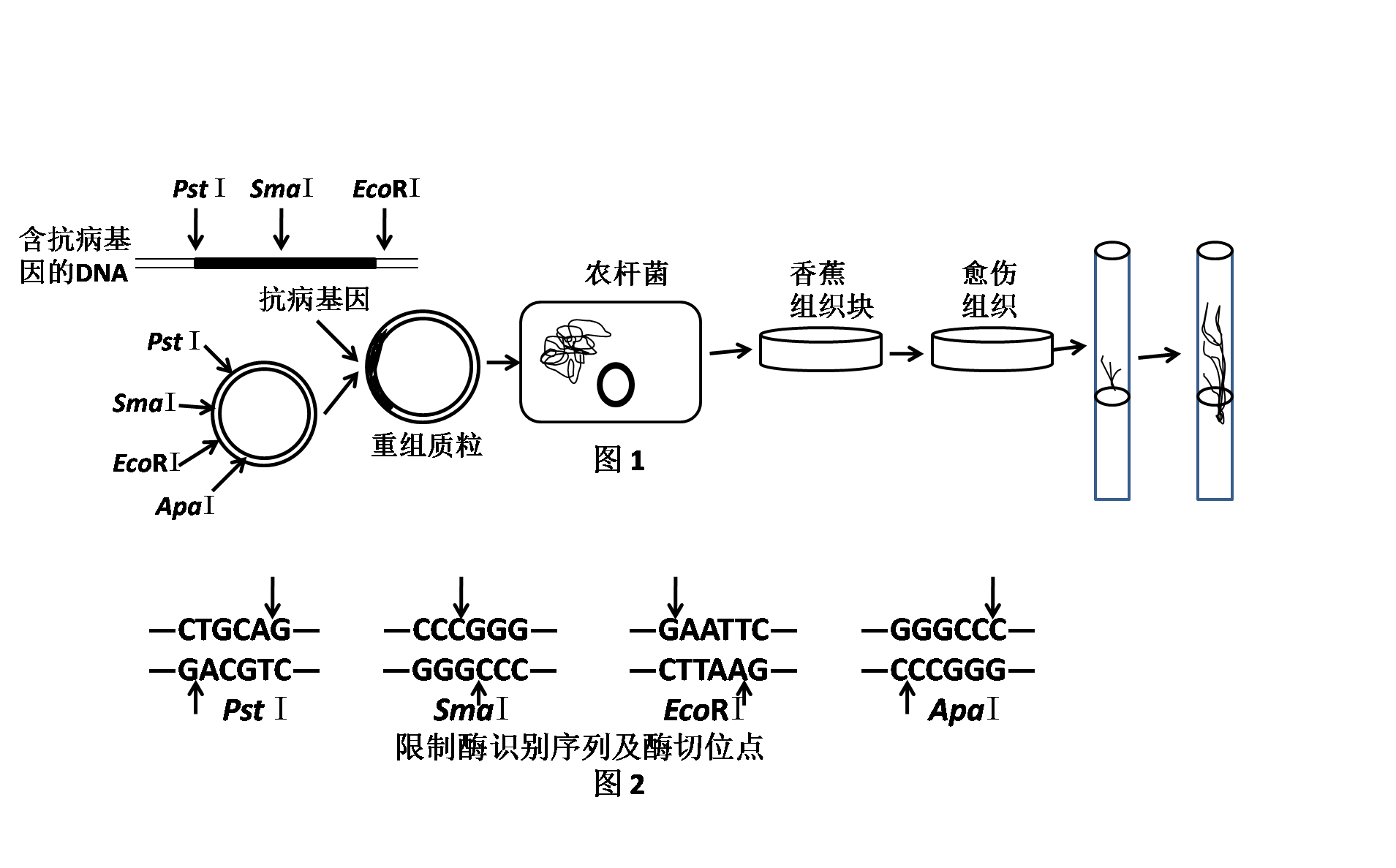 (1)图中限制酶切割DNA时破坏的是两个______________之间的化学键。
(1)图中限制酶切割DNA时破坏的是两个______________之间的化学键。
(2)在构建图1中的重组质粒时要保证目的基因被连接在质粒上特定的 和终止子之间才能保证目的基因在受体细胞中被成功 。
(3)将抗病基因从含抗病基因的DNA中切割下来,使用的限制酶是______________,同时也应该用相同的酶对质粒进行切割,这样处理的原因是 。请写出单独用PstⅠ切割质粒后的片段: 。
(4)转基因抗病香蕉的培育是否发生了可遗传变异? 。药物A会抑制香蕉愈伤组织细胞的生长,根据这一原理可以利用含药物A的培养基筛选已导入重组质粒的香蕉细胞。由此推断,重组质粒中应含有 基因作为标记基因。
化学答案
7、C 8、B 9、A 10、C 11、C 12、B 13、D
26题 共13分
27题 共15分
28题 共15分
35题 共15分

生物答案
选择题:CADDBC
(1)小球藻的光合速率等于呼吸速率
(4)单倍体育种 花药 0
37、(除说明外,每空2分,共15分)
(1)碳源(1分) 伊红美蓝 黑色 琼脂
(2)适量无菌水 等量冰块水
(3)培养基灭菌不合格或倒平板(接种)过程被污染
(答一点即得分,其他合理也给分)
(4)3.8×107
38、(除说明外,每空2分,共15分)
(1)脱氧(核糖)核苷酸(2分)
(2)启动子(2分) 转录(或者填表达)(2分)
(3)PstⅠ和EcoRⅠ(2分) 用相同的酶切割质粒才能产生与目的基因相同的末端,便于二者进行拼接(2分)
如下图:(2分)
G………CTGGA
AGGTC………G
(4)是(1分) 抗药物A(2分)
物理答案
二、选择题:
14. B 15. D 16.C 17. B 18、D 19、ACD 20、AC 21、CD
三、非选择题:共15分。第22~23题为必考题,每个试题考生都必须作答。22题共5分,每空1分,23题共10分,每空2分。
22. (1)C (2) (3)用尽可能小的圆圈住所有落点,圆心即为平均落点的位置
(4)s2
23. 负 15kΩ 6V D ![]()
四、计算题
24.(1)![]() --------------3分
--------------3分
![]() ----------------------2分
----------------------2分
(2)![]() ----------4分
----------4分
![]() ---------------3分。
---------------3分。
25.⑴![]() -------------2分
-------------2分
![]() --------------1分
--------------1分
电流方向B到A;--------------1分
⑵![]() --------2分
--------2分
![]() ----------------------1分
----------------------1分
![]() --------------------------------------1分
--------------------------------------1分
⑶ 达到最大速度时;![]() ---------1分
---------1分
![]() ----------------------1分
----------------------1分
![]() -----------------------1分
-----------------------1分
![]() -----------------------1分
-----------------------1分
![]() ----------------2分
----------------2分
![]() ---------------------------------------1分
---------------------------------------1分
![]() -----------------1分
-----------------1分
![]() -----------------------------------------1分
-----------------------------------------1分
![]() ------------------------------------2分
------------------------------------2分
![]() ----------------------------1分
----------------------------1分
33.(1) A C D
(2)
(2)0.75p0 600 K
(I)要求汽缸内封闭气体的压强,应分析活塞整体,通过受力分析,根据共点力平衡条件求解.活塞整体受力分析如图所示.
![]()
根据共点力平衡有p0SB+p1SA=p0SA+p2SB,………….3分
解得p1=0.75p0. 1分
(II)将汽缸A加热过程中,A、B两部分气体状态变化满足理想气体状态方程,终态时活塞整体仍满足共点力平衡条件.
对气体A有![]() =
=![]() 3分
3分
对气体B有p2hSB=0.5hSBp2′ 1分
根据活塞平衡p0SB+p1′SA=p0SA+p2′SB3分
解得T′=600 K. 1分
44.(1)ABC
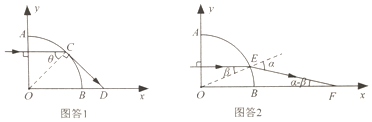
(2) (i)如图答图1,当光射到圆弧面上的入射角等于临界角C时刚好发生全反射,则
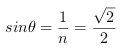 -------------------- 3分
-------------------- 3分
计算得出![]() -----------------------1分
-----------------------1分
根据几何关系得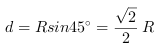 ------------2分
------------2分![]() 如图答2,当射到圆弧面上的入射角很小时,设折射角为
如图答2,当射到圆弧面上的入射角很小时,设折射角为![]() ,入射角为
,入射角为![]() ,由折射定律得:
,由折射定律得:
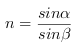 --------------------------------1分
--------------------------------1分
在![]() 中,由正弦定理得
中,由正弦定理得 ------------1分
------------1分
当d→0时,![]() ,则得
,则得![]() ,
,![]() -------------- 1分
-------------- 1分
联立计算得出![]() ------------------------- 1分
------------------------- 1分