
最新!2022湖南物理高考真题及答案解析出炉
06月11日
重庆市巴蜀中学校高2016级高三第三次月考
理科综合能力测试
注意事项:
1、本试卷分为第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的姓名、考生号填写在答题卡上。
2、回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号,答在本试卷上无效。
3、回答第II卷时,将答案写在答题卡上。写在本试卷上无效。
4、考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:Li﹣7 C﹣12 F﹣19 P﹣31 Fe﹣56 Cu﹣64
第I卷
一、选择题:本题共13小题,每题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列有关组成生物体化学元素及化合物的说法正确的是
A.P是组成磷脂、ATP、RNA及核糖等多种化合物的组成元素
B.Mg是叶绿体中各种色素分子必不可少的组成元素
C.ATP和DNA中都含有腺嘌呤和脱氧核糖
D.RNA既可作为遗传信息的载体,也可催化某些生物化学反应
2.下图是真核细胞膜亚显微结构模式图,①~③表示构成细胞膜的物质。下列有关说法错误的是
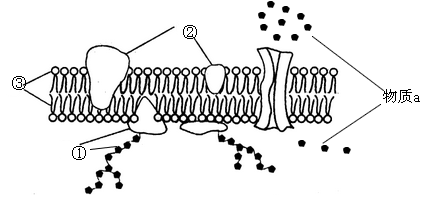
A.细胞膜的基本骨架是③,5种类和数量的多少与细胞膜功能的复杂程度有关
B.癌细胞中①物质减少,导致癌细胞彼此之间的黏着性显著降低,容易在体内分散和转移
C.物质a通过细胞膜由细胞外进入细胞内的方式是主动运输
D.①②③在细胞膜上的位置并不是静止不动的,这说明细胞膜的功能特点是具有流动性
3.关于细胞的分化、衰老、凋亡与癌变,下面选项中表述正确的是
A.胚胎细胞中不存在与细胞凋亡有关的基因
B.原癌基因或抑癌基因发生多次变异积累可导致癌症,因此癌症是可遗传变异
C.衰老细胞内有些酶的活性会升高,但呼吸速率减慢
D.RNA聚合酶基因和生长激素基因在动物各题所有细胞中都会表达
4.下列科学实验描述错误的是
A.巴甫洛夫是近代消化生理学奠基人、诺贝尔奖获得者,他和他的学生通过实验发现并证明了促胰液素的存在
B.观察根尖分生组织细胞有丝分裂实验中解离的目的是使细胞相互分离开来
C.探究酵母菌细胞呼吸方式的实验中,无法根据CO2是否产生来判断其呼吸方式
D.科学家卡尔文用标记的二氧化碳供一种单细胞的绿藻进行光合作用,最终探明了二氧化碳中的碳转化为有机物中碳的途径
5.如图表示人体内的细胞与外界环境之间进行物质交换的过程。下列叙述错误的是

A.①~③分别代表血液、淋巴和组织液,它们属于人体内环境
B.人体剧烈运动后,①中的pH将会由弱碱性变成酸性
C.①中渗透压的大小主要与无机盐、蛋白质的含量有关
D.当人体出现过敏时,③中的液体可能会增多
6.血糖浓度保持平衡对机体生命活动具有重要作用,下图为胰岛素作用机理模式图。下列说法正确的是
A.胰岛素作为信息分子,可直接参与细胞内的代谢过程
B.胰岛素受体由α亚基和β亚基组成,图中β亚基可能属于ATP合成酶
C.胰岛素可以通过调控细胞膜上葡萄糖转运蛋白的数量来调节血糖的浓度
D.葡萄糖转运蛋白合成障碍者,可通过注射胰岛素进行治疗
7.下列说法中正确的是
A.食品中大量添加苯甲酸钠等防腐剂,可有效延长其保质期
B.利用丁达尔效应可区别淀粉溶液和NaCl溶液
C.明矾能水解生成Al(OH)3胶体,可用作饮用水消毒杀菌
D.石油分馏属于化学变化
8.下列各组离子在指定溶液中能大量共存的是
A.强碱性溶液:Mg2+、NH4+、Cl﹣、NO3﹣
B.使甲基橙变红的溶液:Na+、Fe3+、Cl﹣、S2O32﹣
C.无色溶液中:K+、Al3+、HCO3﹣、Cr2O72﹣
D.常温下,c(H+)/c(OH﹣)=1×10﹣12的溶液:K+、Na+、AlO2﹣、CO32﹣
9.下列说法正确的是
A.乙醇既可以发生催化氧化反应,又可以发生酯化反应
B.用溴水可以鉴别乙醇、乙酸和苯
C.糖类、油脂、蛋白质三类物质都只含有C、H、O三种元素
D.C5H10O属于醛类的同分异构体为六种
10.下列判断正确的是:
A.原子半径:S>O>NB.沸点:H2O>HF>H2S
C.离子半径:Cl﹣>Al3+>Mg2+D.还原性:I﹣>S2﹣>Br﹣
11.关于下列图示的说法中正确的是




① ② ③ ④
A.图①装置用于分离沸点相差较大的互溶液体混合物
B.图②装置用于研究不同催化剂对反应速率的影响
C.图③中电流计的指针发生偏转,石墨为正极
D.图④装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯
12.常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是:
A.某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10﹣2mol/L
B.0.1mol/L﹣1的KHA溶液,其pH=10,c(K+)>c(A2﹣)>c(HA﹣)>c(OH﹣)
C.等体积、等物质的,量浓度的Na2CO3溶液与NaHCO3溶液混合:
3c(Na+)=2c(CO32﹣)+2c(HCO3﹣)+2c(H2CO3)
D.将0.2mol·L﹣1的某一元酸HA溶液和0.1mol·L﹣1NaOH溶液等体积混合后溶液pH>7,则反应的混合液中:c(HA)>c(Na+)>c(A﹣)
 13.一定条件下合成乙烯:6H2(g)+2CO2(g)
13.一定条件下合成乙烯:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂效率的影响如图,下列说法不正确的是
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂效率的影响如图,下列说法不正确的是
A.生成乙烯的速率:v(M)有可能小于v(N)
B.平衡常数:KM>KN
C.当温度高于250℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低
D.若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7%
二、选择题:第14~17题只有一项符合题目要求,第18~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。
 14.如图所示的电路中,电源的输出电压恒为U。电动机M的线圈电阻与电炉L的电阻相同,电动机正常工作,在相同的时间内,下列判断正确的是
14.如图所示的电路中,电源的输出电压恒为U。电动机M的线圈电阻与电炉L的电阻相同,电动机正常工作,在相同的时间内,下列判断正确的是
A.电炉放出的热量大于电动机放出的热量
B.电炉两端的电压小于电动机两端的电压
C.电炉两端的电压等于电动机两端的电压
D.电动机消耗的电功率等于电炉消耗的电功率
15.如右图所示,固定光滑细杆与地面的倾角为α,在杆上套有一个光滑小环,小环在水平拉力F作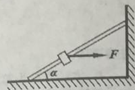 用下向上匀速运动,则杆受到小环压力的大小为
用下向上匀速运动,则杆受到小环压力的大小为
A.![]() B.
B.![]()
C.![]() D.
D.![]()
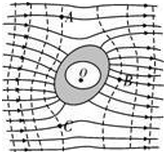
 16.如图,正点电荷放在O点,图中画出了该电荷电场的八条对称分布电场线。以其中一条电场线上的O’点为圆心画一个圆,与电场线分别相交于点a、b、c、d、e和f,下列说法正确的是
16.如图,正点电荷放在O点,图中画出了该电荷电场的八条对称分布电场线。以其中一条电场线上的O’点为圆心画一个圆,与电场线分别相交于点a、b、c、d、e和f,下列说法正确的是
A.b、f两点的电场强度相同
B.a点电势比d点电势高
C.c、b两点间电势差小于c、f两点间电势差
D.电子沿圆周由e到b与c到b,电场力做功相等
 17.如图所示,轻质弹簧上端固定,下端悬挂一个质量为m=0.5kg的物块,处于静止状态,以物块所在处为原点,竖直向下为正方向建立x轴,重力加速度g=10m/s2。现对物块施加竖直向下的拉力F,F随x轴坐标变化的情况如图所示。物块运动至x=0.4m处时速度为零。则物块下降0.4m的过程中,弹簧的弹性势能的增加量为
17.如图所示,轻质弹簧上端固定,下端悬挂一个质量为m=0.5kg的物块,处于静止状态,以物块所在处为原点,竖直向下为正方向建立x轴,重力加速度g=10m/s2。现对物块施加竖直向下的拉力F,F随x轴坐标变化的情况如图所示。物块运动至x=0.4m处时速度为零。则物块下降0.4m的过程中,弹簧的弹性势能的增加量为
 A.5.5JB.1.5JC.2.0JD.3.5J
A.5.5JB.1.5JC.2.0JD.3.5J
18.如图所示,飞行器P绕某星球做匀速圆周运动,星球相对飞行器的张角为θ,下列说法正确的是
A.轨道半径越大,周期越长
B.张角越大,速度越大
C.若测得周期和张角,则可得到星球的平均速度
D.若测得周期和轨道半径,则可得到星球的平均速度
 19.如图所示,为处于静电场中某空腔导体周围的电场分布情况,实线表示电场线,虚线表示等势面,A、B、C为电场中的三个点,O为空腔导体内的一点,下列说法正确的是
19.如图所示,为处于静电场中某空腔导体周围的电场分布情况,实线表示电场线,虚线表示等势面,A、B、C为电场中的三个点,O为空腔导体内的一点,下列说法正确的是
A.B点的电势低于O点的电势
B.A点的电势低于B点的电势
C.A点的电场强度小于B点的电场强度
D.将正电荷从A点移到C点,电场力做正功
 20.某工地上,一架起重机将放在地面的一个箱子吊起,箱子在起重机钢绳的作用下由静止开始竖直向上运动,运动过程中箱子的机械能E与其位移x变化关系的图像如图所示,其中0~x1过程的图线为曲线,x1x2过程的图线为直线,根据图像可知
20.某工地上,一架起重机将放在地面的一个箱子吊起,箱子在起重机钢绳的作用下由静止开始竖直向上运动,运动过程中箱子的机械能E与其位移x变化关系的图像如图所示,其中0~x1过程的图线为曲线,x1x2过程的图线为直线,根据图像可知
A.0~x1过程中箱子的动能一直增大
B.0~x1过程中钢绳的拉力逐渐减小
C.x1~x2过程中钢绳的拉力一直不变
D.x1~x2过程中起重机的输出功率一直增大
 21.如图所示,电源电动势为E,内阻为r,电路中的R2、R3分别为总阻值一定的滑动变阻器,R0为定值电阻,R1为光敏电阻(其电阻随光照强度增大而减小),电压表为理想表。当电键S闭合时,电容器C中一带电微粒恰好处于静止状态,有关下列说法中正确的是( )
21.如图所示,电源电动势为E,内阻为r,电路中的R2、R3分别为总阻值一定的滑动变阻器,R0为定值电阻,R1为光敏电阻(其电阻随光照强度增大而减小),电压表为理想表。当电键S闭合时,电容器C中一带电微粒恰好处于静止状态,有关下列说法中正确的是( )
A.只逐渐增大R1的光照强度的过程中,电阻R0消耗的电功率变大,电阻R3中有向上的电流
B.只调节电阻R3的滑动端P2向上端移动的过程中,电源消耗的功率变大,R3中有向上的电流
C.若断开电键S,电容器C所带的电荷量不变,带电微粒仍然处于静止状态
D.只调节电阻R2的滑动端P1向下端移动的过程中,电压表示数不变,带电微粒将向上运动
第II卷
三、非选择题:包括必考题和选考题两个部分。第22题~第32题为必考题,每个考题考生都必须作答,第33题~第40题为选考题,考生根据要求作答。
(一)必考题(共129分)
 22.(4分)如图所示为《测量弹簧劲度系数》的实验装置图,弹簧的上端固定在铁架台上,下端装有指针及挂钩,指针恰好指向一把竖直立起的毫米刻度尺。测得在挂钩上挂上一定数量钩码时指针在刻度尺上的读数如下表:
22.(4分)如图所示为《测量弹簧劲度系数》的实验装置图,弹簧的上端固定在铁架台上,下端装有指针及挂钩,指针恰好指向一把竖直立起的毫米刻度尺。测得在挂钩上挂上一定数量钩码时指针在刻度尺上的读数如下表:
| 钩码数n | 0 | 1 | 2 | 3 | 4 | 5 |
| 刻度尺读数xn(cm) | 2.62 | 4.17 | 5.70 | 7.22 | 8.84 | 10.64 |
| △xn=xn﹣xn﹣1(cm) | 0 | 1.55 | 1.53 | 1.52 | 1.62 | 1.80 |
已知所有钩码的质量可认为相同且为m=50kg,重力加速度取g=9.8m/s2.请回答下列问题:
(1)△x4、△x5与△x1、△x2、△x3相比较有很大的区别,其可能的原因是:_________________
(2)小刘同学通过k(x2﹣x0)=2mg,k(x3﹣x1)=2mg,得:劲度系数公式:![]()
请根据小刘同学的方法计算出弹簧的劲度系数k=________N/m。(结果保留两位有效数字)
23.(12分)某物理学习小组的同学在研究性学习过程中,用伏安法研究某电子元件R1(6V,2.5W)的伏安特性曲线,要求多次测量并尽可能减小实验误差,备有下列器材:
A.直流电源(6V,内阻不计)
B.电流表G(满偏电流3mA,内阻Rg=10Ω)
C.电流表A(0~0.6A,内阻未知)
D.滑动变阻器R(0~20Ω,5A)
E.活动变阻器R’(0~200Ω,1A)
F.定值电阻R0(阻值为1990Ω)
G.开关与导线若干
 (1)根据题目提供的实验器材,请你设计出测“
(1)根据题目提供的实验器材,请你设计出测“![]() ”表示(请画在方框内)
”表示(请画在方框内)
(2)实验中,为了操作方便且能够准确地进行测量,滑动变阻器应选用_______(填写器材前面的字母序号)
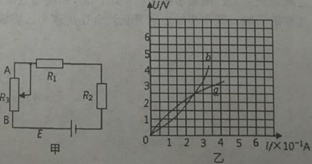
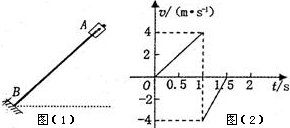 (3)将上述电子元件R1和另一电子元件R2接入如图所示的电路甲中,它们的伏安特性曲线分别如图乙中oa、ob所示,电源的电动势E=7.0V,内阻忽略不计,调节滑动变阻器R3,使电子元件R1和R2消耗的电功率恰好相等,则此时电子元件R1的阻值为_____Ω,R3接入电路的阻值为______Ω(结果保留两位有效数字)
(3)将上述电子元件R1和另一电子元件R2接入如图所示的电路甲中,它们的伏安特性曲线分别如图乙中oa、ob所示,电源的电动势E=7.0V,内阻忽略不计,调节滑动变阻器R3,使电子元件R1和R2消耗的电功率恰好相等,则此时电子元件R1的阻值为_____Ω,R3接入电路的阻值为______Ω(结果保留两位有效数字)
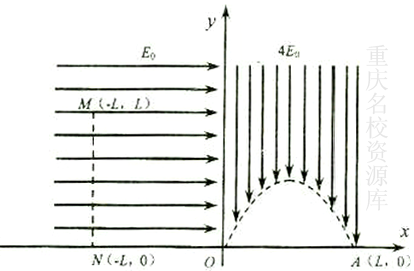
24.(13分)如图(1)所示,一根直杆AB与水平面成某一固定角度,在杆上套一个小物块,杆底端B处有一弹性挡板,杆与板面垂直,现将物块拉到A点静止释放,物块下滑与挡板第一次碰撞前后的v-t图像如图(2)所示,物块最终停止在B点,重力加速度为g=10m/s2,求:
(1)物块与杆之间的动摩擦因数μ;
(2)物块在杆上滑行的总路程s。
 25.(18分)如图所示,在直角坐标系xOy的第一象限中,存在竖直向下的匀强电场,电场强度大小为4E0.虚线是电场的理想边界线,虚线右端与x轴的交点为A,A点坐标为(L,0),虚线x轴所围成的空间内没有电场;在第二象限存在水平向右的匀强电场,电场强度大小为E0,M(﹣L,L)和N(﹣L,0)两点的连线上有一个产生粒子的发生器装置,产生质量均为m,电荷量均为q静止的带正电的粒子,不计粒子的重力和粒子之间的相互作用,且整个装置处于真空中.
25.(18分)如图所示,在直角坐标系xOy的第一象限中,存在竖直向下的匀强电场,电场强度大小为4E0.虚线是电场的理想边界线,虚线右端与x轴的交点为A,A点坐标为(L,0),虚线x轴所围成的空间内没有电场;在第二象限存在水平向右的匀强电场,电场强度大小为E0,M(﹣L,L)和N(﹣L,0)两点的连线上有一个产生粒子的发生器装置,产生质量均为m,电荷量均为q静止的带正电的粒子,不计粒子的重力和粒子之间的相互作用,且整个装置处于真空中.
(1)若粒子从M点由静止开始运动,进入第一象限后始终在电场中运动并恰好到达A点,求这个过程中该粒子运动的时间及到达A点的速度大小;
(2)若从MN线上M点下方由静止发出的所有粒子,在第二象限的电场加速后,经第一象限的电场偏转穿过虚线边界后都能到达A点,求此边界(图中虚线)方程.
26.(15分)A、B、D、R、Q五种短周期主族元素,其原子序数依次增大。其中A原子核内无中子,B与D同周期,R与Q同周期,A与R同主族,D与Q同主族,D元素的原子最外层电子数是次外层电子数的三倍,B元素的最高正价和最低负价代数和为2.请用对应的化学用语回答下列问题:
(1)Q元素位于元素周期表中第_______周期_______族
(2)D、R、Q三种元素形成的简单离子的半径由大到小的顺序是______(用离子符号表示)。
(3)由A、B两种元素以原子个数比5:1形成离子化合物X,X的电子式为_________
(4)由A、B元素形成的化合物B2Q4可以与O2、KOH溶液形成原电池,该原电池负极的点击反应式为___________________。
(5)由A、D、R、Q四种元素形成的化合物Y(RAQD3)(已知A2QD3的Ka1=1.3×10﹣2、Ka2=6.3×10﹣8),则Y溶液中各离子浓度由大到小的顺序为___________________________;室温下,向Y溶液中加入一定量的NaOH,使溶液中c(AQD3﹣)=c(QD32﹣),则此时溶液呈_________(填“酸性”、“碱性”或“中性”)
(6)Fe与D元素可形成Fe2D3、Fe3D4等化合物.向5.2gFe3D4、Fe2D3、Cu的混合物中加入0.5mol·L﹣1的硫酸溶液140ml,固体恰好完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为_______g
27.(14分)乙醛能与银氨溶液反应析出银。如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,这个反应又叫银镜反应。银镜的光亮程度与反应条件有关。某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究。
Ⅰ. 探究银镜反应的最佳实验条件部分实验数据如下表:
| 实验变量 实验序号 | 银氨溶液 /mL | 乙醛的量 /滴 | 水液温度/℃ | 反应混合液的PH | 出现银镜时间/min |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
请回答下列问题:
(1)读表若只进行实验1和实验3,其探究目的是 。
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是 ;
(3)进一步实验还可以探索____________________________对出现银镜快慢的影响。
Ⅱ. 探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
| 银氨溶液 | 加(NH4)2S ① | 过滤、洗涤 ② | 烘干 ③ | Ag2S沉淀 | 铁粉还原 ④ | 银 粉 |
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,并放出臭鸡蛋气味的气体,反应的化学方程式为_________________________________。过滤需要用到的玻璃仪器有____________(填编号)。要得到纯净的Ag2S沉淀,需要洗涤沉淀。实验室在过滤器中洗涤沉淀的操作是:__________________________________

a b c d e f g
(5)根据电化学原理也可Ag2S转变为Ag。方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去。
①该装置中银器为__________极。
②该装置总反应的化学方程式为___________________________________________。
28.(14分)运用化学反应原理研究部分单质及其化合物的反应又重要意义。
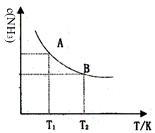 (1)氨是碳循环过程中的重要物质,是氮肥工业的重要原料。氨的合成是目前普遍使用的人工固氮方法:N2(g)+2H2(g)
(1)氨是碳循环过程中的重要物质,是氮肥工业的重要原料。氨的合成是目前普遍使用的人工固氮方法:N2(g)+2H2(g)![]() 2NH3(g) △H
2NH3(g) △H
①已知:H—H键能为436KJ/mol,N≡N键能为945KJ/mol,N—N键能为391KJ/mol。计算△H=________。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______移动(填“向左”、“向右”或“不”);
②右图是在平衡体系中c(NH3)随温度的变化。当温度由T1变化到T2时,平衡常数KA_____KB(填“>”、“<”或“=”)
(2)氨气溶于水得到氨水。NO2可用氨水吸收生成NH4NO3,25℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是___________________________(用离子方程式表示)。向该溶液滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将______(填“正向”、“不”或“逆向”)移动,所滴加氨水的浓度为_______mol·L﹣1(用含a、b的代数式表示)。(NH3·H2O的电离平衡常数取Kb=2×10﹣5mol·L﹣1)
(3)硫酸生产中,SO2催化氧化生成SO3:SO2(g)+1/2O2![]() SO3(g) △H<0,是工业上生产硫酸的关键步骤。
SO3(g) △H<0,是工业上生产硫酸的关键步骤。
①在某温度是,该反应的平衡常数K=0.75,若在此温度下,向100L的恒容密闭容器中,充入3mol SO2(g)、4mol O2(g)和4mol SO3(g),则反应开始时正反应速率______逆反应速率(填“<”、“>”或“=”)
②在①中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是________
a.保持温度和容器体积不变,充入1.0molSO3(g)
b.保持温度和容器内压强不变,充入2.0molHe(g)
c.降低温度
d.在其他条件不变时,减小容器的容积
③由硫酸可制得硫酸盐。在一定温度下,向K2SO4溶液中滴加Na2CO3溶液和BaCl2溶液,当两种沉淀共存时,![]() =_______________。[已知该温度时,Ksp(BaSO4)=1.3×10﹣10,Ksp(BaCO3)=5.2×10﹣9]
=_______________。[已知该温度时,Ksp(BaSO4)=1.3×10﹣10,Ksp(BaCO3)=5.2×10﹣9]
29.(8分)光合作用于细胞呼吸是植物体的两个重要生理活动,甲图表示绿色植物的光合作用与细胞呼吸两者之间的关系。乙图表示在光照充足、CO2浓度适宜的条件下,温度对某植物的真正光合作用速率和呼吸作用速率的影响。图中实线表示真正光合作用速率,虚线表示呼吸作用速率。据图分析回答下列问题:
(1)甲图中,消耗ATP的过程是 (写标号);过程④是在 中进行的。
(2)分析乙图可知,光合作用、呼吸作用都受到温度的影响,其中与 作用有关的酶对高温更为敏感;
(3)若昼夜不停地光照,乙图植物生长的最适宜温度约是_______;若温度保持在25℃的条件下,长时间每天交替进行12h(小时)光照、12h黑暗,该植物是否能正常生长?___________。
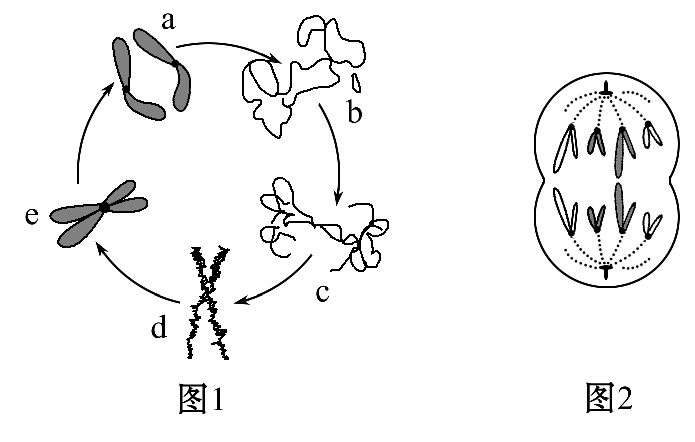
30.(10分)如图1表示植物根尖细胞有丝分裂过程中染色体(质)形态的周期性变化,图2是某动物(2N=4)细胞分裂过程中某一时期的图象,图3是细胞分裂过程中染色体变化曲线,请据图回答:

31.(12分)如图表示人体维持内环境稳态的几种调节方式。据图回答问题:
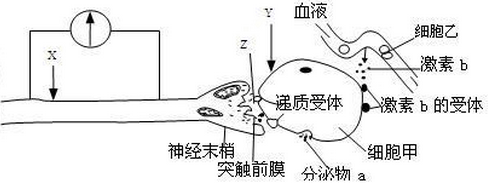
32.(9分)血栓主要由不溶性的纤维蛋白等物质组成。纳豆激酶(NK)是一种在纳豆发酵过程中由纳豆杆菌产生的蛋白酶,它具有溶栓的作用,其机理如下图所示,请根据图回答:
(1)据图分析,NK不但能直接催化分解________,还能间接激活_________,从而达到溶栓作用。
(2)请根据下列出示的实验材料,比较NK与内源性纤溶酶溶栓效果,并在下面横线位置上,补全相应内容。
实验材料:NK溶液、内源性纤溶酶溶液、纤维蛋白块、蛋清溶液、缓冲液、双缩脲试剂、量筒、试管和秒表。实验步骤:
①按顺序依次加入相关物质:第2步加缓冲液的主要作用是_____________________________;第4步加的物质是 。
②观察和记录__________________________ ,从而分析实验结果。
(二)选考题:共45分。请考生从给出的3道物理题,3道化学题,2道生物体中每科任选一题作答,并用2B铅笔在答题卡上把所选题目的题号涂黑。注意所做题目的题号必须与所涂题目的题号一致。在答题卡选答区域指定位置答题。如果多做,则每学科按所做的第一题计分。
33.【物理——选修3-3】
(1)(6分)下列说法正确的是_________(填正确答案的标号,选对一个得3分,选对2个得4分,选对3个得6分。每选错一个扣3分,最低分为0分)
A.晶体有天然规则的几何外形,而非晶体无天然规则的几何外形
B.由于液体表面层的分子间距离大于液体内部分子间距离,液体表面存在张力导致小露珠呈球形
C.熵增加原理也可表述为:一个系统的熵永远不会减少
D.当氢气和氦气的温度相同时,它们分子的平均动能一定相同
 E.一定质量的理想气体,吸收热量内容可能减少
E.一定质量的理想气体,吸收热量内容可能减少
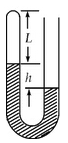
(2)(9分)如图,一端封闭、粗细均匀的U形玻璃管开口向上竖直放置,管内用水银将一段气体密封在管中。当温度为280K时,被封闭的气柱长L=22cm,两边水银柱高度差h=16cm,大气压强p0=76cm Hg
(1)为使左端水银面下降3cm,封闭气体温度应变为多少?
(2)封闭气体的温度重新回到280K后为使封闭气柱长度变为20cm,需向开口端注入的水银柱长度为多少?
34.【物理——选修3-4】
(1)(6分)下列说法中正确的有______(填正确答案的标号,选对一个得3分,选对2个得4分,选对3个得6分。每选错一个扣3分,最低分为0分)
A.不管光源与观察者是否存在相对运动,观察者观察到的光速是不变的
B.水面上的油膜呈现彩色是光的干涉现象
C.在光导纤维束内传送图象是利用光的色散现象
D.声源向静止的观察者运动,观察者接收到的频率小于声源的频率
E.未见其人先闻其声,是因为声波波长较长,容易发生衍射现象
(2)(9分)如图甲所示是由透明材料制成的半圆柱体,一束光束由真空沿着径向与AB成θ角射入,对射出的折线光纤的强度随θ角的变化进行记录,得到的关系如图所示,如图丙所示是这种材料制成的器具,左侧是半径为R的半圆,右侧是长为8R,高为2R的长方体,一束单色光从左侧A’点沿半径方向与长边成37°角射入器具。已知光在真空中的传播速度为c,求:(sin37°=0.6,cos37°=0.8)
①该透明材料的折射率;
②光线至少要经过几次全反射才能穿过器具?并求出穿过器具所用的时间?(必须有必要的计算说明)

35.【物理——选修3-5】
(1)(6分)下列说法正确的是_______(填正确答案的标号,选对一个得3分,选对2个得4分,选对3个得6分。每选错一个扣3分,最低分为0分)
A.β衰变中产生的β射线世纪上是原子的核外电子挣脱原子核的束缚而形成的
B.据玻尔理论,氢原子辐射处一个光子后,氢原子电势能减小,核外电子运动的加速度增大
C.每一种原子都有自己的特征谱线
D.比结合能越大,原子核中核子结合得越牢固,原子核越稳定
E.宏观物体的物质波波长非常小,极易观察到它的波动性
(2)(9分)如图所示,A、B两个物体粘在一起以v0=3m/s的速度向右运动,物体中间有少量炸药,经过O点时炸药爆炸,假设所有的化学能全部转化为A、B两个物体的动能且两物体仍然在水平面上运动。爆炸后A物体的速度依然向右,大小变为vA=2m/s,B物体继续向右运动进入半圆轨道且恰好通过最高点D。已知两物体的质量mA=mB=1kg,O点到半圆最低点C的距离xOC=0.25m,水平轨道的动摩擦因数μ=0.2,半圆轨道光滑无摩擦。求:
(1)炸药的化学能E;
(2)半圆弧的轨道半径R
36.【化学—选修 化学与技术】(15分)
七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
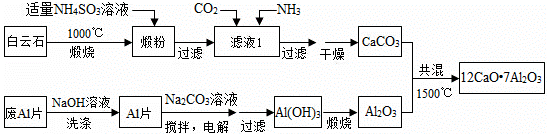
(1)锻粉主要含MgO和 ______;用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,或滤液Ⅰ中c(Mg2+)小于5×10-6mol/L,则溶液pH大于______;该工艺中不能用(NH4)2SO4代替NH4NO3,原因是 ____________________________。(Mg(OH)2的Ksp=5×10-12)
(2)滤液Ⅰ中阴离子有 _________(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成_______ ,从而导致CaCO3产率降低.
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为 _____________________
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为 _____________________
(5)一种可超快充电的新型铝电池,充放电时AlCl4﹣和Al2Cl7﹣两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为_______________________
37.【化学—选修物质结构与性质】(15分)
第二周期中碳、氮、氧是构成生命物质的三种主要元素,在生产生活中也有着重要的应用。
(1)第二周期中,第一电离能处于B与N之间的元素有________种
(2)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的为成对电子数相同,则其基态原子的价层电子排布式为________
(3)NH3分子的VSEPR模型为________,SO3分子的空间构型为________
(4)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在痕量(C2H5O)3P=O存在下加热脱水得到。乙烯酮分子中碳原子杂花轨道类型有_______。CH3COOH的沸点比HCOOCH3高,其主要原因是____________________
(5)CH2=CHCN是制备晴纶的原料,其分子中![]() 键和
键和![]() 键的个数之比为________(填最简整数比)
键的个数之比为________(填最简整数比)
(6)[LiC60]PF6与NaCl具有类似的晶胞结构([LiC60]+表示1个Li+位于1个C60内部)。[LiC60]PF6晶体中包含的化学键有_______(填字母)
A.金属键B.离子键C.极性键D.非极性键E.范德华力
已知[LiC60]PF6晶体晶胞边长为a nm,计算[LiC60]PF6晶体的密度为_______g/cm3(用含a、阿伏伽德罗常数NA的式子表示)
38.【化学—选修 有机化学基础】(15分)
现有分子式为CnH8O2X2的物质M,可发生如下所示转化:
 已知知:①物质B在质谱分析中,在质谱图显示存在多种质荷比不相同的粒子,其中质荷比最大的为32,物质B在核磁共振氢谱分析中,有两个吸收峰,吸收峰面积之比为3∶1。
已知知:①物质B在质谱分析中,在质谱图显示存在多种质荷比不相同的粒子,其中质荷比最大的为32,物质B在核磁共振氢谱分析中,有两个吸收峰,吸收峰面积之比为3∶1。
②1mol G需要2mol H2加成
③两个—OH同时连在一个C原子上,结构不稳定,会自动失水,如:

请回答下列问题:
(1)n= ,M中官能团名称为 ___________ 。
(2)①、③的反应类型:① _______ ,③ _______ 。
(3)写出M、E、G的结构简式;M: _____________ ;G: _______________ 。
(4)写出下列反应的化学方程式:A→D: _______________________________________ ;
(5)符合下列条件的E的同分异构体有______种,写出其中核磁共振氢谱有五组峰,峰面积之比为1:1:2:2:2的同分异构体的结构简式为___________(写一种)
①能发生水解反应②能发生银镜反应③遇FeCl3溶液显紫色
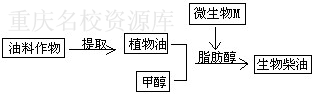 39.生物柴油是一种可再生的清洁能源,其应用在一定程度上能够减缓人类对化石燃料的消耗,科学家发现,在微生物M产生的脂肪酶作用下,植物油与甲醇反应能够合成生物柴油(如右图)
39.生物柴油是一种可再生的清洁能源,其应用在一定程度上能够减缓人类对化石燃料的消耗,科学家发现,在微生物M产生的脂肪酶作用下,植物油与甲醇反应能够合成生物柴油(如右图)
40.胚胎工程是一项综合性的动物繁育技术,可在畜牧业、制药业等领域发挥重要作用,下图是通过胚胎工程培育试管牛的过程。

(1)采集的精子需_______处理后才能进行受精作用:卵子的成熟在过程_______中(用图中数字作答)
(2)图中过程③称为_______,它在胚胎工程中的意义在于____________。此过程的进行需要将胚胎培养至________时期。
(3)为了提高已有胚胎的利用率,可采用________技术,它可看作_________(有性/无性)繁殖。
(4)胚胎工程技术包含的内容很丰富,如胚胎干细胞培养技术,这种细胞是从________中分离出来的。




