
最新!2022湖南物理高考真题及答案解析出炉
06月11日
2015广东省高考压轴卷理综
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 S 32 Cl 35.5 Fe 56 Cu 64
一、单项选择题:本大题共16小题,每小题4分,共64分。在每小题给出的四个选项中,只有一个选项符合题目要求,选对的得4分,选错或不答的得0分。
1.下列关于细胞生理过程的描述,正确的是
A.大肠杆菌在有氧状态下利用细胞质中的相关酶系合成ATP
B.吞噬细胞摄入抗原,经处理后合成相应的抗体
C.人的红细胞成熟后,仍继续合成蛋白质
D.叶肉细胞利用核孔实现核内外DNA、RNA和蛋白质的交换
2、某双链DNA分子含有400个碱基,其中一条链上A:T:G:C=1:2:3:4。下列表述错误的是
A.该DNA分子的一个碱基改变,不一定会引起子代性状的改变
B.该DNA分子连续复制两次,需要游离的腺嘌呤脱氧核苷酸120个
C.该DNA分子中4种碱基的比例为A:T:G:C=3:3:7:7
D.该DNA分子中的碱基排列方式共有4200种
3. 酵母菌在含乳糖的培养基上生长时,细胞中出现了分解乳糖的酶,将其转移到不含乳糖的培养基上时,这些酶就不存在了,下列说法正确的是
| 选项 | 叙述I | 叙述II |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | 浓HNO3具有酸性和强氧化性 | 金属铜可与浓HNO3反应 |
| C | Li与Na属于同一主族元素 | Li与O2共热反应产物为Li2O2 |
| D | HF可用于雕刻玻璃 | HF为强酸 |
 15.1930年劳伦斯制成了世界上第一台回旋加速器,其原理如图所示. 这台加速器由两个铜质D形盒D1、D2构成,其间留有空隙. 下列说法正确的是
15.1930年劳伦斯制成了世界上第一台回旋加速器,其原理如图所示. 这台加速器由两个铜质D形盒D1、D2构成,其间留有空隙. 下列说法正确的是  A.人所受的合力方向与自动扶梯运动方向相同
A.人所受的合力方向与自动扶梯运动方向相同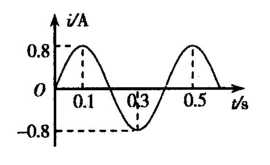 19.某手摇交流发电机,其线圈绕垂直于匀强磁场方向的轴(位于线圈平面内)匀速转动, 产生的交变电流i随时间t变化的图象如图所示,由图象可知
19.某手摇交流发电机,其线圈绕垂直于匀强磁场方向的轴(位于线圈平面内)匀速转动, 产生的交变电流i随时间t变化的图象如图所示,由图象可知| 卫星半径(m) | 卫星质量(kg) | 轨道半径(m) | |
| 土卫十 | 8.90×104 | 2.01×1018 | 1.51×108 |
| 土卫十一 | 5.70×104 | 5.60×1017 | 1.51×108 |
 21.如图甲所示,某静电除尘装置中有一矩形通道,其前、后面板使用绝缘材料,上、下面板使用金属材料.图乙是装置的截面图,上、下两板与电压恒定的高压直流电源相连.带负电的尘埃水平进入矩形通道,当碰到下板后其所带电荷被中和,同时被收集.不计尘埃的重力.
21.如图甲所示,某静电除尘装置中有一矩形通道,其前、后面板使用绝缘材料,上、下面板使用金属材料.图乙是装置的截面图,上、下两板与电压恒定的高压直流电源相连.带负电的尘埃水平进入矩形通道,当碰到下板后其所带电荷被中和,同时被收集.不计尘埃的重力.| 选项 | 操作或事实 | 现象及结论 |
| A | 向硫酸钡固体中加入过量的饱和Na2CO3,溶液充分反应,过滤、洗涤、再往滤渣中滴入少量盐酸溶液 | 产生能使澄清石灰水变浑浊的气体,证明:KSP(BaSO4)>KSP(BaCO3) |
| B | 将CO2气体通入足量的CaCl2溶液中 | 产生白色沉淀,该沉淀为CaCO3 |
| C | 向某溶液加入过量NaOH溶液并加热,将湿润的红色石蕊试纸靠近试管口 | 红色石蕊试纸变蓝,原溶液中一定含有NH4+ |
| D | 往酸性高锰酸钾溶液中滴入过量的乙醇溶液 | 酸性高锰酸钾溶液褪色,证明乙醇有一定的还原性 |
| R | ||||
| X | T | Z | Q |


B. 乙病是常染色体隐性遗传病
C. 如果Ⅲ8是女孩,则其基因型只有两种可能
D. Ⅲ10不携带甲、乙两病致病基因的概率是1/3
二、非选择题:本大题共11小题。按题目要求作答。解答题应写出必要的文字说明、方程式和重要演算步骤,只写出最后答案的不能得分。有数值计算的题,答案中必须明确写出数值和单位。
26.为了提高设施农业的经济效益,科研人员对温室栽种的作物进行了相关研究。表中数据为在密闭实验装置内,给予不同光照强度时所测得的该作物氧气释放量;图1表示该作物相对光合速率(即不同叶龄时的净光合速率与B点时的比值)与叶龄的关系,A点表示幼叶成折叠状,B点表示叶片充分展开;图2中曲线1、2分别表示作物在适宜的光照强度下不同温度时的实际光合量和净光合量。请回答:
| 光照强度(klx) | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| O2释放量(μL·cm-2叶面积·min-1) | -0.2 | 0 | 0.2 | 0.4 | 0.8 | 1.2 | 1.2 | 1.2 |
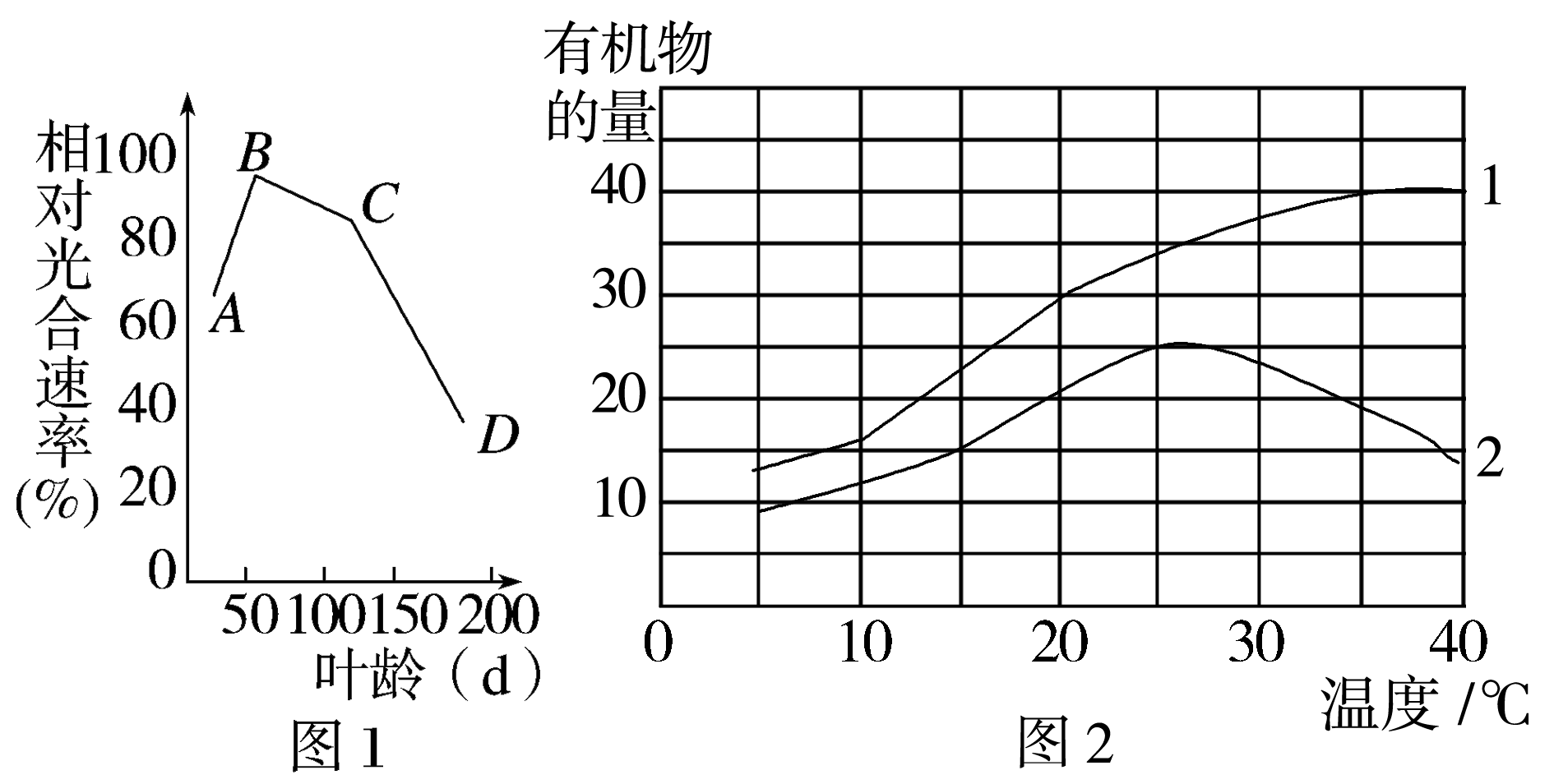
(1)绿色植物释放O2的同时还产生______________;该过程发生的场所是 ;由表可知,在光照强度为4 klx时,该作物光合作用的实际产氧量为________μL·cm-2叶面积·min-1。
(2)图1中AB段相对光合速率上升,从光反应角度分析原因是________________________,CD段相对光合速率明显下降的原因是_______________________________________。
(3)由图2分析,假如植物生活在12小时光照,12小时黑暗的环境中,则在环境温度高于约________不能正常生长,原因是____________________________________________。
(4)根据以上研究结果,该温室作物白天生长的最佳环境条件是________________________
_____________________________________________。
27.某自花传粉、闭花受粉的植物,花的颜色有红、白两种,由A、a,B、b两对等位基因控制。回答以下问题:
(1) 现有一基因型为AaBb的植株,其体细胞中相应基因在DNA上的位置及控制花色的生化流程如下图:

①控制花色的两对基因符合孟德尔的 定律。
②该植株花色为 ,其体细胞内的DNA1和DNA2所在的染色体之间的关系是 。
③该植株自交时(不考虑基因突变和交叉互换现象),后代中纯合子的表现型为 ,红色植株占 。
④该植株进行测交时,应对母本进行 等一系列处理。
(2) 该植物种子的形状有饱满和皱缩之分,研究发现种子形状的改变是由于基因突变引起的。由下图可知,该植物的AGpaes基因1突变为AGpaes基因2时,发生了碱基对的 。从这一实例还可看出,基因通过 ,进而控制生物体的性状。

28.下图表示人体内激素的分泌及作用机制,请回答下列问题:

(1)人体的组织细胞有特异性受体与激素分子相结合,这样的细胞称为该激素分子的 ,激素能使细胞原有的生理活动发生变化,因此激素又称为 。
(2)若乙是胰岛B细胞,则激素①对糖代谢的调节情况是:除了抑制肝糖原分解和非糖物质转化为葡萄糖外,特别是能 ;若乙是胰岛A细胞,则激素①的调节结果是 。
(3) 激素②进入细胞内,通过影响f的活动以及g、h的形成,即影响 过程而调节生命活动。
(4)a、b过程表示激素②分泌的 调节;c、d的调节过程是:当激素②的含量增加到一定程度时,对甲和垂体的分泌活动起 作用。
(5) 甲监测着人体的多种功能,能及时将信息反馈到大脑,而大脑发出的“指令”要经甲转达,从而协调内分泌系统的活动,所以,激素的分泌又受 的调节。
29.回答以下与雾霾天气有关的问题:
(1)治理雾霾,既要控制城市人口规模、还要考虑自然—经济—社会效益,遵循的生态工程建设原理分别是 、 。
(2)某小组尝试用纤维素制备燃料酒精,为了获得能高效合成纤维素酶的单菌落,可采用 法将初筛菌液接种在固体培养基上,从功能上看,这种培养基属于 培养基。欲在此基础上获得纤维素酶活性更高的菌株,最简单可行的做法是 。
(3)下面是一个探究雾霾天气与肺癌的相关性的实验方案。(实验用具及材料:与雾霾天气类似的烟雾箱,大白鼠若干),请完成相关的内容。
| 实验组 | 对照组 | |
| 饲养空气条件 | ① | ② |
| 饲养其他条件 | ③ | |
| 肿瘤成分检测 | ④定期抽血检测细胞表面的 化学成分 | |
①
②
③
④
⑤我们认为:即使实验组的肿瘤成分检出高于对照组,也不能肯定得出“雾霾天气会导致人类肺癌”的结论,你认为理由有 。
30.(16分)酰化反应是有机合成中一种重要的反应,如反应①:
化合物Ⅰ可由化合物Ⅲ合成:
(1)化合物Ⅱ的分子式为 ,1mol该物质与H2完全加成消耗H2.mol
(2)化合物Ⅰ与Br2加成的产物的结构简式为______________。化合物Ⅳ生成化合物I的反应类型为 。
(3)已知化合物Ⅲ的核磁共振氢谱有两组吸收峰,峰面积之比为为6:1,则化合物Ⅲ的结构简式为 。化合物Ⅲ与足量醇溶液共热反应的化学方程式为:
。
(4)写出满足下列条件Ⅱ的其中一种同分异构体的结构简式 。
①苯环上的一氯代物只有2种;
②可发生水解反应,且水解产物能使FeCl3溶液显色
③能发生银镜反应
④能与NaHCO3反应产生气泡
(5)化合物Ⅴ:与足量的化合物Ⅰ在一定条件下也能发生类似反应①的反应,生成有机化合物Ⅵ,则Ⅵ的结构简式为 。
31.(16分)一氧化碳、氢气和乙醇均可以燃烧放出能量,热化学方程式分别为:
① 2CO(g)+ O2(g)=2CO2(g) △H1
② 2H2(g)+ O2(g)=2H2O(g) △H2
③CH3CH2OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3
(1)工业上由CO与H2直接合成乙醇的反应④:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g)△H,则△H= (用△H1、△H2、△H3表示)
CH3CH2OH(g)+H2O(g)△H,则△H= (用△H1、△H2、△H3表示)
(2)已知反应③的△H>0,则下列措施能增大反应③逆反应速率的是
A.移去部分CO2B.增大容器容积 C.通入大量O2D.升高体系温度
(3)在1L恒容密闭容器中通入一定量的CO和H2,在5000C恒温下发生反应④,CH3CH2OH(g)、CO(g)和H2(g)的浓度随时间的变化如下表所示:
| 时间/min | 10 | 30 | 50 | 60 |
| c(CH3CH2OH)/ mol·L-1 | 0.40 | 0.75 | 0.90 | 0.90 |
| c(CO)/ mol·L-1 | 1.20 | c1 | 0.20 | c3 |
| c(H2)/ mol·L-1 | 2.40 | c2 | 0.40 | 0.40 |
①根据表中数据填写:c1= mol·L-1;c2= mol·L-1;c3= mol·L-1;
5000C平衡常数K=
②计算反应进行到10min时,CO的平均反应速率(写出计算过程,结果保留两位有效数字)。
(4)已知某条件下,反应④中H2的转化率α(H2)与反应时间t的变化曲线如下图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出增大容器体积和加入催化剂时α(H2)~t的变化曲线示意图(进行相应的标注)

32.(16分)实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),其过程如下:

(1)过程①中,FeS和O2、H2SO4反应的化学方程式为 。
(2)过程②中产生的尾气会对大气造成污染,可选用下列试剂中的 吸收。
a.浓硫酸 b.蒸馏水 c.NaOH溶液d.浓硝酸
(3)过程③中,需要加入的物质名称是 。
(4)过程④的实验操作是 。
(5)过程⑥中,将溶液Z加热到70℃~80℃,目的是 。
(6)实验室为测定所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取样品2.700 g;②将样品溶于足量盐酸后,加入足量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495 g。若该聚铁主要成分为[Fe(OH)SO4]n,则该聚铁中铁元素的质量分数为 。
33.(16分)化学实验室探索物质性质的重要手段,并对工农业的发展起着重要的作用。
(1)硫及其化合物的实验探究:
①下列是对硫及其化合物性质的实验探究装置,其中能达到目的或实验合理的是
A.用a装置制取SO2气体
B. 用b装置验证非金属性:S﹥C
C. 用c装置除去CO2中混有的少量SO2气体
D. 验证SO2气体的漂白性
② SO2中S的化合价为+4价,说明其具有氧化性和还原性,SO2具有还原性,所以其可以使
褪色;请设计实验证明SO2具有氧化性,操作和现象是:
。
(2)处理工业废水中Cr(+6价)元素的实验探究:
①加入FeSO4·7H2O还原法:往含Cr2O72-的酸性废水中加入适量的FeSO4·7H2O,Cr2O72-被还原为Cr3+,继续加入适量的NaOH溶液调节pH产生Cr(OH)3沉淀,完成上述氧化还原反应的离子方程式:
Cr2O72- + Fe2+ + H+![]() Cr3++ Fe3++
Cr3++ Fe3++
② 电化学除Cr:请设计一个电化学装置,通过该装置同样可以完成上述反应。部分装置和电极已画出,请继续完成该电化学装置图,并进行必要的标注。
限选材料:直流电源;石墨棒,铁片,导线。
③在上述电化学实验装置图中,阳极的电极反应式为: ;该电化学装置可有效除去废水的Cr的工作原理是:
。
34.(18分)
(1)某同学利用打点计时器测量小车做匀变速直线运动的加速度.
①电磁打点计时器是一种使用__________(填 “交流”或 “直流”)电源的计时仪器,它的工作电压是4-6V,当电源的频率为50Hz时,它每隔_______s打一次点.
②使用打点计时器时,接通电源与让纸带随小车开始运动这两个操作过程的操作顺序,应该是 ( )
A.先接通电源,后释放纸带 B.先释放纸带,后接通电源
C.释放纸带的同时接通电源 D.哪个先,哪个后都可以
③实验中该同学从打出的若干纸带中选取一条纸带,如下图所示,纸带上按时间顺序取为A、B、C、D四个计数点,每两个点之间还有四个点未画出.用尺子测得各点的距离为s1=3.62cm,s2=4.75cm,s3=5.88cm.
根据纸带数据可以判断小车在做匀加速直线运动,理由是_____________________(请用文字描述);在记数点C所代表的时刻,纸带运动的瞬时速度是__________m/s;小车的加速度是_________m/s2.(以上两空均保留三位有效数字)
(2)某物理兴趣小组的同学利用实验探究电池的电动势和内阻,实验的主要操作如下:
①先用多用电表的电压档直接接在电池两极粗测电池的电动势,表盘如图(甲)所示,示数为 V,这样测出的电动势比真实值_______(选填“偏大”或“偏小”).
(乙)
(甲)
②若按图(乙)所示接好电路进行实验,记下电阻箱和电压表对应的一系列读数R、U ,并将数据记录在下表中.第2次实验中,电阻箱的示数如图(丙)所示,此时电阻箱接入电路的电阻是 Ω;
| 实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.80 | 1.07 | 1.30 | 1.47 | 1.80 | 2.27 | |
| 0.20 | 0.80 | 1.0 | 1.5 | 2.0 |
③图(丁)是根据上表中的数据,在坐标纸
上画出的![]() —
—![]() 图象.根据图象可知:
图象.根据图象可知:
电池的电动势E=________V,
内阻r=________Ω .
(结果保留三位有效数字)
35.如图(a)所示,一个电阻值为R,匝数为n的圆形金属线圈与阻值为2R的电阻R1连结成闭合回路,a、b端点通过导线与水平放置、间距为d的平行金属板相连.线圈的半径为r1.在线圈中半径为r2的圆形区域存在垂直于线圈平面向里的匀强磁场,磁感应强度B随时间t变化的关系图线如图(b)所示.图线与横、纵轴的截距分别为t0和B0.导线的电阻不计.在0至t1时间内:
(1)求通过电阻R1上的电流方向;
(2)求通过电阻R1上的电流大小;
(3)一质量为m的带电微粒水平射入金属板间,恰能匀速通过,试判断该微粒带何种电荷?
带电量为多少?(重力加速度为g).
36.如图所示,小球A以初速v0沿光滑平台向右运动,竖直静止悬挂的小球B,恰好与平台右端接触.一水平放置、半径R=0.5 m的薄壁圆桶绕轴OO′匀速转动,转动角速度ω=5π rad/s,桶壁上离左端s=0.2m处开有一长度d=0.8m的长孔,孔宽略大于小球A的直径.圆桶左端和平台右端平齐,顶端距平台h=0.8 m.若A、B两球发生弹性正碰时(碰撞时间极短),长孔恰好运动到桶的正上方,碰后B上摆,A沿水平方向抛射向长孔.已知v0方向、悬线和圆桶的轴线在同一竖直面上,小球B的质量为m,A的质量是B的k倍,悬线长L=0.8m,视两球为质点,g=10 m/s2,不考虑空气阻力.
(1)若k=2,碰后B刚好能摆到与悬点同一高度,试求初速v0的大小;
(2)试通过计算,判断(1)情形中小球A是否会和圆桶碰撞;
(3)若v0取(1)中数值,小球A落入孔中且不会与桶壁发生碰撞,试求k的取值范围.
生物参考答案
1. 【答案】A
【解析】抗原被抗体杀死,或被吞噬细胞吞噬,或被抗体杀死后,再被吞噬细胞吞噬。人的红细胞不能合成蛋白质。叶肉细胞利用核孔实现核内外mRNA和蛋白质的交换。
2. 【答案】 B
【解析】 本题考查DNA的结构知识。DNA双链有400个碱基,一条链有200个碱基,一条链上A:20个,T:40个,G:60个,C:80个。双链中A =T:有60个,G=C:有140个。该DNA分子一个碱基改变,有可能改变(氨基酸种类、数目、排列顺序已变),有可能不变(氨基酸种类、数目、排列顺序不变)。DNA复制两次,需游离的腺嘌呤脱氧核苷酸为(2n-1)*60=180个,B错。
3. 【答案】C
【解析】缺乏乳糖时,编码乳糖分解酶的基因不消失,只不过是不表达,A错误。在乳糖的诱导下,酵母菌没有发生突变,只不过编码乳糖分解酶的基因进行表达,B错误。在乳糖的诱导下,酵母菌分解乳糖的酶的基因得到表达,C正确。乳糖不是乳糖分解酶基因的重要组成成分,D错误。
4. 【答案】C
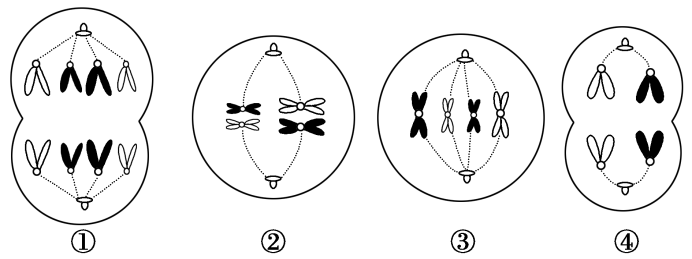
【解析】分析细胞中染色体的行为变化可知,①②③④所示细胞分别处于有丝分裂后期、减数第一次分裂中期、有丝分裂中期、减数第二次分裂后期,①中无染色单体,④中无同源染色体。由于不能通过①②③④所示细胞确定是雄性动物还是雌性动物,故动物睾丸或卵巢中可能同时出现以上细胞。④细胞质均等分裂,所以其子细胞可能是精细胞或极体。
5. 【答案】D
【解析】植物激素是植物体内特定部位产生的,从产生部位运输到作用部位,继而发挥作用。各种植物激素并不是孤立地起作用,而是多种激素相互作用共同调节。植物激素是一种信号分子,能引起植物其他部位细胞的生理过程发生改变,从而影响植物生理过程。植物激素对植物的生长、发育、产生调节作用,而非催化作用。
6. 【答案】B
【解析】植物细胞工程中体现了植物细胞的全能性,而动物细胞工程利用的是细胞增殖的原理,A错误。胚胎工程要以动物细胞培养为基础,基因工程的受体细胞需要进行细胞培养,B正确。用于制果酒的微生物为酵母菌,制腐乳的微生物主要为毛霉,均属于真核生物,含线粒体,而制果醋的醋酸杆菌属于原核生物,无线粒体,C错误。单克隆抗体的特点是灵敏度高、特异性强等,D错误。
24. 【答案】AB
【解析】小瓶中含有CO2缓冲液,可以保持装置中的CO2浓度不变,而液滴不动,说明装置中气体体积未发生变化,光合速率等于呼吸速率,A正确。色素分离是利用不同色素在层析液中溶解度不同,溶解度越低的,扩散速度越慢,扩散距离越小,B正确。图丙已经形成新的细胞核,细胞膜凹陷形成两个子细胞,应为有丝分裂末期,C错误。丁图为质壁分离现象,高浓度的KNO3溶液也可引起质壁分离,区别是一段时间后会自动复原,D错误。
25. 【答案】AB
【解析】Ⅰ1和Ⅰ2不患乙病,其女儿Ⅱ4患病,可知乙病的遗传方式为常染色体隐性遗传病,而甲病的致病基因位于X染色体上,又由Ⅰ1、Ⅰ2和Ⅱ6可知为显性遗传,A、B正确。如果Ⅲ8是女孩,则其基因型有四种可能,C错误。Ⅲ10不携带甲、乙两病致病基因即纯合的概率是2/3,D错。
26. 【答案】(1)[H]和ATP 类囊体 0.4
(2)幼叶展开,叶面积增大,光合色素含量增多 叶片衰老,叶绿素含量减少,相关酶活性降低
(3)35 ℃ 此时净光合量与呼吸量相等,大于35 ℃则净光合量小于呼吸量,植物不能正常生长
(4)光照强度为10 klx、室温为25 ℃
【解析】(1)绿色植物光合作用过程中,光反应阶段释放O2的同时还产生[H]和ATP用于暗反应。表中所测氧气的释放量代表净光合量。光照强度为0时,氧气的释放量代表呼吸量,所以在光照强度为4 klx时,该作物光合作用的实际产氧量=净光合量+呼吸量=0.4 μL·cm-2叶面积·min-1。
(2)已知图1中A点表示幼叶成折叠状,B点表示叶片充分展开,即AB段表示幼叶展开,叶面积增大,光合色素含量增多,所以该段相对光合速率上升。而CD段叶片衰老,叶绿素含量减少,相关酶活性降低,所以相对光合速率明显下降。
(3)若植物生活在12小时光照、12小时黑暗的环境中,该植物一天中有机物的积累量=光照时有机物的积累量-黑暗时有机物的消耗量=12×净光合量-12×呼吸量。由此可见,只有净光合量大于呼吸量时,植物才能积累有机物,正常生长。分析图2可知环境温度为35 ℃时,该植物净光合量与呼吸量相等,高于35 ℃时,净光合量小于呼吸量,植物不能正常生长。
(4)由表中数据可知,光照强度为10 klx时,植物净光合量最大;由图2可知环境温度为25 ℃时,植物净光合量最大。所以该温室作物白天生长的最佳环境条件是光照强度为10 klx、室温为25 ℃。
27. 【答案】 (1) ①分离 ②红色 同源染色体 ③白色 1/2 ④未成熟花的去雄→套袋→授粉→套袋(“去雄→套袋→授粉→套袋”) (2) 增添 控制酶的合成来控制代谢过程
【解析】(1) ①根据图示,这两对等位基因位于一对同源染色体上,不能进行自由组合,因此符合基因的分离定律。②酶A可以将前体物质转化为中间产物,酶B可以将中间产物转化为终产物,AaBb的植株同时具有酶A和酶B,因此能形成终产物红色物质,花色为红色,两条DNA分子所在的染色体,相同的位置构成等位基因,因此两条染色体是同源染色体。③该植株自交时,根据基因的分离定律可知形成的后代基因型的比例为AAbb∶AaBb∶aaBB=1∶2∶1,其中纯合子为AAbb和aaBB两者都只能合成酶A或酶B,不能同时合成两种酶,因此表现型为白色,红色植株为AaBb,占1/2。④根据题意,该植株是自花传粉、闭花受粉,要进行杂交首先要防止其自交,因此先要对母本去雄,然后套袋处理,等雌蕊成熟后再授粉,继续套袋,才能实现人工杂交。(2)根据图示可知,突变后的基因所合成的蛋白质增加了两个氨基酸,所以最有可能是发生了碱基对的增添。从图示可知,基因可以通过控制酶的合成控制代谢过程,进而控制生物的性状。
28. 【答案】 (1) 靶细胞 信息分子 (2) 促进细胞加速摄取、利用和储存葡萄糖(促进血糖氧化分解、合成糖原、转化非糖物质) 血糖水平升高 (3) 基因的表达(蛋白质的合成) (4) 分级 抑制(反馈调节、负反馈调节)
(5) 神经系统
【解析】 (1) 激素作用的细胞为靶细胞,激素又称信息分子。(2) 若乙是胰岛B细胞,则激素①是胰岛素,胰岛素能促进血糖氧化分解、合成糖原、转化非糖物质,抑制肝糖原分解和非糖物质转化为葡萄糖,若乙是胰岛A细胞,则激素①是胰高血糖素,胰高血糖素能使血糖浓度升高。(3) 由图可知,激素②能影响基因的表达。(4) a、b过程表示激素的分级调节,c、d过程表示反馈调节。(5) 甲是下丘脑,大脑发出的“指令”要经甲转达,从而协调内分泌系统的活动,即激素的分泌受神经系统调节。
29.【答案】
(1) 协调与平衡原理 整体性原理 (2) 平板划线(或稀释涂布平板) 选择 人工诱变(紫外线等照射)处理菌株,再进行筛选 (3) ①与雾霾天气类似的烟雾箱 ②在空气质量正常的环境 ③相同且适宜 ④癌胚抗原或甲胎蛋白 ⑤人与鼠还有一些诸如体重饮食生理等方面的差异;雾霾的成分也不一定完全相同; 在雾霾中生活的时间等不确定因素,癌症的发病是一个非常漫长的过程,对于空气污染同癌症之间的关联,目前国际上也没有确定结论等
【解析】 (1) 控制城市人口规模需遵循的生态工程建设原理是协调与平衡原理,考虑自然—经济—社会效益遵循的生态工程建设原理则是整体性原理。(2) 微生物的接种方法有平板划线法和稀释涂布平板法;获得能高效合成纤维素酶的单菌落应该用选择培养基;在原有基础上获得更优的性状的个体通常利用基因突变,最简单可行的做法是人工诱变(紫外线等照射)处理菌株,再进行筛选。(3) 探究雾霾天气与肺癌的相关性,自变量为雾霾空气与正常空气,其他条件为无关变量且应保持相同且适宜,因变量为癌变的情况,可检测细胞表面的癌胚抗原或甲胎蛋白。人与鼠还有一些诸如体重饮食生理等方面的差异;雾霾的成分也不一定完全相同; 在雾霾中生活的时间等不确定因素,癌症的发病是一个非常漫长的过程,对于空气污染同癌症之间的关联,目前国际上也没有确定结论等,因此即使实验组的肿瘤成分检出高于对照组,也不能肯定得出“雾霾天气会导致人类肺癌”的结论。
化学参考答案
7.【答案】D
【解析】植物油在碱性条件下水解生成高级脂肪酸盐和丙三醇,A错误;苯和甲苯均难溶于水且密度小于水,故水滴入苯溶液或甲苯溶液中,现象一样,无法区分,B错误;甲醇不能发生消去反应,C错误;煤的干馏指的是在将煤在隔绝空气下加热分解,产物有焦炭、粗氨水、苯等,该过程属于化学变化,D正确。
8.【答案】D
【解析】:A项OH-与Mg2+生成沉淀不能大量共存;B项H+、NO3-和I-发生氧化还原反应而不能大量共存;C选项Al3+与HCO3-发生完全双水解反应而不能大量共存;NH4+与CO32-虽然发生了双水解反应,但不是彻底的双水解,因而也可以大量共存,D正确。
9.【答案】A
【解析】N2含有24个电子,故16g O3含有的电子数为8mol,即8nA个,A正确;盐酸为液体,11.2L盐酸的物质的量非0.5 mol,B错误;常温下,Fe置于足量浓硫酸溶液中发生钝化,反应不完全,C错误;D选项没有给出溶液的体积,计算不出具体粒子的数目,D错误。
10.【答案】C
【解析】氯水具有漂白性,漂白过程中发生氧化还原反应,漂白过的物质性质稳定,不容易复原,C错误。
11.【答案】D
【解析】0.1 mol·L-1的H2SO4溶液中c(H+)=0.2 mol·L-1,与0.1 mol·L-1的NaOH溶液等体积混合,溶液呈酸性,A错误;Na2CO3溶液中,CO32-水解,CO32-+H2O![]() HCO3-+OH-(主要),HCO3-+H2O
HCO3-+OH-(主要),HCO3-+H2O![]() H2CO3+OH-(次要),根据水解方程式即可判断出,c(Na+)﹥c(CO32-)﹥c(OH-)﹥c(HCO3-)﹥c(H+),B错误;碳酸钠促进水的电离,溶液中的OH-离子全部由水电离产生,水电离出的c(OH-)=10-2mol·L-1,C错误; D选项考察物料守恒,Na原子与CH3COO原子团个数比为1:2,D正确。
H2CO3+OH-(次要),根据水解方程式即可判断出,c(Na+)﹥c(CO32-)﹥c(OH-)﹥c(HCO3-)﹥c(H+),B错误;碳酸钠促进水的电离,溶液中的OH-离子全部由水电离产生,水电离出的c(OH-)=10-2mol·L-1,C错误; D选项考察物料守恒,Na原子与CH3COO原子团个数比为1:2,D正确。
12.【答案】B
【解析】电解质限定的对象是化合物,而Cl2是单质,故不属于电解质,A错误;铜与浓硝酸反应时体现了浓硝酸的酸性和强氧化性,B正确;Li与Na属于同一主族元素,但钠的金属性比Li强,故Li与O2共热反应产物为Li2O,C错误;HF可与玻璃的主要成分之一SiO2反应,但HF电离程度小,属于弱酸,D错误。
22.【答案】A B
【解析】BaSO4的溶解度小于BaCO3,即KSP(BaSO4)<KSP(BaCO3),但在CO32-浓度较大的溶液中,BaSO4溶解于水中的Ba2+ 能与CO32-结合形成BaCO3沉淀,A错误。CO2气体通入足量的CaCl2溶液中不会出现沉淀,B错误; NH3为碱性气体,可使湿润的红色石蕊试纸变蓝,C正确;乙醇的醇羟基具有一定的还原性,可被酸性高锰酸钾溶液氧化,D正确
23.【答案】AC
【解析】含Al3+的盐溶液可能呈酸性,含AlO2-的盐溶液可能呈碱性,故X元素为Al,再根据元素在周期表中位置可推断出R、T、Z、Q元素分别为:F、Si、S,Cl。Al、Si和S的电子层数目比F多,故原子半径大,当电子层数目相同时,核电荷数越大,原子半径越小, A正确;非金属性与相应简单离子的还原性呈反比,非金属性S<Cl,故简单气态氢化物还原性比较:HCl﹤H2S,B错误;Al2O3为活泼金属氧化物,是离子化合物,C正确;Cl元素的氧化物对应的水化物有可能是HClO,HClO为弱酸,D错误。
30.【答案】(1)C9H8O4(1分) 4(1分)
(2)(2分) 取代反应(1分)
(3)(2分)
(3分)
(4)(3分) (其它合理答案也给分)
(5)(3分)
【解析】(1)化合物Ⅱ的分子式为C9H8O4,其中的苯环和醛基均可与氢气发生加成反应,故1mol该物质与H2完全加成需要消耗氢气4mol。
(2)化合物Ⅰ中碳碳双键可与溴发生加成产物,前后结构可判断出化合物Ⅳ生成化合物Ⅱ的反应为取代反应。
(3)结合化合物Ⅲ的分子式,再结合核磁共振氢谱有两组吸收峰且峰面积之比为为6:1,即可推断出化合物Ⅲ的结构简式。
(4)苯环上的一氯代物只有2种,推断可能是在苯环有2个取代基且处于对位,可发生水解反应,且水解产物能使FeCl3溶液显色,推断出苯环上其中一个取代基是甲酸酯,再结合化合物Ⅱ的分子式,即可推断出正确结构。
(5)反应①原理是-COCl断C-Cl键,醇羟基断H,再重新形成新的官能团酯基,类推出化合物Ⅴ:在相同条件下-NH-断H,-COCl断C-Cl键,重新结合生成肽键。
31.【答案】
(1)△H1+2△H2-△H3(2分)
(2)CD(4分)
(3)① 0.50;1.00;0.20;791.02(各1分,共4分)
②解:
V(CH3CH2OH) = ![]() 0.04
0.04![]() /(L·min)(2分)
/(L·min)(2分)
V(CO) = 2V(CH3CH2OH) =0.08![]() /(L·min)(1分)
/(L·min)(1分)
(4)(3分)
【解析】(1)根据盖斯定律即可得出△H1+2△H2-△H3
(2)增大容器容积和移去部分CO2, 减小了浓度,正逆反应速率均降低。
(3)①
根据反应进行到10min时给出的浓度列出三段式:
2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
起始(mol·L-1): 2.00 4.00 0 0
转化(mol·L-1): 0.80 1.60 0.40 0.40
10min时(mol·L-1):1.20 2.40 0.40 0.40
CO和H2的起始浓度分别为2.00 mol·L-1和4.00 mol·L-1。
30min时,CH3CH2OH浓度为0.75 mol·L-1,所以CO浓度为:2.00 mol·L-1-0.75 mol·L-1×2=0.50 mol·L-1,H2的浓度为:4.00mol·L-1-0.75 mol·L-1×4=1.00mol·L-1,50min时反应已经达到平衡,浓度不发生改变,故c3=0.20 mol·L-1。根据平衡常数K的计算公式以及反应进行到50min时的数据得:K=![]() ;
;
②计算CO的平均反应速率可先计算出乙醇的平均反应速率,再根据速率之比等于化学计量数之比,可知CO的平均反应速率是乙醇的平均反应速率的2倍。
(4)作图时注意,催化剂只加快反应速率,不改变转化率,增大容器体积,压强减小,反应速率减慢,平衡逆向移动,H2的转化率减小。
32.【答案】(1)4FeS+3O2+6H2SO4![]() 2Fe2(SO4)3+6H2O+4S(3分)
2Fe2(SO4)3+6H2O+4S(3分)
(2)c(2分) (3)铁粉(2分) (4)蒸发(浓缩)、(冷却)结晶、过滤、洗涤(3分)
(5)促进Fe3+的水解(3分) (6)31.11%(3分)
【解析】(1)根据固体W的成分中存在S,推出FeS和O2、H2SO4发生氧化还原反应,FeS作还原剂,O2作氧化剂,产物有Fe2(SO4)3、S、H2O。
(2)污染物是SO2,用碱液吸收。
(3)溶液X中的铁是Fe3+,绿矾中的铁为Fe2+,故应加入铁粉,将Fe3+还原为Fe2+。
(4)将滤液进行蒸发浓缩,待有大量晶体析出时,冷却结晶,然后过滤,并洗涤沉淀。
(5)温度过低水解程度低,升高温度促进Fe3+的水解,过高温度不利于聚铁的形成。
(6)③得到的沉淀是BaSO4,n(BaSO4)=![]() =0.015 mol,根据聚铁主要成分为[Fe(OH)SO4]n,推出n(Fe3+)=0.015 mol,则m(Fe3+)=0.84 g,铁元素的质量分数:w(Fe)=(0.84 g/2.700 g)×100%=31.11%。
=0.015 mol,根据聚铁主要成分为[Fe(OH)SO4]n,推出n(Fe3+)=0.015 mol,则m(Fe3+)=0.84 g,铁元素的质量分数:w(Fe)=(0.84 g/2.700 g)×100%=31.11%。
33.【答案】(1)①B (2分)②酸性高锰酸钾(或溴水)(1分);将SO2气体通入H2S溶液中,见到产生黄色沉淀,证明SO2具有氧化性(2分)。
(2)①1 6 14 2 6 7 H2O(3分)
②
②(3分)
③Fe-2e-=== Fe2+;(2分) 电解池工作时,阳极铁放电产生Fe2+,与酸性Cr2O72-溶液发生氧化还原反应,生成Cr3+,同时阴极H+得电子,溶液中OH-浓度增大,OH-与Cr3+产生Cr(OH)3沉淀。(3分)
【解析】(1)①a装置中铁遇冷浓硫酸发生钝化,阻止其进一步反应,故不能用于制取SO2气体,A错误;b装置根据现象可得出结论,酸性:H2SO4﹥H2CO3,且两种酸中S和C元素均是最高价,故可进一步推断出非金属性:S﹥C ,B正确;c装置CO2也可与饱和碳酸钠溶液反应,C错误;SO2具有漂白性也具有较强的还原性,当SO2气体遇到氧化性较强的溴水溶液时,发生氧化还原反应,体现了SO2的还原性,而不是漂白性,D错误。
②SO2具有还原性,可与强氧化性溶液反应,如酸性高锰酸钾溶液或溴水溶液等,SO2与H2S,根据价态归中原理,反应生成了S单质,SO2中S的化合价降低,体现其具有氧化性。
(2)①该反应为氧化还原反应,配平时可先根据电子得失数目相等进行配平,再根据电荷守恒以及原子个数守恒即可得出正确答案。
②设计时应注意,该电化学装置需能够快速提供还原性Fe2+,故只能是电解池装置,且阳极材料为铁片。
③阳极材料为铁皮,活性电极,工作时电极材料自身放电,电极反应式:Fe-2e-=== Fe2+;Fe2+继续与与废水中的Cr2O72-溶液发生氧化还原反应,生成Cr3+,同时阴极H+得电子,溶液中OH-浓度增大,OH-与Cr3+产生Cr(OH)3沉淀。
物理答案
13.B
14.C
15.D
16.C
17.BD
18.AC
19.AD
20.AD
21.AD
34.(1)①交流(1分) 0.02(1分) ②A(2分)
③相等时间间隔内的位移差相等(2分,其它意思表述正确的同样给这2分);0.532(1分,0.531也给分) 1.13(1分)
(2)①1.55(2分)偏小(2分)
②2.2(2分)
③1.54~1.64(2分), 1.24~1.39 (2分)
35.(1)由楞次定律可判断通过电阻R1上的电流方向为从b到a(2分)
(2)由图(b)可知,0至t1时间内,磁感应强度的变化率:![]() ①(1分)
①(1分)
由法拉第电磁感应定律有![]() ②(2分)
②(2分)
而![]() ③(1分)
③(1分)
由闭合电路欧姆定律有![]() ④(2分)
④(2分)
联立以上各式解得,通过电阻![]() 上的电流大小为
上的电流大小为![]() ⑤(2分)
⑤(2分)
(3)由于金属板间的电场强度方向向上,带电微粒所受电场力与场强方向相同,带正电.
设带电微粒带电量为q,有:mg=qE⑥(2分)
金属板两板间电压U=I1R1⑦(2分)
电场强度大小![]() ⑧(2分)
⑧(2分)
⑤~⑧式联立,得:![]() ⑨(2分)
⑨(2分)
36.解:
(1)小球A与B发生弹性正碰,根据动量守恒定律:
![]() ①(2分)
①(2分)
碰撞过程无动能损失:
![]() ②(2分)
②(2分)
其中![]()
碰后小球B上摆过程,由机械能守恒定律:
![]() ③(1分)
③(1分)
以上三式联立,代入数值得:v0=3m/s (1分)
vB=4m/s
vA=1m/s
(2)碰后小球A做平抛运动,设下落至圆桶顶端的时间为t1,下落至底端的时间为t2,有:
![]() ④(1分)
④(1分)
![]() ⑤(1分)
⑤(1分)
解得:t1=0.4st2=0.6s
i)圆桶转动的周期![]() ,说明小球A下落至圆桶顶端时,长孔恰好又处于圆桶的正上方.此时小球A的水平位移
,说明小球A下落至圆桶顶端时,长孔恰好又处于圆桶的正上方.此时小球A的水平位移![]() ,s<x1<s+d,说明小球恰好能够落入长孔,不与桶壁相碰. (2分)
,s<x1<s+d,说明小球恰好能够落入长孔,不与桶壁相碰. (2分)
ii)小球A在桶内下落的时间△t=t2–t1= 0.2s =![]() ,说明小球A下落至圆桶底端时,长孔又恰好又处于圆桶的正下方.
,说明小球A下落至圆桶底端时,长孔又恰好又处于圆桶的正下方.
此时小球A的水平位移![]() ,s<x2<s+d,说明小球A恰好能够穿出长孔,不与桶壁相碰. (2分)
,s<x2<s+d,说明小球A恰好能够穿出长孔,不与桶壁相碰. (2分)
(3)由(2)中分析知,小球A不与长孔左边相碰的条件为:
![]() ⑥(2分)
⑥(2分)
小球A不与长孔右边相碰的条件为:
![]() ⑦(2分)
⑦(2分)
由①②式可得,![]() ⑧(1分)
⑧(1分)
⑥~⑧式联立,得![]() (1分,也可用①②⑥⑦联立得出,⑧式的1分并入这里,得2分)
(1分,也可用①②⑥⑦联立得出,⑧式的1分并入这里,得2分)