
最新!2022湖南物理高考真题及答案解析出炉
06月11日
2012年普通高等学校招生全国统一考试(天津卷)
理科综合
物理部分
第Ⅰ卷
一,单项选择题(每小题6分,共30分。每小题给出的四个选项中,只有一个选项是正确的)
 原子核所含核子单独存在时的总质量小于该原子核的质量
原子核所含核子单独存在时的总质量小于该原子核的质量2. 如图所示,金属棒MN两端由等长的轻质细线水平悬挂,处于竖直向上的匀强磁场中,棒中通以由M向N的电流,平衡时两悬线与竖直方向夹角均为,如果仅改变下列某一个条件,θ角的相应变化情况是
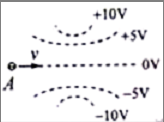
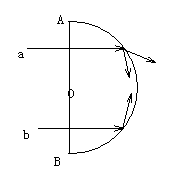
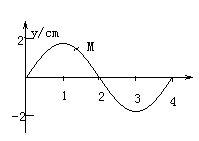
8. 如图甲所示,静止在水平地面的物块A,受到水平向右的拉力F的作用,F与时间t的关系如图乙所示,设物块与地面的静摩擦力最大值fm与滑动摩擦力大小相等,则
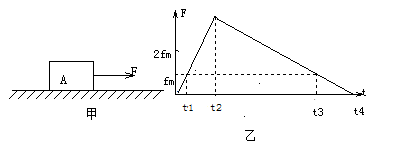
A.0—t1时间内F的功率逐渐增大
B.t2时刻物块A的加速度最大
C.t2时刻后物块A做反向运动
D.t3时刻物块A的动能最大
第二卷
注意事项:
1. 用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2. 本卷共4题,共72分。
9.(18分)
(1)质量为0.2kg的小球竖直向下以6m/s的速度落至水平地面,再以4m/s的速度反向弹回,取竖直向上为正方向,则小球与地面碰撞前后的动量变化为 kg•m/s。
若小球与地面的作用时间为0.2s,则小球受到地面的平均作用力大小为 N(g=10m/s2)。
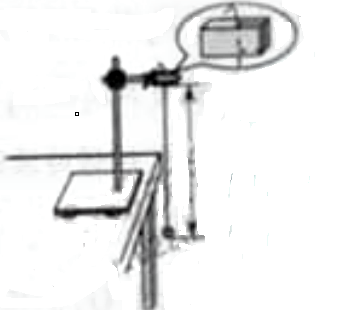 (2)某同学用实验的方法探究影响单摆周期的因素。
(2)某同学用实验的方法探究影响单摆周期的因素。
①他组装单摆时,在摆线上端的悬点处,用一块开有狭缝的橡皮夹牢摆线,再用铁架台的铁夹将橡皮夹紧,如图所示。这样做的目的是 (填字母代号)。
A.保证摆动过程中摆长不变
B.可使周期测量得更加准确
C.需要改变摆长时便于调节
D.保证摆球在同一竖直平面内摆动

②他组装好单摆后在摆球自然悬垂的情况下,用毫米刻度尺从悬点量到摆球的最低端的长度L=0.9990m,再用游标卡尺测量摆球直径,结果如图所示,则摆球的直径为 mm,单摆摆长为 m。
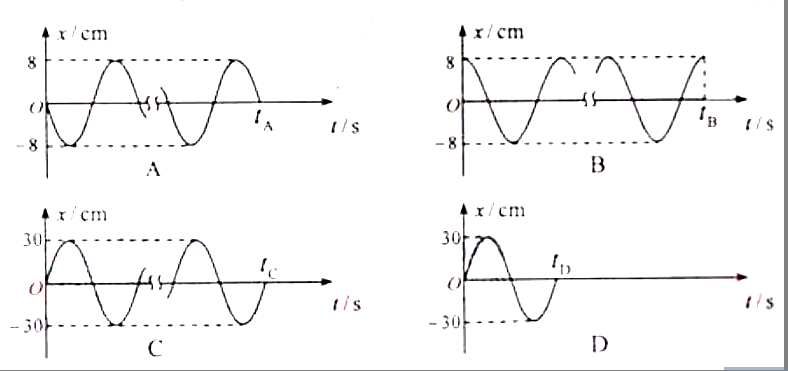
③下列摆动图像真实地描述了对摆长约为1m的单摆进行周期测量的四种操作过程,图中横坐标原点表示计时开始,A、B、C均为30次全振动图像,已知sin5°=0.087,sin15°=0.026,
这四种操作过程合乎实验要求且误差最小的是 (填字母代号)
(3)某同学在进行扩大电流表量程的实验时,需要知道电流表的满偏电流和内阻。他设计了一个用标准电流表G1来校对待测电流表G2的满偏电流和测定G2内阻的电路,如图所示。已知G1的量程略大于G2的量程,图中R1为滑动变阻器。R2为电阻箱。该同学顺利完成了这个实验。
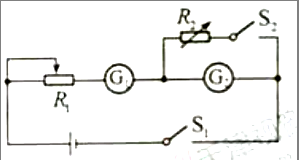
①实验过程包含以下步骤,其合理的顺序依次为__________________

②仅从实验设计原理上看,用上述方法得到的G2内阻的测量值与其真实值相比_______(填偏大、偏小或相等)
③若要将G2的量程扩大为I,并结合前述实验过程中测量得结果,写出须在G2上并联的分流电阻RS的表达式,RS=
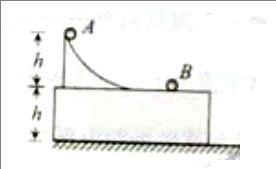 10、如图所示,水平地面上固定有高为h的平台,台面上固定有光滑坡道,坡道顶端局台面高也为h,坡道底端与台面相切。小球A从坡道顶端由静止开始滑下,到达水平光滑的台面后与静止在台面上的小球B发生碰撞,并粘连在一起,共同沿台面滑行并从台面边缘飞出,落地点与飞出点的水平距离恰好为台高的一半。两球均可视为质点,忽略空气阻力,重力加速度为g。求
10、如图所示,水平地面上固定有高为h的平台,台面上固定有光滑坡道,坡道顶端局台面高也为h,坡道底端与台面相切。小球A从坡道顶端由静止开始滑下,到达水平光滑的台面后与静止在台面上的小球B发生碰撞,并粘连在一起,共同沿台面滑行并从台面边缘飞出,落地点与飞出点的水平距离恰好为台高的一半。两球均可视为质点,忽略空气阻力,重力加速度为g。求
(1)小球A刚滑至水平台面的速度VA
(2)A、B两球的质量之比ma:mb
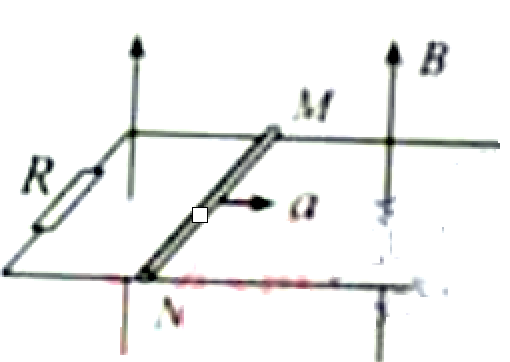 11.(18分)如图所示,一对光滑的平行金属导轨固定在同一水平面内,导轨间距L=0.5m,左端接有阻值R=0.3Ω的电阻,一质量m=0.1kg,电阻r=0.1Ω的金属棒MN放置在导轨上,整个装置置于竖直向上的均强磁场中,磁场的磁感应强度B=0.4T。棒在水平向右的外力作用下,由静止开始a=2m/s2的加速度做均加速运动,当棒的位移x=9m时撤去外力,棒继续运动一段距离后 停下来,已知撤去外力前后回路中产生的焦耳热比Q1:Q2=2:1.导轨足够长且电阻不计,棒在运动过程中始终与导轨垂直且两端与导轨保持良好接触。求
11.(18分)如图所示,一对光滑的平行金属导轨固定在同一水平面内,导轨间距L=0.5m,左端接有阻值R=0.3Ω的电阻,一质量m=0.1kg,电阻r=0.1Ω的金属棒MN放置在导轨上,整个装置置于竖直向上的均强磁场中,磁场的磁感应强度B=0.4T。棒在水平向右的外力作用下,由静止开始a=2m/s2的加速度做均加速运动,当棒的位移x=9m时撤去外力,棒继续运动一段距离后 停下来,已知撤去外力前后回路中产生的焦耳热比Q1:Q2=2:1.导轨足够长且电阻不计,棒在运动过程中始终与导轨垂直且两端与导轨保持良好接触。求
(1)棒在匀加速运动过程中,通过电阻R的电荷量q;
(2)撤去外力后回路中产生的焦耳热Q2;
(3)外力做的功Wf。
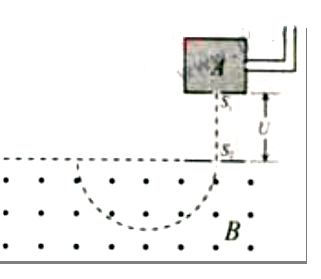 12.(20分)对铀235的进一步研究在核能的开发和利用中具有重要的意义。如图所示,质量为m、电荷量为q的铀235离子,从容器A下方的小孔S1不断飘入加速电场,其初速度可视为零,然后经过小孔S2垂直与磁场方向进入磁感应强度为B的均强磁场中,做半径为R的均速圆周运动,离子行进半个圆周后离开磁场并被收集,离开磁场时离子束的等效电流I。不考虑离子重力及离子间的相互作用。
12.(20分)对铀235的进一步研究在核能的开发和利用中具有重要的意义。如图所示,质量为m、电荷量为q的铀235离子,从容器A下方的小孔S1不断飘入加速电场,其初速度可视为零,然后经过小孔S2垂直与磁场方向进入磁感应强度为B的均强磁场中,做半径为R的均速圆周运动,离子行进半个圆周后离开磁场并被收集,离开磁场时离子束的等效电流I。不考虑离子重力及离子间的相互作用。
(1)求加速电场的电压U;
(2)求出在离子被收集的过程中任意间t内收集到离子的质量M;
(3)实际上加速电压的大小在U±ΔU范围内微小变化。若容器A中有电荷量相同的铀235和铀238两种离子,如前述情况它们经电场加速后进入磁场中发生分离,为使这两种离子在磁场中运动的轨迹不发生交叠,![]() 应小于多少?(结果用百分数表示,保留两位有效数字)
应小于多少?(结果用百分数表示,保留两位有效数字)
2012年普通高等学校招生全国统一考试(天津卷)
理科综合 生物部分
理科综合共300分,考试用时150分钟
生物试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至2页,第Ⅱ卷3至5页,共80分。
答卷前,考生务必将自己的姓名、准考号填写在答题卡上,并在规定位置粘贴考试用条形码。答卷时,考试务必将答案涂写在答题卡上,答在试卷上的无效。考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第Ⅰ卷
注意事项:

据图分析,下列叙述错误的是
 ①、②两过程均需要植物激素来诱导细胞脱分化
①、②两过程均需要植物激素来诱导细胞脱分化其对刺激的适应能力。右图为皮质醇分泌的调节示
意图。据图分析,下列叙述错误的是
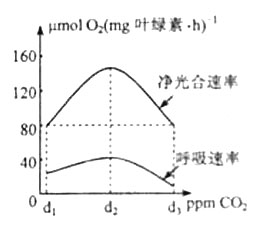 5.设置不同CO2浓度,分组光照培养蓝藻,测定净光合速率和呼吸速率(光合速率=净光合速率+呼吸速率),结果见右图。据图判断,下列叙述正确的是
5.设置不同CO2浓度,分组光照培养蓝藻,测定净光合速率和呼吸速率(光合速率=净光合速率+呼吸速率),结果见右图。据图判断,下列叙述正确的是
A.与d3浓度相比,d1浓度下单位时间内蓝藻细胞光反应生成的[H]多
B.与d2浓度相比,d3浓度下单位时间内蓝藻细胞呼吸过程产生的ATP多
C.若d1、d2、d3浓度下蓝藻种群的K值分别为K1、K2、K3,则K1>K2>K3
D.密闭光照培养蓝藻,测定种群密度及代谢产物即可判断其是否为碱性厌氧生物
6.果蝇的红眼基因(R)对白眼基因(r)为显性,位于X染色体上;长翅基因(B)对残翅基因(b)为显性,位于常染色体上。现有一只红眼长翅果蝇与一只白眼长翅果蝇交配,F1代的雄果蝇中约有1/8为白眼残翅。下列叙述错误的是
A.亲本雌果蝇的基因型是BbXRXr
B.亲本产生的配子中含Xr的配子占1/2
C.F1代出现长翅雄果蝇的概率为3/6
D.白眼残翅雌果蝇能形成bbXrXr类型的次级卵母细胞
2012年普通高等学校招生全国统一考试(天津卷)
理科综合 生物部分
第II卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共3题,共44分。
7.(13分)生物分子间特异性结合的性质广泛用于生命科学研究。以下实例为体外处理“蛋白质-DNA复合体”获得DNA片段信息的过程图。
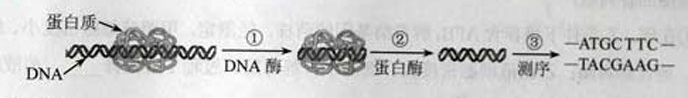
据图回答:
(1)过程①酶作用的部位是 键,此过程只发生在非结合区DNA,过程②酶作用的部位是 键
(2)①、②两过程利用了酶的 特性。
(3)若将得到的DNA片段用于构建重组质粒,需要将过程③的测序结果与 酶的识别序列进行比对,以确定选用何种酶。
(4)如果复合体中的蛋白质为RNA聚合酶,则其识别、结合的DNA序列区为基因的 。
(5)以下研究利用了生物分子间特异性结合性质的有(多选)。
A.分离得到的核糖体,用蛋白酶酶解后提取rRNA
B.用无水乙醇处理菠菜叶片,提取叶绿体基粒膜上的光和色素
C.通过分子杂交手段,用荧光物质标记的目的基因进行染色体基因定位
D.将抑制成熟基因导入番茄,其mRNA与催化成熟酶基因的mRNA互补结合,终止后者翻译,延迟果实成熟
8.(20分)黄曲霉毒素B1(AFB1)存在于被黄曲霉菌污染的饲料中,它可以通过食物链进入动物体内并蓄积,引起癌变。某些微生物能表达AFB1解毒酶,将该酶添加在饲料中可以降解AFB1,消除其毒性。
回答下列问题:
(1)AFB1属于 类致癌因子。
(2)AFB1能结合在DNA的G上,使该位点受损伤变为G·在DNA复制中,G·会与A配对。现有受损伤部位的序列为![]() ,经两次复制后,该序列突变为 。
,经两次复制后,该序列突变为 。
(3)下图为采用基因工程技术生产AFB1解毒酶的流程图。
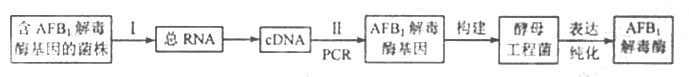
据图回答问题:
①在甲、乙条件下培养含AFB1解毒酶基因的菌株,经测定,甲菌液细胞密度小、细胞含解毒酶:乙菌液细胞膜密度大、细胞不含解毒酶。过程I应选择 菌液的细胞提取总RNA,理由是 。
②过程II中,与引物结合的模板是 。
③检测酵母过程菌是否合成了AFB1解毒酶。应采用 方法。
(4)选取不含AFB1的饲料和某种实验动物为材料,探究该AFB1解毒酶在饲料中的解毒效果。实验设计及测定结果见下表。

据表回答问题:
①本实验的两个自变量分别为 。
②本实验中,反映出AFB1解毒酶解毒效果的对照组是 。
③经测定,某污染饲料中AFB1含量为100μg/kg,则每千克饲料应添加 克 解毒酶,解毒效果最好,同时节约了成本。
(5)采用蛋白质工程进一步改造该酶的基本途径是:从提高酶的活性出发,设计预期的蛋白质结构,推测应有的氨基酸序列,找到相对应的 序列
9.(11分)夏初。在某河口多地点采集并测定水样,结果表明,各采样点无机氮浓度相近,而无机磷浓度差异较大。按无机磷浓度由低到高的顺序,绘制各采样点对应的浮游植物和浮游动物的密度曲线,结果如下图。
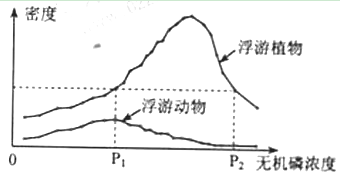
据图回答:
(1)磷元素进入浮游植物细胞后,以 分子的形式成为细胞膜支架的成分;在细胞内,磷元素通过参与 反应(写反应式),保持细胞内ATP含量的相对稳定。
(2)分析发现,P1、P2采样点浮游植物种类差别非常明显,从进化角度分析,这是
的结果。
(3)无机磷浓度高于P1的采样点,浮游动物的密度反而比P1采样点低,下列有关其原因分析,不可能的是(单选)。
A.可被浮游动物取食的浮游植物种类较少
B.水体溶解氧较高
C.浮游动物的捕食者数量较多
D.水体有害物质浓度较高
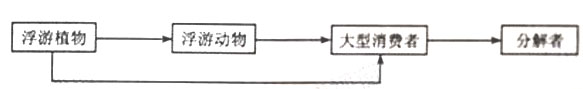
(4)请用箭头补充完成该河口生物群落中氮元素的流向图。、
绝密★启用前
2012年普通高等学校招生全国统一考试(天津卷)
理科综合 化学部分
理科综合共300分,考试用时150分钟。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至2页,第Ⅱ卷3至6页,共100分。
答卷前,考生务必将自己的姓名、准考号填写在答题卡上,并在规定位置粘贴考试用条形码。答卷时,考生务必将答案涂写在答题卡上,答在试卷上的无效。考试结束后,将本试卷和答题卡一并交回。
祝各位考生考试顺利!
第Ⅰ卷
注惹事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
2.本卷共6题,每题6分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:相对原子质量:H 1 O 16 S 32 Cu 64
1.根据下列物质的化学性质,判断其应用错误的是 ( )
A.酒精能使蛋白质变性,可用于杀菌消毒
B.CaO能与SO2反应,可作工业废气的脱硫剂
C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
D.镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料
2.下列单质或化合物性质的描述正确的是 ( )
A.NaHSO4水溶液显中性B.SiO2与酸、碱均不反应
C.NO2溶于水时发生氧化还原反应D.Fe在足量Cl2中燃烧生成FeCl2和FeCl3
3.下列叙述正确的是 ( )
A.乙酸与丙二酸互为同系物
B.不同元素的原子构成的分子只含极性共价键
C.![]() U和
U和![]() U是中子数不同质子数相同的同种核素
U是中子数不同质子数相同的同种核素
D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
4.完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是 ( )
| A | B | C | D | |
| 实 验 | 用CCl4提取 溴水中的Br2 | 除去乙醇中的苯酚 | 从KI和I2的固体 混合物中回收I2 | 配制100 mL 0.1000 mol·L-1K2Cr2O7溶液 |
| 装 置 或 仪 器 | 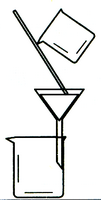 | 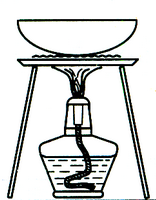 | 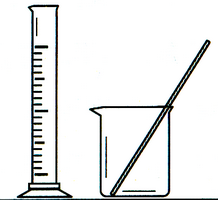 |
5.下列电解质溶液的有关叙述正确的是 ( )
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含l mol KOH的溶液与l mol CO2完全反应后,溶液中c(K+)=c(HCO![]() )
)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
6.已知2SO2 (g) + O2(g)![]() 2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是 ( )
2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是 ( )
A.容器内压强P:P甲=P丙 >2P乙B.SO3的质量m:m甲=m丙 >2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙 >k乙D.反应放出或吸收热量的数值Q:Q甲=G丙 >2Q乙
绝密★启用前
2012年普通高等学校招生全国统一考试(天津卷)
理科综合 化学部分
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共4题,共64分。
7.(14分)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
⑴ Y在元素周期表中的位置为________________。
⑵ 上述元素的最高价氧化物对应的水化物酸性最强的是_______________(写化学式),非金属气态氢化物还原性最强的是__________________(写化学式)。
⑶ Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
⑷ X2M的燃烧热ΔH = -a kJ·mol-1,写出X2M燃烧反应的热化学方程式:
________________________________________________________________________。
⑸ ZX的电子式为___________;ZX与水反应放出气体的化学方程式为___________________________。
⑹ 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:
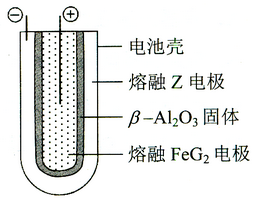 2Z + FeG2
2Z + FeG2 ![]() Fe + 2ZG
Fe + 2ZG
放电时,电池的正极反应式为__________________________:
充电时,______________(写物质名称)电极接电源的负极;
该电池的电解质为___________________。
8.(18分)萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成a-萜品醇G的路线之一如下:
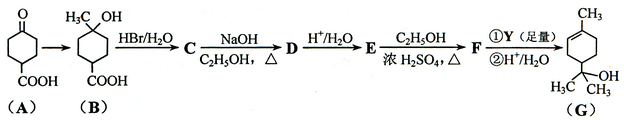
已知:RCOOC2H5![]()
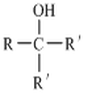
请回答下列问题:
⑴ A所含官能团的名称是________________。
⑵ A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式:
______________________________________________________________________。
⑶ B的分子式为_________;写出同时满足下列条件的B的链状同分异构体的结构简式:_____________。
① 核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
(4) B → C、E → F的反应类型分别为_____________、_____________。
⑸ C → D的化学方程式为________________________________________________________。
⑹ 试剂Y的结构简式为______________________。
⑺ 通过常温下的反应,区别E、F和G的试剂是______________和_____________。
⑻ G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式:________________________。
9.(18分)信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
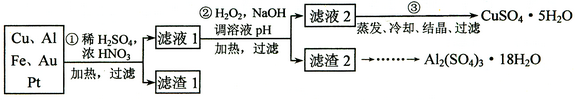
请回答下列问题:
⑴ 第①步Cu与酸反应的离子方程式为___________________________________________;
得到滤渣1的主要成分为___________________。
⑵ 第②步加H2O2的作用是_____________________,使用H2O2的优点是___________________________;调溶液pH的目的是使________________________________________生成沉淀。
⑶ 用第③步所得CuSO4·5H2O制备无水CuSO4的方法是________________________________________。
⑷ 由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
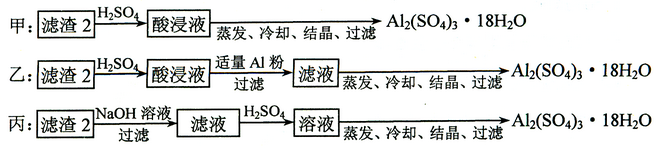
上述三种方案中,_________________方案不可行,原因是_____________________________:
从原子利用率角度考虑,___________方案更合理。
⑸ 探究小组用滴定法测定CuSO4·5H2O (Mr=250)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol LL-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液6 mL。滴定反应如下:Cu2+ + H2Y2- = CuY2- + 2H+
写出计算CuSO4·5H2O质量分数的表达式ω= _____________________________ ;
下列操作会导致CuSO4·5H2O含量的测定结果偏高的是_____________。
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡 c.未除净可与EDTA反应的干扰离子
10.(14分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s) + 3H2(g)![]() W (s) + 3H2O (g)
W (s) + 3H2O (g)
请回答下列问题:
⑴ 上述反应的化学平衡常数表达式为___________________________。
⑵ 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____________________;随温度的升高,H2与水蒸气的体积比减小,则该反应为反应(填“吸热”或“放热”)。
⑶ 上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3W2O5WO2W |
第一阶段反应的化学方程式为___________________________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________________________________。
⑷ 已知:温度过高时,WO2(s)转变为WO2(g);
WO2 (s) + 2H2(g)![]() W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2![]() W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g);ΔH = -137.9 kJ·mol-1
则WO2(s)![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
⑸ 钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2(g)![]() WI4(g)。下列说法正确的有________________。
WI4(g)。下列说法正确的有________________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢






绝密★启用前
2012年普通高等学校招生全国统一考试(天津卷)
理科综合化学部分参考答案
Ⅰ卷共6题,每题6分,共36分。
1·C 2.C 3.D 4.A 5.D 6.B
Ⅱ卷共4题,共64分。
7.(14分)
⑴ 第二周期第ⅥA族
⑵ HClO4H2S
⑶ Cl2、O3、ClO2(任写两种,其他合理答案均可)
⑷ H2S (g) + O2 (g)= SO2 (g) + H2O (l);ΔH = -a kJ·mol-1
⑸ Na+[![]() ]- NaH + H2O = NaOH + H2↑
]- NaH + H2O = NaOH + H2↑
⑹ Fe2+ + 2e- = 一Fe 钠 β-Al2O3
8.(18分)
⑴ 羰基、羧基
⑵ n ![]()
![]()
![]() + (n-1)H2O
+ (n-1)H2O
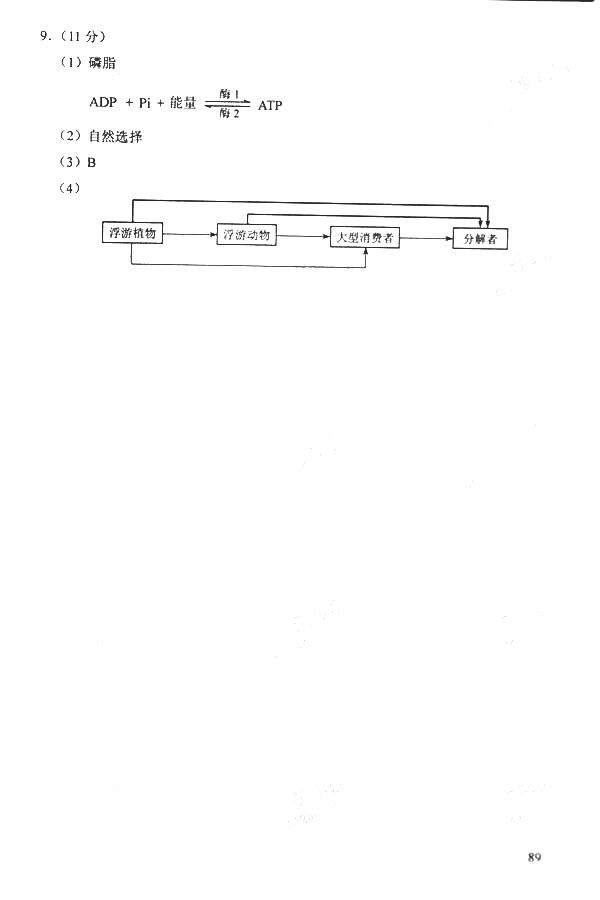
⑶ C8H14O3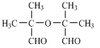
⑷ 取代反应 酯化反应(或取代反应)
⑸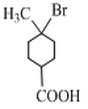 + 2NaOH
+ 2NaOH ![]()
![]() + NaBr + 2H2O
+ NaBr + 2H2O
⑹ CH3MgX(X=Cl、Br、I)
⑺ NaHCO3溶液 Na (其他合理答案均可)
⑻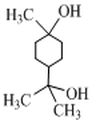
9.(18分)
⑴ Cu + 4H+ + 2NO![]()
![]() Cu2+ + 2NO2↑+ 2H2O 或3Cu + 8H+ + 2NO
Cu2+ + 2NO2↑+ 2H2O 或3Cu + 8H+ + 2NO![]()
![]() 3Cu2+ + 2NO↑+ 4H2O Au、Pt
3Cu2+ + 2NO↑+ 4H2O Au、Pt
⑵ 将Fe2+氧化为Fe3+ 不引入杂质,对环境无污染 Fe3+、Al3+
⑶ 加热脱水
⑷ 甲 所得产品中含有较多Fe2(SO4)3杂质 乙
⑸ × 100% c
10.(14分)
⑴ K =
⑵ 60% 吸热
⑶ 2WO3 + H2![]() W2O5 + H2O W2O5、WO21:1:4
W2O5 + H2O W2O5、WO21:1:4
⑷ +203.9 kJ·mol-1
⑸ a、b