
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日

班级:姓名:成绩:
说明:本试卷答题时间为90分钟,试卷满分为100分。
考生须知:试题所有答案必须填写在答题卡和答题纸上,在试卷上作答无效。
可能用到相对原子质量: H:1 C:12 O:16 Na:23 N:14 S:32 Cl:35.5
第一部分(共50分)
一.选择题(每题只有一个选项符合要求,每题2分,共50分)
1.在汽车加油站见到的油罐车上,所贴有的危险化学品标志是
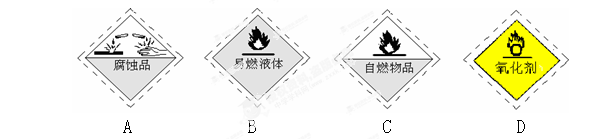
2.当光束通过下列分散系时,可观察到丁达尔效应的是
A.乙醇溶液 B.氯化钠溶液 C.硫酸铜溶液 D.氢氧化铁胶体
3.下列实验仪器不能用于混合物分离提纯的是
A.漏斗 B.蒸馏烧瓶 C.容量瓶 D.分液漏斗
4.小明体检的血液化验单中,葡萄糖为5.8mmol/L。表示该体检指标的物理量是
A.质量分数 B.溶解度 C.物质的量浓度 D.摩尔质量
5.用特殊方法把固体物质加工到纳米级(1nm~100nm)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是
A.溶液 B.悬浊液 C.胶体 D.乳浊液
6.下列物质不属于电解质的是
A.Cu B.KOH C.H2SO4D.Na2CO3
7.下列实验操作中不正确的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处。
C.蒸发时,要用玻璃棒不断搅动溶液
D.过滤时,将待过滤的液体直接倒入漏斗,使液面低于滤纸的边缘。
8.下列各组物质中,能用分液漏斗进行分离的是
A.酒精和水 B.碘和四氯化碳 C.水和四氯化碳 D.汽油和植物油
9.胶体区别于与其它分散系的本质特征是
A.胶体粒子直径在1-100nm之间 B.均一、稳定、透明
C.有丁达尔效应 D.胶体分散质能透过滤纸
10.下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是
A.石灰石 B.Ca(OH)2 C.CaCO3 D.CH4
11.下列离子在溶液中可大量共存的一组是
A. Ag+、H+、Cl-、OH- B. Na+、Ba2+、NO3-、CO32-
C. H+、Na+、CO32-、Cl- D. K+、Cu2+、NO3-、SO42-
12.下列解释实验事实的离子方程式不正确的是
A.Fe与稀H2SO4反应放出气体:Fe + 6H+![]() 2Fe3++3H2↑
2Fe3++3H2↑
B.稀H2SO4与BaCl2溶液反应生成沉淀:Ba2++![]() BaSO4↓
BaSO4↓
C.用大理石与稀盐酸制备CO2:CaCO3 + 2H+![]() Ca2++ CO2↑+ H2O
Ca2++ CO2↑+ H2O
D.碳酸钠溶液与足量稀盐酸:CO32-+ 2H+![]() CO2↑+ H2O
CO2↑+ H2O

14.下列电离方程式书写正确的是( )
| A.NaOH=Na++O2-+H+ | B.FeCl3=Fe3++Cl3- |
| C.Ca(NO3)2=Ca2++2(NO3)2- | D.H2SO4=2H++SO42- |
15.下列说法正确的是
A.在标准状况下,1mol水的体积是22.4L
B.1mol氢气所占的体积一定是22.4L
C.80gNaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L
D.标准状况下,28克N2和CO的混合气体,体积为22.4L
16.在无色透明的强酸性溶液中,能大量共存的是
A. Ca2+、K+、HCO3-、Na+ B. Fe3+、Cl-、H+、NO3-
C. Mg2+、Na+、NO3-、Cl- D. K+、OH-、Cl-、SO42-
17.瓦斯中甲烷与氧气的质量比为1:4时,极易爆炸,此时甲烷与氧气的体积比为
A.1:4 B.1:2 C.1:1 D.2:1
18.下列叙述正确的是
A.1molH2O的质量为18g/mol
B.CH4的摩尔质量是16g
C.6.02×1023个O2分子的质量为32g
D.标准状况下,1mol任何物质的体积均为22.4L
19.0.5L 1 mol·L–1的AlCl3溶液与0.2L 1mol·L–1的BaC12溶液中,Cl-的浓度比为
20.下列反应中,水作还原剂的是( )
A.2Na+2H2O![]() 2NaOH+H2↑ B.Cl2+H2O
2NaOH+H2↑ B.Cl2+H2O![]() HCl+HClO
HCl+HClO
C.2F2+2H2O![]() 4HF+O2D.SO2+H2O
4HF+O2D.SO2+H2O![]() H2SO3
H2SO3
21.下列说法一定正确的是
A.0.5 mol Cl2所占体积约为11.2 L
B.16 g O2中含有的分子数约为6.02×1023
C.0.1 mol/L NaCl溶液中含溶质的物质的量为0.1 mol
D.标准状况下,11.2 L N2和CO的混合气体所含原子数约为6.02×1023
22.现有3组混合物:①碘和氯化钠溶液 ② 汽油和柴油 ③苯和水,正确的分离方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
 C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
24.下列反应的离子方程式正确的是
A. Mg(OH)2和稀硫酸反应:H+ + OH-![]() H2O
H2O
B.碳酸钡与稀盐酸反应:CO32-+ 2H+![]() CO2↑+ H2O
CO2↑+ H2O
C.澄清石灰水跟盐酸:H+ + OH-![]() H2O
H2O
D.硫酸溶液与氢氧化钡溶液:H++SO42- + Ba2++ OH-![]() BaSO4↓+ H2O
BaSO4↓+ H2O
25.在反应3S+6KOH=K2SO3+2K2S+3H2O中,被氧化与被还原的硫原子数之比为
A.1:2 B.2:1 C.1:1 D.3:2
第二部分(共50分)
高温
26.(3分)工业上炼铁的主要反应为:Fe2O3+3CO![]() 2Fe+3CO2。其中,氧化剂是 (填化学式),被氧化的物质是 (填化学式);若反应中消耗了3 mol CO,则生成 mol Fe。
2Fe+3CO2。其中,氧化剂是 (填化学式),被氧化的物质是 (填化学式);若反应中消耗了3 mol CO,则生成 mol Fe。
27.(每空2分,共10分)写出下列反应的离子或化学方程式
①写出氢氧化铜与稀硫酸反应的离子方程式: 。
②写出碳酸氢钠与稀盐酸反应的离子方程式: 。
③写出离子方程式H++OH-=H2O相对应的一个化学方程
式: 。
④写出铁与硫酸铜溶液反应的离子方程式: 。
⑤写出离子方程式Ag++Cl-=AgCl↓相对应的一个化学方程
式: 。

(3)H2SO4 Ca(OH)2 Mg Na2CO3 ; ,
(4)CuSO4•5H2O 金刚石 食盐水 NaOH ; ,
(5)CO2NaHCO3CaCO3CH4。
29(每空1分,共6分)
写出除去下列物质中的杂质(括号内物质)所用的试剂,并写出发生的离子方程式。
(1)NaOH溶液(Na2CO3) , 。
(2)NaCl溶液(MgCl2) , 。
(3)KCl溶液(CuSO4) , 。
30(每空1分,共5分)某河道两旁有甲、乙两厂.它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和NO3-六种离子.
(1)甲厂的废水明显呈碱性,那么乙厂废水中含有的三种离子是; 。
(2)乙厂的废水中含有三种离子,如果向其中加入一定量 (选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属 (填写金属元素符号)
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的 (填写离子符号)转化为沉淀.经过滤后的废水主要含 ,可用来浇灌农田。
三.实验题(共18分)
31.(每空1分,共5分)对于混合物的分离或提纯,常用到的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。下列各组混合物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3颗粒。可用 的方法
除去Ca(OH)2溶液中悬浮的CaCO3颗粒。

32.[第(1)(3)(4)(6)问每空1分;(2)(5)每空2分,共13分]
粗食盐中常含有少量Ca2+、Mg2+、SO42-以及泥沙等杂质,实验室提纯NaCl的流程如下(加入的试剂稍过量)
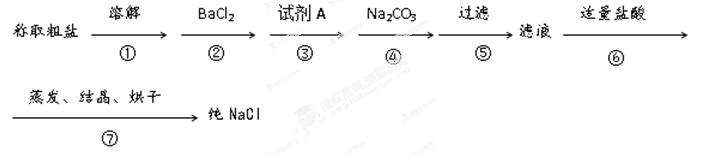
(1)步骤③中加入的试剂A是 (填化学式),其目的是 。
(2)第⑥步中,写出相应的离子方程式
。
(3)步骤⑤和⑥之间,若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是 。
(4)实验室提纯NaCl的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,其中过滤时,使用玻璃棒的目的是 。
(5)用上述方法获得的氯化钠去配制200mL0.1mol/LNaCl溶液。
①用托盘天平称氯化钠固体的质量是 g
②配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
③下列操作中,可能造成所配制溶液的浓度偏低的是 。
A、没有洗涤烧杯和玻璃棒 B、定容时,仰视刻度线读数
C、定容时,俯视刻度线读数 D、洗涤后的容量瓶中残留少量蒸馏水
(6)此方法获得的氯化钠溶液的导电性远远强于氯化钠固体,是因为氯化钠固体在水分子的作用下,电离成自由移动的离子,请写出相关的电离方程
式: 。
四、计算题(3分)
33.配制0.2mol/LNa2SO4溶液100mL,需要Na2SO4的质量是多少?
(要求写出计算过程及涉及的公式)

一.选择题(每小题2分,共50分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | D | C | C | C | A | D | C | A | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | A | A | D | D | C | B | C | D | C |
| 题号 | 21 | 22 | 23 | 24 | 25 | |||||
| 答案 | D | B | D | C | A |
二.填空题(共29分)
26.(每空1分,共3分) Fe2O3、CO、2
27.(每空2分,共10分)

28.(每空1分,共4分)(1)CO2(2)H2SO4 (3)Mg (4)食盐水 (5)CH4
29.(每空1分,共6分)
(1) Ca(OH)2或Ba(OH)2Ca2++CO32-=CaCO3↓或Ba2++CO32-=BaCO3↓
(2)NaOH Mg2++2OH-=Mg(OH)2↓
(3)Ba(OH)2Cu2++SO42-+Ba2++2OH-=BaSO4↓+Mg(OH)2↓
30.(每空1分,共5分)(1)Ag+、Cu2+、NO3- (漏填不得分,下同)
(2)铁粉 ;Ag、Cu
(3)Ag+、Cu2+、OH-、Cl- ; KNO3或K+和NO3-
三.实验题(共18分)
31.(每空1分,共5分)
(1)过滤 (2)蒸发 (3)萃取 (4)蒸馏 (5)加热分解
32.[(1)(3)(4)(6)每空1分;(2)(5)每空2分,共13分]
(1)NaOH;除去Mg2+
(2)H++OH-=H2O
2H++CO32-![]() CO2↑+ H2O (每个离子方程式1分)
CO2↑+ H2O (每个离子方程式1分)
(3)在酸性条件下,BaCO3、CaCO3、Mg(OH)2会溶解,从而使制得氯化钠的混有杂质 (答案合理可得分)
(4)引流
(5)①1.2
②200mL容量瓶
③AB
(6) NaCl = Na++Cl-
四、计算题(3分)
33、解: 100mL=0.1L ………1分
n(Na2SO4)=c(Na2SO4)·Vaq
=0.2mol/x0.1L
=0.02mol ………1分
m(Na2SO4)=n(Na2SO4)·M(Na2SO4)
=0.02molx142g/mol
=2.84g ………1分
答:略