
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
铜陵市一中2016-2017学年度第一学期
高一年级学段(期中)考试化学试卷
命题教师:凌崇忠审题教师:王玉红
考试时间:90分钟满分:100分
可能用到的相对原子质量:H:1 C:12 N:14 O:16Na:23 S:32 Cl:35.5
一、选择题(每题3分,共48分,每题只有一个选项符合题意)
1.固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
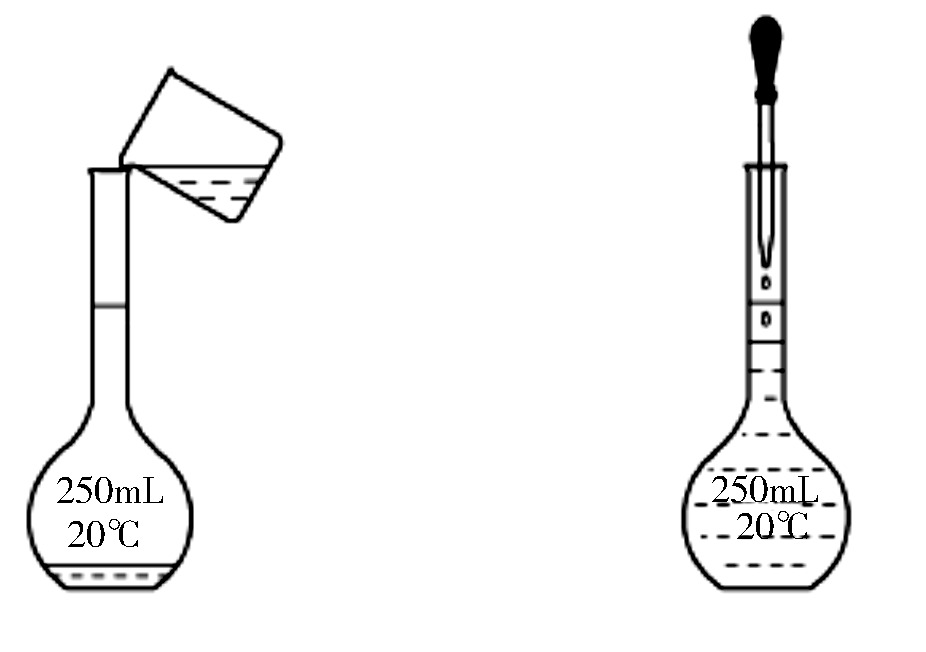
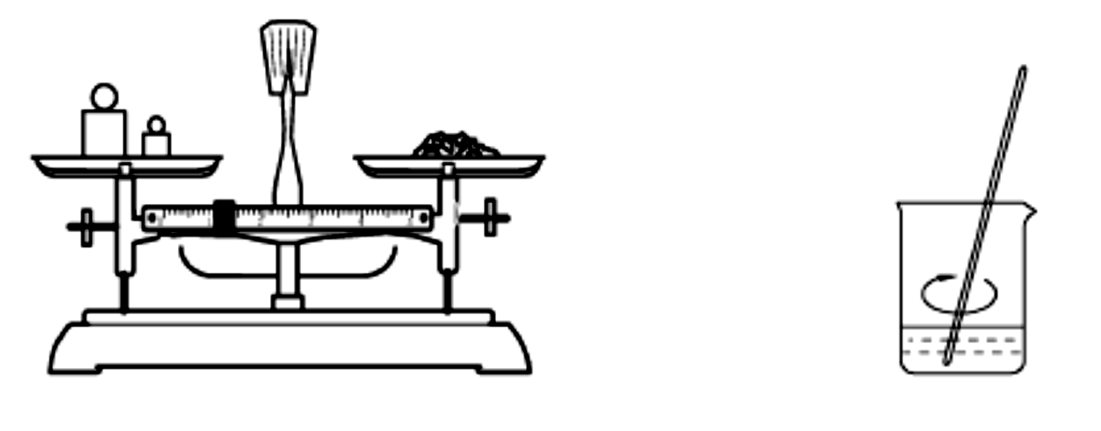
A.称量 B.溶解C.转移溶液 D.定容
2.下图所表示的一些物质、化学反应或概念间的从属关系不正确的是( )
| X | Y | 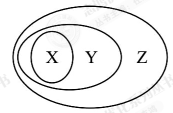 Z Z | |
| A | 碳在氧气中燃烧 | 氧化反应 | 化合反应 |
| B | 冰水混合物 | 电解质 | 化合物 |
| C | 淀粉溶液 | 胶体 | 分散系 |
| D | 干冰 | 氧化物 | 纯净物 |
3.下列混合物不采用蒸馏法分离的一组是( )
A.液态氮气和氧气B.盐酸中的水和氯化氢
C.乙醇和水D.四氯化碳和水
4.分类是人们认识事物时常用的科学方法,下列关于碳酸钾分类的说法错误的是( )
A.属于电解质 B.属于化合物
C.属于碳酸盐D.属于分散系
5.下列说法正确的是( )
A.NH3的摩尔质量为17g
B.1mol/L MgCl2溶液中含有1mol镁离子和2mol氯离子
C.1molN2的体积为22.4L
D.常压下200℃时,18克的水与2克H2体积比约为1:1
6.NA为阿伏伽德罗常数,下列说法不正确的是( )
A.常温常压下,28gCO和N2混合气体中含有的原子总数为2![]()
B.标准状况下,11.2L的水中含有水分子0.5NA
C.2molOH-中电子数为20NA
D.0.1mol FeCl3形成Fe(OH)3胶体,Fe(OH)3胶粒的数目小于0.1![]()
7.欲配制100ml 1.0 mol/L Na2SO4溶液,下列会使配得的溶液浓度偏小的是()
A.容量瓶中原有少量蒸馏水
B.定容时俯视凹液面
C.称量Na2SO4时,物质与砝码位置放反了(1克以下用游码)
D.将32.2g Na2SO4·10H2O溶于少量水中,再配制成100 ml溶液
8.下列各组中的离了,能在溶液中大量共存的是( )
A.SO42-、Na+、Cl-、Ba2+B.H+、Fe2+、NO3-、OH-
C.H+、K+、CO32-、HCO3-D.Na+、Cu2+、NO3-、SO42-
9.下列物质属于电解质并且能导电的是( )
A.Na2CO3·10H2O晶体B.熔融的Al2O3
C.稀硫酸 D.蔗糖
10.下列化学方程式中,不能用离子方程式,Ba2++SO42-=BaSO4↓表示的是( )
A.Ba(NO3)2+Na2SO4=BaSO4↓+2HNO3
B.BaCl2+H2SO4=BaSO4↓+2NaCl
C.Ba(OH)2+K2SO4=BaSO4↓+2KOH
D.Ba(OH)2+H2SO4=BaSO4↓+2H2O
11.下列说法正确的是( )
A.分离Br2和CCl4的混合物,用分液漏斗进行分液
B.500mL0.5mol/L的Al2(SO4)3溶液,取出50mL,其中SO42-浓度为1.5mol/L
C.蒸发时,应使混合物中的水分完全蒸干后,才能停止加热
资*源%库D.分液时,分液漏斗中下层液体从下口放出,上层液体从下口放到另一个烧杯
12.由N2和CO2组成的混合气体的密度在同温、同压下是氢气密度的16倍,则该混合气体中N2和CO2的体积比为()
A.7∶11B.11∶7C.3∶1D.1∶3
13.下列各组数值或物理量中,都不随水的“物质的量”的变化而变化的是()
资*源%库 A.水的密度;水的摩尔质量B.水的质量;水的相对分子质量
C.水的体积;水中所含原子的数目 D.水的沸点;水分子的数目
14.下列物质含有的氧原子数最多的是( )
A.32g O2和O3的混合气体
B.0.5mol CuSO4·5H2O晶体
C.6.02×1023个CO2分子
D.1L 1mol/L的稀H2SO4
15.某MgSO4和H2SO4的混合溶液中,c(Mg2+)=2mol/Lc(SO42-)=3mol/L,若将100mL此混合溶液中的Mg2+沉淀完全,最少需加2mol/L的NaOH溶液体积是( )
A.100mL B.200mL C.300mL D.400mL
16.关于Fe(OH)3胶体的说法正确的是( )
A.向NaOH溶液中,滴加饱和的FeCl3溶液,可制得Fe(OH)3胶体
B.FeCl3溶液和Fe(OH)3胶体,都能产生丁达尔效应
C.分散质的粒子,不能透过半透膜,也不能透过滤纸
D.逐滴加入稀硫酸,先产生沉淀后沉淀溶解
二、非选择题(共52分)
17.(8分)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
①②③④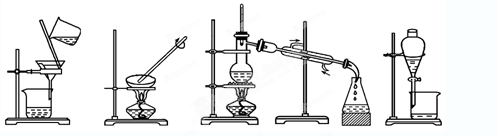
从海水中提取水:从KCl溶液中获取KCl晶体
分离CaCO3和水;分离植物油和水
18.(10分)按要求完成下列5小题
19.(10分)
实验室用密度为1.25g·mL-1,质量分数为36.5%的浓盐酸配制成240mL 0.1mol/L的稀盐酸,请回答:
(4)定容时,加水超过了刻度线,应怎样操作:
20.(8分)根据阿伏加德罗定律进行填空
密度之比
21.(10分)实验室需要纯净的NaCl溶液,但现有的NaCl晶体中混有少量的Na2SO4和(NH4)2CO3,设计实验除去杂质,并回答下列问题:
(1)除去(NH4)2CO3:加热样品,使其完全分解。判断(NH4)2CO3已经除尽的方法是:取少量加热后的固体,溶于水后加盐酸,若,证明(NH4)2CO3已经除尽。(NH4)2CO3溶于水能发生电离,其电离方程式为
(2)除去Na2SO4:把(1)加热后的样品溶于水形成溶液,向其中加入过量的BaCl2溶液,再加入过量的溶液,过滤后,向滤液中加入适量的即可。判断SO42-已经除尽的方法是:取少量加入BaCl2溶液后的上层清液,再滴入少量Na2SO4溶液,若看到,证明SO42-已经除尽。
22.计算题(本题包括1小题,共6分)(写出简要的计算过程)
12g的碳单质在一定量的O2中充分反应,当碳完全反应后,气体通入足量的澄清石灰水中,剩余的气体的体积为11.2L(在标准状况下测定),则原来O2的物质的量为多少?
铜陵市一中2016-2017学年度第一学期
高一年级学段(期中)考试化学试卷
考试时间:90分钟满分:100分
一、选择题(每题3分,共48分,每题只有一个选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | ||||||||
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | 资*源%库 |
二、非选择题(共52分)
17.(8分) (1)(2)___________
(3)(4)_____
18.(10分)
$来&源:(3)
(4)__
(5)_______________
19.(10分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | B | A | D | D | D | B | C | D |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | B | D | B | C | A | D | C | D |
19.(10分)(1)12.5 (2)250 2.0
(3) 胶头滴管 (4)重新配置
20.(8分)(1)2:1 1:2 (2)1:2 14:17
21.(10分)(1)无气泡 (NH4)2CO3=2NH4++CO32-
(2)Na2CO3 稀盐酸 白色沉淀
22.(6分)(写出计算过程)
(1)解:由题意可知:
n(C)=1mol 11.2L气体为O2,则CO2为1mol,原氧气为1.5mol.
11.2L气体为CO,则CO2为0.5mol,CO也为0.5mol,原氧气为0.75mol.