
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016-2017学年海南中学第一学期期末考试
高一化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 K-39 S-32 Cl-35.5 Fe-56 Cu-64 Ag-108
第Ⅰ卷 选择题(共36分)
一、选择题:本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列叙述错误的是
A.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
B.过氧化钠可用于呼吸面具作为氧气的来源
C.氧化铁常用作红色油漆和涂料
D.合金的硬度一般比它的各成分金属的大,熔点一般比它的各成分金属的高
2.下列试剂能贮存在磨口玻璃塞的试剂瓶里的是
A.HF溶液 B.KOH溶液 C.盐酸 D.水玻璃
3.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2 L氧气所含的分子数为NA
B.1.8 g 的NH![]() 中含有的电子数为1.1NA
中含有的电子数为1.1NA
C.22g二氧化碳与标准状况下11.2LH2含有相同的原子数
D.2.3 g金属钠与O2完全反应,转移电子的物质的量为0.1mol
4.钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是
A.因为K的活泼性强,所以钾应该保存在煤油中
B.K在空气中点燃,产物只有K2O
C.K与水能够反应,但不如Na与水的反应剧烈,但产物都有氢气
D.K可以和CuSO4溶液发生置换反应,置换出Cu
5.为了延长小包装食品袋中食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是
A.无水硫酸铜、蔗糖B.硅胶、硫酸亚铁
![]() C.食盐、硫酸亚铁D.生石灰、食盐
C.食盐、硫酸亚铁D.生石灰、食盐
6.点燃的镁条能在氨气中剧烈燃烧,发生如下反应:Mg+2NH3=== Mg(NH2)2+H2 ,对该反应说法正确的是
A.NH3既是氧化剂又是还原剂 B.氢元素既被氧化又被还原
C.0.5mol氢气生成时转移1mol电子 D.镁具有氧化性
二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。
7.下列化学反应的离子方程式,书写不正确的是
B.向氯化铝溶液中加入过量氨水:Al3++4OH-=AlO![]() +2H2O
+2H2O
C.氯化亚铁溶液中通入少量氯气:Cl2+ 2Fe2+=2Fe3++2Cl-
D.往明矾溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:
2Ba2++2SO42-+Al3++4OH-==2BaSO4↓+AlO2-+2H2O
8.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+
D.该药剂不适合于胃溃疡患者服用
9.除去下列物质中的杂质(括号中为杂质)只选用给出试剂(不考虑操作),正确的是
A.Al2O3(Fe2O3)用盐酸
B.Al2O3(SiO2)用氢氧化钠溶液
C.NaHCO3溶液(Na2CO3)通入过量CO2
D.NaHCO3溶液(Na2SiO3)通入过量CO2
10.用下列装置不能达到有关实验目的的是
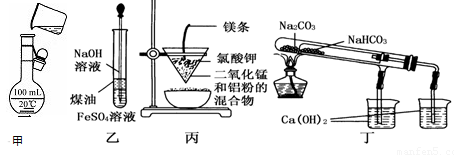
A.用甲图所示装置将溶液定容到100 mL
B.用乙图装置制备Fe(OH)2
C.用丙图装置可制得金属锰
D.用丁图装置验证NaHCO3和Na2CO3的热稳定性
11.某溶液中可能含有H+、Na+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是
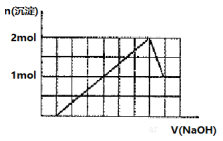
A.原溶液中含有的阳离子是H+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4
12.氢化亚铜(CuH)是一种难溶物质,具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+===Cu2++Cu。根据以上信息,下列叙述正确的是
A.用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作氧化剂
B.CuH在氯气中燃烧的化学反应方程式为2CuH+3Cl2![]() 2CuCl2+2HCl
2CuCl2+2HCl
C.CuH溶解在稀盐酸中生成的气体是氯气
D.如果选项C反应中生成了标准状况下22.4 L的气体,则转移电子3 mol
第II卷(共64分)
13.(8分)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
(1)工业上制造光导纤维的基本原料是。
(2)下列物质中,能用来制造耐火材料的是。(填字母)
A.铝B.氧化钠C.三氧化二铝
(3)在生铁和钢这2种金属材料中,含碳量较高的是。
(4)传统的无机非金属材料有_____________________(举出一种)。
14.(12分)A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
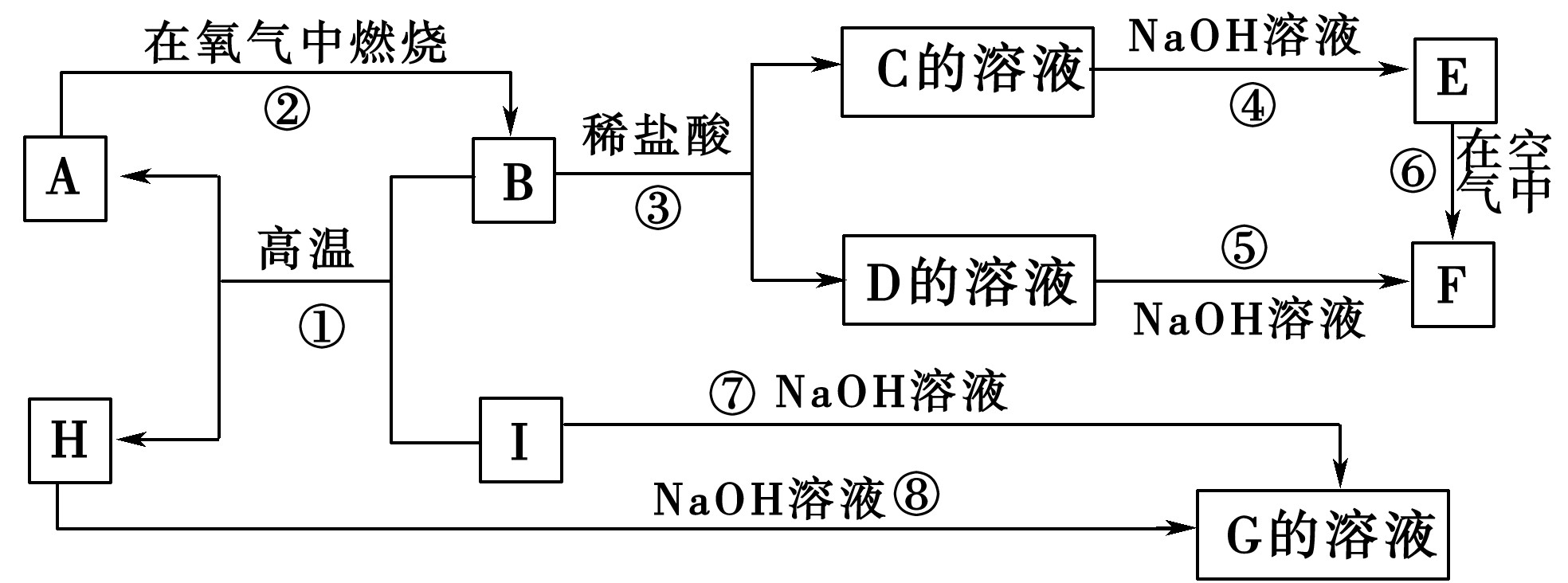
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应①的化学方程式为_____________________________________
反应的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______L。
15.(9分)某工厂用![]() 溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为:2
溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为:2![]() =
=![]() 。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
①取少量废液,滴加KSCN溶液显红色。
②取100mL废液,加入足量的![]() 溶液,析出沉淀43.05 g。
溶液,析出沉淀43.05 g。
③另取100mL废液,加入一定质量的铜片,充分反应后,测得铜片的质量减少了2.56g,再向反应后的溶液中滴加KSCN溶液不变色。
根据探究实验得出结论:
(1)废液中含有的金属离子是_______。
(2)100mL废液中Cl-的物质的量是___________________。
(3)原100mL废液中铜离子的物质的量浓度是_______。
16.(15分)Ⅰ.已知A、B、D为单质,其中B、D在常温常压下为气体。甲、乙、丙为常见化合物,甲、丙的焰色反应均为黄色,乙常温下为液体,有关转化关系如下图所示
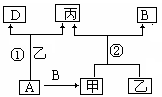
(1)写出有关物质的化学式A_____丙_____
(2)反应②的化学方程式为________________________。
(3)焰色反应主要需要的仪器和试剂为_____________________。
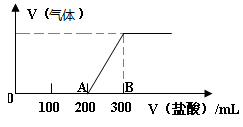
Ⅱ.向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示。
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | D | C | D | A | B | C | AB | D | CD | A | C | BD |
(2)Cu+H2O2+H2SO4==CuSO4+2H2O
(3)5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2++4H2O
(4)1.5
18.(12分)
SiO2 + 2C ![]() Si + 2CO↑
Si + 2CO↑
(1)b
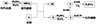
(2)防止加热条件下H2与空气混合爆炸;Mg与SiO2的反应是放热反应;
(3)Mg2Si+4HCl= 2MgCl2+SiH4↑ SiH4+2O2= SiO2↓+2H2O