
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
吉林省延边二中2015~2016学年度第二学期期中考试试卷
高一化学
考试说明:本试卷分第Ⅰ卷(选择题60分)和第Ⅱ卷(非选择题55分)两部分,试卷共8页,27小题。
可能用到的相对原子质量:C-12 H-1 O-16 N-14 Fe-56 Cl-35.5 Br-80
第Ⅰ卷 选择题
注意事项:
一、选择题(每题只有一个正确选项,每题3分,共60分)
1.下列各组中的性质比较,正确的是
①酸性:![]()
②碱性:![]()
③还原性:![]()
④稳定性:![]()
A.①②④ B.①②③ C.②③④ D.都正确
2、氢化钠(NaH)是一种离子化合物,其中钠元素是+1价,NaH跟水反应放出![]() ,下列叙述正确的是
,下列叙述正确的是
A.该反应中每生成1molH2转移2mol电子
B.NaH中的氢离子被还原成氢气
C.NaH跟水反应后溶液呈酸性
D.在NaH中的氢离子的电子层排布与氦原子相同
3.80年代,科学研制得一种新分子,它只由一种非金属元素碳组成,具有空心的类似足球状的结构,分子式为C60。下列说法正确的是
A. C60是只由同种元素碳组成的新型化合物
B. C60是由非金属元素碳组成的含有离子键的单质
C. C60是由同种非金属元素碳组成的含有共价键的单质
D. C60和金刚石互称为同位素
4.下列实验不能达到预期实验目的的是
| 序号 | 实验操作 | 实验目的 |
| A | 在浓硫酸和稀硫酸中分别加入Cu片,加热 | 比较稀、浓硫酸氧化性强弱 |
| B | F2、Cl2分别与H2反应 | 比较氟、氯的非金属性强弱 |
| C | 把CO2通入到水玻璃中 | 比较碳、硅的非金属性强弱 |
| D | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
5.化学与生活、社会发展息息相关,下列有关说法不正确的是
A.14C可用于文物的年代的鉴定,12C和14C互为同位素
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
D.在元素周期表的金属和非金属分界线附近寻找半导体材料
6.几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是
A.X、Y元素的金属性X
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.四种元素形成的单核离子半径由大到小的顺序为Z3->W2->X2+>Y3+
7.已知某元素的阳离子R2+的核内中子数为n,质量数为A,则m g它的氧化物中所含质子的物质的量是
A.![]() mol B.
mol B.![]() mol
mol
C.(A-n+2)mol D.(A-n+6)mol
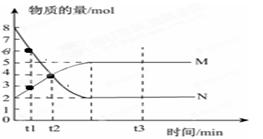
8.在2L的恒容容器中,充入1molN2气体和3molH2气体,并在一定条件下发生如下反应:N2(g) + 3H2(g)![]() 2NH3(g),若经3s后测得NH3的浓度为0.6mol•L-1,现有下列几种说法其中正确的是
2NH3(g),若经3s后测得NH3的浓度为0.6mol•L-1,现有下列几种说法其中正确的是
①用N2表示的反应速率为0.1mol•L-1•s-1
②用H2表示的反应速率为0.4mol•L-1•s-1
③3s时N2与 H2的转化率相等 ④3s时H2的浓度为0.6mol•L-1
A.①②④ B.①③④ C.②④ D.①②③④
9.下列关于化学键的说法正确的是
①离子化合物中可能同时含有离子键和共价键
②第IA族和第ⅦA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物
④活泼金属与非金属化合时,能形成离子键
⑤离子键就是阴、阳离子间的相互引力
⑥含有离子键的化合物一定是离子化合物
⑦含有金属元素的化合物一定是离子化合物
A.①④⑥ B.④⑥⑦ C.①③④ D.②③⑤
10.一定温度下,下列叙述是可逆反应N2(g)+3H2(g)![]() 2NH3(g),在定容密闭容器中达到平衡的标志的是
2NH3(g),在定容密闭容器中达到平衡的标志的是
①NH3的生成速率与NH3的分解速率相等;
②单位时间内amolN2生成,同时生成3a mol H2;
③N2的浓度不再变化; ④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦ N2、H2、NH3的分子数目比为1:3:2;
⑧混合气体的密度不再变化。
A.②⑤ B.②⑥⑦⑧ C.①③④⑤ D.①③④⑤⑧
11.为探究Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
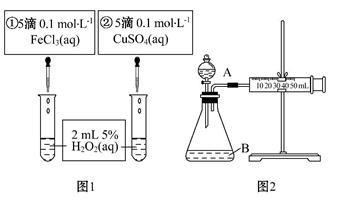
A.图1实验可通过观察产生气泡的快慢来比较反应速率的大小
B.若图1所示的实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置比较反应速率,可测定在相同状况下反应产生的气体体积及反应时间
D.为检查图2装置的气密性,可关闭分液漏斗A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否复原
12.某鱼雷采用Al-Ag2O动力电池,以溶解有氢氧化钾的流动海水为电解质溶液,电池反应为:2Al+3Ag2O+2KOH=6Ag+2KAlO2+H2O,下列说法不正确的是
A.Ag2O为电池的正极 B.Al在电池反应中被氧化
C.电子由Ag2O极经外电路流向Al极 D.溶液中的OH-向Al极迁移
13.短周期主族元素A、B、C、D、E的原子序数依次增大,A是原子半径最小的元素,B是地壳中含量最多的元素, A与C同主族,C、D两原子的电子数之和为A、B两原子的电子数之和的3倍。下列叙述正确的是
A.最高价氧化物对应的水化物酸性最强的是E
B.原子半径:A<B<C< D< E C.B与C形成的化合物中不可能含共价键
D.氢化物的热稳定性:D >E
14.下列各元素中,一定属于主族元素的是
A、X元素能形成+7价的含氧酸及其盐 B、Y元素原子最外层电子数为2
C、Z元素的阴离子与同一周期稀有气体元素的原子电子层结构相同
D、R元素的最高价氧化物是酸性氧化物
15.短周期元素W、X、Y、Z 的原子序数依次增大,W的单质是空气中体积分数最大的气体,W与Y最外层电子数之和为X最外层电子数的2倍,X、Y、Z简单离子的电子层结构相同,Z最外层电子数等于最内层电子数。下列说法正确的是
A.元素非金属性由强到弱的顺序:Y、X、W
B.W的简单气态氢化物比Y的简单气态氢化物稳定
C.原子半径由大到小的顺序:Z、Y、X、W
D.WX与ZX中的化学键类型相同
16.温度不变恒容的容器中0.1mol·L-1H2进行反应H2![]() 2H,若某段时间内H2浓度由0.06mol·L-1降到0.036mol·L-1所需的反应时间为12s ,则反应起始时H2浓度由0.1mol·L-1降到0.06mol·L-1需的时间为
2H,若某段时间内H2浓度由0.06mol·L-1降到0.036mol·L-1所需的反应时间为12s ,则反应起始时H2浓度由0.1mol·L-1降到0.06mol·L-1需的时间为
A.等于24sB.等于20sC.大于20sD.小于20s
17.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18。下列说法正确的是
A.阴离子的半径:Z>Y
B.元素W、X、Z各自最高和最低化合价的代数和分别为0、2、6
C.氧化物的水化物的酸性:Z>Y D.气态氢化物稳定性:Z>Y>X
18.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4===Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
19.短周期元素 A、B、C、D、E 的原子序数依次增大;A 的一种核素在考古时常用来鉴定一些文物的年代,B的氢化物的水溶液呈碱性;C、D 为金属元素,且 D 原子最外层电子数等于其 K 层电子数,而 C 的阳离子半径大于 D 的阳离子半径;若往 E 单质的水溶液中滴加少量紫色石蕊试液,能观察到先变红后褪色的现象。下列说法中正确的是
A.B的氢化物和E的氢化物能反应,且得到的产物只含有共价键
B.C在元素周期表中的位置是第三周期第ⅠA族
C.五种原子中E的原子半径最大
D.A的最低价氢化物分子中所有原子都满足8电子稳定结构
20.下列关于化学反应速率的说法中,正确的是
①用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②决定化学反应速率的主要因素是反应物的浓度.
③一定量的锌与过量的稀硫酸反应制取氢气,为减慢反应速率而又不影响生成H2的量,可向其中加入KNO3溶液。
④汽车尾气中的NO和CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
A.④⑤⑥ B.④⑥ C.①④⑥ D.③④⑥
第Ⅱ卷 非选择题
注意事项:
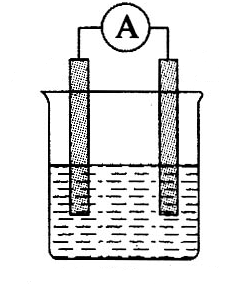
26.将CH3OH(甲醇)设计成燃料电池,其利用率更高,写出该燃料电池在酸性条件下的负极电极反应式:
27、一定条件下,NO2和SO2反应生成SO3(g)和NO两种气体,现将体积比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列不能说明反应达到平衡状态的是 。(填序号)
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3、NO的体积比保持不变
D.每消耗 1 mol SO2,同时生成1 mol NO
吉林省延边二中2015~2016学年度第二学期期中考试
高一化学参考答案及评分标准
一、选择题(单选题,共60分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | D | C | D | C | D | A | B | A | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | B | C | A | D | A | D | B | D | B | B |
二、非选择题(共55分)
21、(10分)(每空2分) (1)第四周期第IIA族 CaCl2
(2)S2-![]()
![]()
![]() (3)
(3)
22、(10分)(1)![]() NO
NO
![]() (2)3NO2 + H2O = 2HNO3 + NO
(2)3NO2 + H2O = 2HNO3 + NO
(3)N2H4–4e-+ 4OH- = N2 + 4H2O (每空2分)
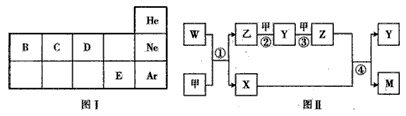
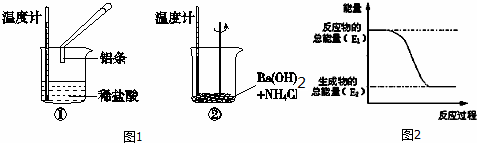
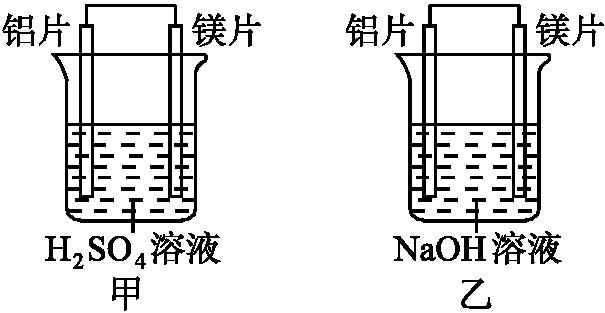
23、(10分)(1) 放热 吸热 ① ②
(2)Al+4OH--3e-![]() AlO2—+2H2O (每空2分)
AlO2—+2H2O (每空2分)
24、(10分)(1)2 (2) ![]() mol/( L·min)
mol/( L·min)
(3)a、b (4) C (5) ④>③>②>① (每空2分)

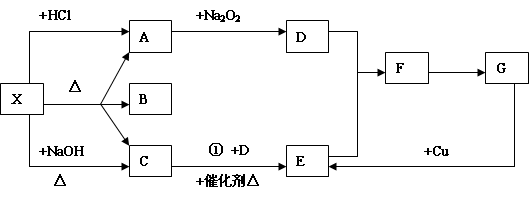
25、(1)NH4HCO3(2)
(3) 3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑
26、(3分))负极:2CH3OH-12e-+2H2O 2CO2+12H+ 27、(3分) ACD