
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016-2017学年海南中学第二学期期中考试
高一化学试题
可能用到的相对原子质量:Cu-64
第Ⅰ卷 选择题(共36分)
一、选择题:本题共6小题,每小题2分,共12分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.化学与资源、环境、生活关系密切, 下列说法错误的是
A.北京城区限制冬季燃煤供暖,是因为燃烧化石燃料会产生二氧化硫
B.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱溶液会“断路”
C.碘是人体必需的微量元素,所以要多吃富含高碘酸的食物
 D.活性炭与二氧化硫都可用于漂白,其漂白原理不同
D.活性炭与二氧化硫都可用于漂白,其漂白原理不同
2.京剧脸谱是中国戏曲特有的化妆艺术,具有很强的表现力和艺术价值。如图为窦尔敦京剧脸谱,若要将脸谱嘴唇部位涂成红色,则下列各组溶液中可达到该效果的是( )
A.氨水和石蕊溶液 B.碘水和淀粉溶液
C.CuCl2溶液和NaOH溶液 D.FeCl3溶液和KSCN溶液
3.下列表示物质结构的化学用语正确的是( )
A.含17个中子的镁元素的核素符号:Mg B.Na2O2的电子式:![]()
C.S2-离子的结构示意图: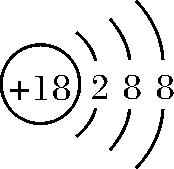 D.HF的电子式:H+[∶∶]-
D.HF的电子式:H+[∶∶]-
4.已知x、y、z元素的原子具有相同的电子层数,最高价氧化物对应水化物酸性依次增强,则下列判断正确的是( )
A.原子半径按x、y、z顺序增大
B.阴离子的还原性按x、y、z顺序增强
C.单质的氧化性按x、y、z顺序增强
D.氢化物的稳定性按x、y、z顺序减弱
5.下列反应中浓硫酸只表现强氧化性的是( )
A.2NH3+H2SO4(浓) = (NH4)2SO4
B.C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
C.Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.2FeO+4H2SO4(浓) = Fe2(SO4)3+SO2↑+4H2O
6.下列装置所示的实验中,能达到实验目的是( )
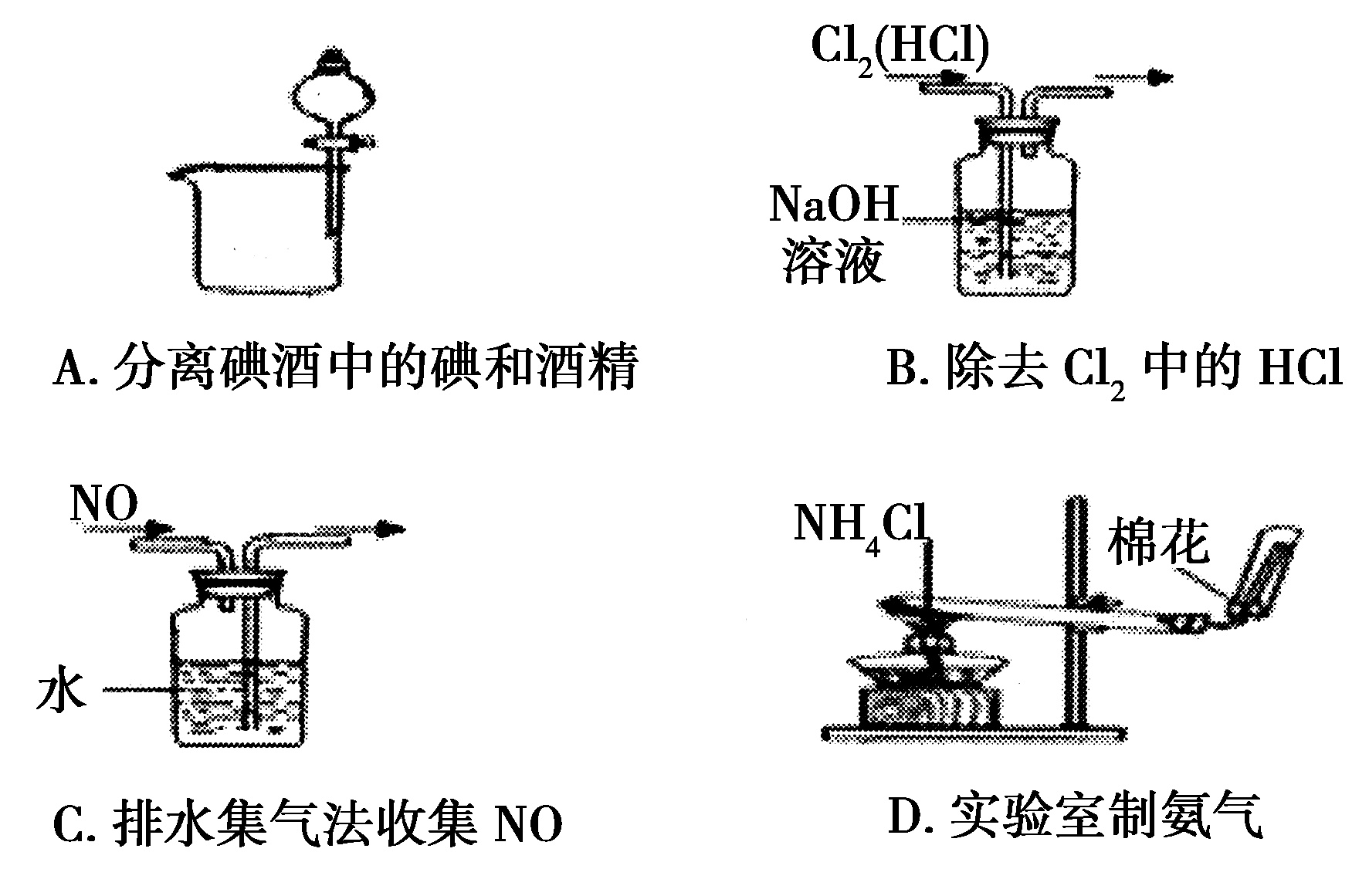
二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。
7.若R元素无同位素,R原子的质量数为A,Rm-的核外电子数为x,则Wg Rm-所含中子的物质的量为( )
A.(A-x+m) mol B.(A-x-m) mol
C.![]() (A-x-m) mol D.
(A-x-m) mol D.![]() (A-x+m) mol
(A-x+m) mol
8.解释下列事实的离子方程式或化学方程式不正确的是
A.向澄清石灰水中加入过量的碳酸氢钠溶液有白色沉淀生成:
Ca2++OH-+HCO3-=CaCO3↓+H2O
B..铜与浓硫酸受热产生无色气体: Cu+2H+ = Cu2++ H2↑
C.不宜用无色试剂瓶保存氯水:2HClO![]() 2HCl +O2↑
2HCl +O2↑
D.保存烧碱溶液的试剂瓶不能用玻璃塞:SiO2+2OH- = SiO32-+H2O
9.将含有等体积NH3、CO2、NO的混合气体依次通过盛有足量浓硫酸、Na2O2和NaHCO3溶液的装置,充分作用后,最后得到的气体是( )
A.CO2和NO B.CO2C.NO D.NO2
10.将3.2 g Cu与30.0 mL10 mol/L HNO3充分反应,测得还原产物为NO和NO2混合物,转换为标准状况下的体积是a L。如反应的溶液中有b mol H+,则此溶液中含NO的物质的量是( )
A.0.5 b mol B.0.1 mol
C.(0.3-![]() )molD.(0.1+b) mol
)molD.(0.1+b) mol
11.没有做实验而欺骗老师的学生是( )
A.老师,我用Na2SO3与BaCl2溶液作用,有白色沉淀生成,加入盐酸后沉淀消失
B.老师,我向NaAlO2溶液溶液中通入CO2气体,有白色沉淀生成
C.老师,我向BaCl2溶液中通入SO2气体,也有白色沉淀生成
D.老师,我向用硝酸酸化的BaCl2溶液中通入SO2气体,我以为不会有沉淀,可出现了白色沉淀
12.已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W和Z、X和Y分别同主族,Y、Z同周期。Z能与X形成两种常见的离子化合物,离子个数比均为2:1。下列说法错误的是( )
A.Z、Y、X、W的原子序数依次减小
B.W与X可形成既含极性共价键又含非极性共价键的化合物
C. Z的最高价氧化物对应的水化物是短周期元素形成的最强碱
D.X的简单氢化物的沸点低于Y的简单氢化物的沸点
第II卷(共64分)
13、(8分) B、C、D、E、F为由六种短周期元素构成的粒子,它们都有10个电子,其结构特点如下表:
| 粒子代号 | B | C | D | E | F |
| 原子核数 | 单核 | 双核 | 多核 | 单核 | 多核 |
| 电荷数 | 1+ | 1- | 0 | 2+ | 1+ |
其中,B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C常用于F 的检验(加热)。请填写下列空白:
(1)E位于元素周期表第 周期第 族。
(2)比较BC和EC2的碱性强弱BC EC2(填< 、> 、= )。
(3)写出D的电子式$来&源:
(4)用C检验F加热时反应的离子方程式
14.(6分)矿泉水一般是由岩石风化后被地下水溶解其中可溶部分生成的,此处所指的风化作用是指矿物与水和CO2同时作用的过程.例如长石(KAlSi3O8)风化生成黏土[Al2(Si2O5)(OH)4],此时反应的离子方程式为:
2KAlSi3O8+2H2CO3+5H2O===2K++2HCO+4H2SiO3+Al2(Si2O5)(OH)4
(1)将复杂硅酸盐改写成氧化物形式:
KAlSi3O8:__________________________________________;
(2)上述反应能够发生的原因是:________________________________
(3)1mol Al2(Si2O5)(OH)4与足量盐酸完全反应,盐酸中至少需含 mol HCl。
15.(11分)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
M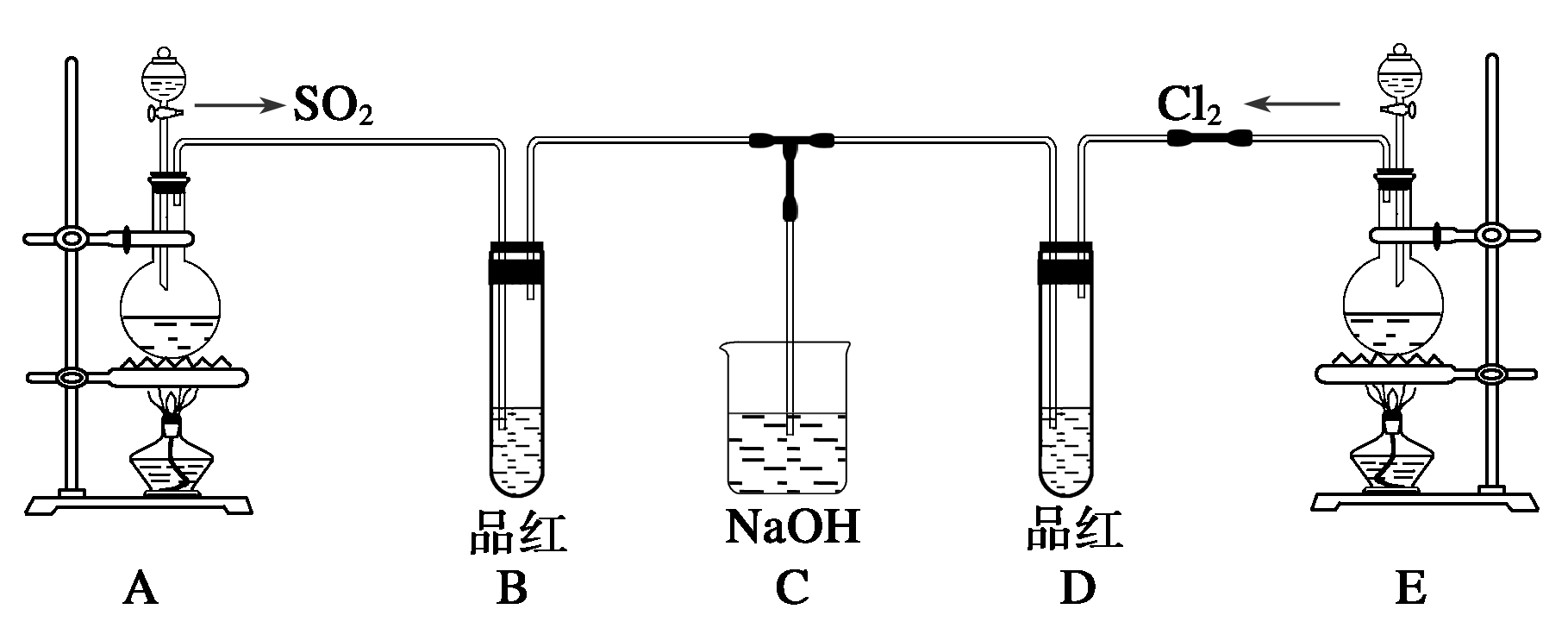
(1)M装置的名称
(2)实验室用装置E制备Cl2,其反应的化学方程式为: 。
若有6 mol 的HCl参加反应,则转移的电子总数为 mol;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B ,D: 。
②停止通气后,再给B、D两个试管分别加热;B、D两试管的现象分别为:
B______________,D: 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)
。
16.(12分)现有部分元素的性质与原子(或分子)结构如下表所示:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
(1)画出元素T的原子结构示意图:________________。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填字母)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质与水反应剧烈
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中的两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式:______________________。
(4)T可以形成稳定的阴离子Tm-,Y可以形成稳定的阳离子Yn+,其半径关系为r(Tm-) r(Yn+)(填“>”,“<”或“=”)
(5)X、Y、Z的最高价氧化物对应的水化物可以相互发生反应,写出Y、Z的最高价氧化物对应的水化物之间反应的离子方程式 。
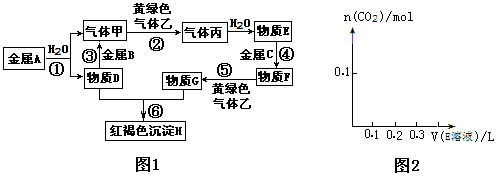 17.(10分)中学化学常见物质间的转化如下图。其中A、B、C是金属单质,A的一种化合物具有强氧化性,可用作呼吸面具和潜水艇的供氧剂。回答下列问题:
17.(10分)中学化学常见物质间的转化如下图。其中A、B、C是金属单质,A的一种化合物具有强氧化性,可用作呼吸面具和潜水艇的供氧剂。回答下列问题:
(1)检验D中所含阳离子的实验方法是________________
(2)物质F的溶液中加入D的溶液观察到的现象是
(3)常温下,金属C中加入浓硫酸产生 现象
(4)物质F的溶液中加入硝酸溶液,反应的离子方程式为
(5)将红褐色沉淀H加热后得到的一种氧化物。该氧化物与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾).同时还生成KNO2和H2O 。该反应的化学方程式是
18.(17分)依据下图中氮元素及其化合物的转化关系,回答问题:
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为 。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。(请在答题卷的相应位置画出连接图)
(3)下列试剂不能用于干燥NH3的是 。
(4)以NH3、空气、水为原料制取硝酸分为三步:
① NH3→NO化学方程式为 。
② NO→NO2实验现象是 。
③ NO2 H2O →
(5)图1中,X的化学式为 ,从物质性质上看,X属于 氧化物(填“酸性”,“碱性”或“两性” )。将X转化为HNO3属于 反应(填“氧化还原”或“ 非氧化还原”)。
(6)若要将NH3→N2,从原理上看,下列试剂可行的是 。
A.O2B.NaC.NH4ClD.NO2
2016-2017学年海南中学第二学期期中考试高一化学答案
第Ⅰ卷 选择题(共36分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| C | D | B | C | B | C | D | AB | A | CD | C | AD |
13、(8分)(1)3 , ⅡA ; (每空1分) (2 ) > (2分)
(3)![]() (2分) (4)NH4++OH—
(2分) (4)NH4++OH—![]() NH3↑+H2O (2分)
NH3↑+H2O (2分)
14.(6分)(1)K2O·Al2O3·6SiO2
(2)H2CO3的酸性比H2SiO3的酸性强,由较强的酸可制得较弱的酸
(3)6 (每空2分)
15 (11分) (1)圆底烧瓶 (1分)
加热
MnO2+4HCl(浓) === MnCl2+Cl2↑ +2H2O (2分) 3 (2分)
(3)①品红溶液褪色 品红溶液褪色
②褪色的品红溶液又恢复成红色 无明显现象 (每空1分)
(4)Cl2+SO2+2H2O===2HCl+H2SO4(2分)
16.(12分)(1) O ![]() (2分) (2) Na(2分) cd(2分) (3) Na2O2(2分)
(2分) (2) Na(2分) cd(2分) (3) Na2O2(2分)
(4) > (2分) (5)Al(OH)3+OH-=AlO-+2H2O(2分)
17(10分)(每空2分)
(1)进行焰色反应 (2)得到白色沉淀迅速变灰绿色,最终变成红褐色(3)钝化
(4)3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
(5)Fe2O3+3KNO3+4KOH![]() 2K2FeO4+3KNO2+2H2O
2K2FeO4+3KNO2+2H2O
18. (17分)(1)2NH4Cl + Ca(OH)2![]() CaCl2+ 2H2O + 2NH3↑ (2分)
CaCl2+ 2H2O + 2NH3↑ (2分)
(2)如右图 导管短进长出 (2分)
(3)A D (2分)
(4)4NH3 + 5O2![]() 4NO + 6H2O 无色气体变为红棕色
4NO + 6H2O 无色气体变为红棕色
通足量O2(每空2分)
(5)N2O5 酸性 非氧化还原 (每空1分) (6)A D (2分)