
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
海南国科园实验学校2015-2016学年度第一学期
高一年级化学科期中考试试卷
满分:100 时间:90分钟 命题人:黄登高
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Mg-24 Cu-64 Ba-137
一.选择题(本题包括6个小题,每小题只有一个正确选项,各2分,共12分)
1.下列说法正确的是
A.氧气的摩尔质量是32 B.CO32-摩尔质量是60g/mol
C.CO2的相对分子质量是44gD.硫酸的摩尔质量是98g
2.下列溶液中Cl﹣浓度最小的是
A.200mL 2mol/L MgCl2溶液B.1000mL 2.5mol/L NaCl溶液
C.300mL 5mol/L KCl溶液 D.250mL 1mol/L AlCl3溶液
3.容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度 ②浓度 ③容量 ④压强⑤刻度线 ⑥酸式或碱式 这六项中的哪几项
A.②④⑥B.③⑤⑥C.①②④D.①③⑤
4.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为
A 蒸馏水 氨水 氧化铝 二氧化硫
B 盐酸 空气 硫酸 干冰
C 胆矾 盐酸 铁 碳酸钙
D 生石灰 硫酸 氯化铜 碳酸钠
5.下列有关胶体的叙述正确的是
A. 胶体粒子的大小通常在0.1~1nm之间
B. 阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现
C. 可以通过过滤分离溶液和胶体
D. 向FeCl3溶液中加入NaOH溶液,会出现红褐色Fe(OH)3胶体
6.下列电离方程式中,不正确的是
A.H2SO4 = 2H++SO42- B.Ba(OH)2 = Ba2++2OH-
C.NaNO3 = Na++NO3- D.KClO3 = K++Cl-+3O2-
二、不定项选择题(本题包括6小题,每小题4分,共计24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分:若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题就得0分)
7.能用H++OH﹣=H2O来表示的化学反应是
A.氢氧化镁和稀盐酸反应B.Ba(OH)2溶液滴入稀硫酸中
C.烧碱溶液和稀盐酸反应D.二氧化碳通入澄清石灰水中
8.质量都为4. 2 g的A气体和B气体,在标准状况下的体积分别为2.94 L和3.36 L,则这两种气体的摩尔质量之比为
A.1∶1B.15∶13C.7∶8D.8∶7
9.下列反应的离子方程式正确的是
A.澄清的石灰水跟稀硝酸反应: Ca(OH)2+2H+= Ca2++2H2O
B.氢氧化钡溶液和硫酸铜溶液反应: Ba2++ SO42-= BaSO4↓
C.用小苏打治疗胃酸过多:HCO3-+H+ = CO2↑+H2O
D.往澄清石灰水中通入过量二氧化碳气体: CO2+OH-= HCO3-
10.在酸性无色溶液中,下列各组离子一定能大量共存的是
A. MnO4﹣、H+、K+、NO3﹣ B. Na+、H+、Cl﹣、NO3﹣
C. Ba2+、H+、SO42﹣、Cl﹣ D. H+、Fe3+、SO42﹣、Cl﹣
11..用NA表示阿伏加德罗常数,下列叙述不正确的是
A.64 g SO2中含有的氧原子数为2NA
B.物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数目为1NA
C.常温常压下,14 g 氮气所含分子数为0.5 NA
D.标准状况下,22.4 L 水所含水分子数为1NA
12.把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.(b-a)/V mol·L-1B.(2b-a)/V mol·L-1
C.2(b-a)/V mol·L-1D.2(2b-a)/V mol·L-1
三、填空题
13.(12分)(1)49gH2SO4的物质的量为________,所含氧原子的质量为 ______;
(2)同温同压下,同体积的A气体和H2的质量分别是4.8g和0.2 g,则气体A的摩尔质量为_____,A与氢气的物质的量之比为______。
(3)有二氧化碳与一氧化碳的混合气体共10.8 g,其物质的量为0.3 mol。则混合气体中二氧化碳的物质的量为_____,一氧化碳的质量分数为_________。
14.(7分) 下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:
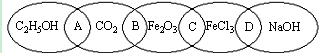
15.(11分) 按要求完成化学用语
I. (8分)写出下列反应的离子方程式:
(1)石灰石与稀硝酸反应: ;
(2)氢氧化钡溶液与硫酸氢钠溶液反应至中性:_____;
(3)锌与硫酸铜溶液反应: ;(4)氧化铜溶于稀盐酸: 。
II.(3分)将下列离子方程式改写成相对应的化学方程式:
(1)CO32—+2H+ = CO2↑+H2O: ; (2)Mg2++2OH— = Mg(OH)2↓: ;
(3)3Hg2++2Al = 3Hg+2Al3+: 。
四、实验题
16.(14分)用10mol/L的浓H2SO4配制250ml0.5mol/L的稀H2SO4,请按要求填空:
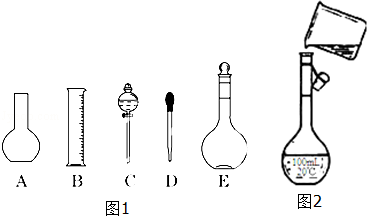
(1)所需浓H2SO4的体积为_____mL;如果实验室有10mL、20mL、50mL量筒,应选用______mL量筒.
(2)如图1所示的仪器中配制该溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是__________;
(3)如图2是配制过程中转移溶液的示意图,图中有两处错误,分别是:①______,②_____
(4)配制过程中,下列操作会导致所配稀硫酸浓度偏小的是____
A.所用过的烧杯、玻璃棒未洗涤
B.定容时俯视容量瓶刻度线
C.摇匀后静置,发现液面低于刻度线,继续滴加蒸馏水至刻度线
D.容量瓶用蒸馏水洗涤后残留有少量的水
(5)在250mL 0.5mol/LH2SO4溶液取出5mL该溶液,它的H+物质的量浓度为______mol/L.
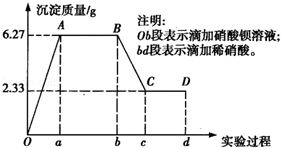
17.(12分)某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl﹣中的若干种离子.该小组同学取100mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加2mol/L的硝酸,实验过程中沉淀质量的变化情况如下图所示:
(1)水样中一定含有的阴离子是 ,其物质的量浓度之比为 .
(2)写出BC段所表示反应的离子方程式: .
(3)由B到C点变化过程中消耗硝酸的体积为 .
(4)试根据实验结果推测K+是否存在? (填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是 .(若K+不存在,则不必回答该问).
五、计算题
18.(8分)
(1)在标准状况下16克气体X的体积为5.6L,则此气体的摩尔质量为多少
(2)常温下,在78g水中溶解32g CuSO4,恰好达到饱和,该溶液密度为1.2g/cm3,求:
①该溶液溶质质量分数
②该溶液中CuSO4的物质的量浓度
③取出20.0ml该溶液,配成浓度为0.50mol/L的稀溶液,则稀释后溶液的体积是
海南国科园实验学校2015-2016学年度第一学期
高一年级化学科期中考试答题卷
| 题号 | 选择题 | 13 | 14 | 15 | 16 | 17 | 18 | 总分 |
| 得分 |
选择题答案栏(其中1-6题各2分,7-12题各4分,共36分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 |
三、填空题
13题(每空2分,共12分) (1)___________, ___________;(2)____________, _____________; (3)_____________, _______________。 14题(每空1分,共7分) _____________ ______________;(2)__________________; (3)_________________________________________________; (4)______________ ________________.(5)_______________。
15题I:(每小题2分,共8分)
(1)________________________________________________,
(2)__________________________________________________,
(3)__________________________________________________,
(4)__________________________________________________.
II(每空1分,共3分)
(1)_________________________________________________;
(2)_________________________________________________;
(3)_________________________________________________.
16题(第1小题每空1分,其余每空2分,共14分)
(1)_______;____mL量筒.(2)___________________
(3)①_______________________,②______________________;
(4)_________(5)________mol/L.
17题(每空2分,共12分)
(1) _______________, __________;
(2) ____________________________________;
(3) .(4) ____, __________.
18题(每空2分,共8分)
(1) (2)① ② ③
海南国科园实验学校2015-2016学年度第一学期
高一年级化学科期中试卷参考答案
一:1B,2B,3D,4A,5B,6D;
二:7C,8D,9CD,10B,11BD,12D
三:13(1)0.5mol,32克; (2)48 g/mol,1:1; (3)0.15mol,38.9%
14(1)CD ;B (2)a、c (3)Fe2O3 + 6H+ = 2Fe3++3H2O
(4)D 复分解 (5)胶体
15,I,(1)CaCO3+2H+=Ca2++H2O+CO2↑(2)Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
(3)Zn+Cu2+=Zn2++Cu (4)CuO+2H+=Cu2++H2O
II,符合题意即可得分
16: (1) 12.5, 20.(2)AC 烧杯,玻璃棒
(3):①容量瓶的规格选错,②未用玻璃棒引流.
(4)AC (5)1mol/L.
17(1)SO42﹣,CO32﹣ ; 1:2 .
(2): BaCO3+2H+=Ba2++CO2↑+H2O .
(3) 20ml .(4) 是 ≥0.6mol/L .
18:(1) 64 g/mol, (2) 29.1%; 2.17 mol/L; 86.8ml