
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
市一中2015-2016学年度第二学期期末考试
高一化学试题
命题人:刘宇蓉
可能用到的相对原子质量:H:1 C:12 0:16 N:14 CI:35.5
一.选择题(每小题只有一个选项符合题意,每小题2分;共52分)
来源:1.许多国家十分重视海水资源的综合利用,不需发生化学变化就能从海水中获得的物质是( )
A.氯、溴、碘 B.钠、镁、铝
C.食盐、淡水 D.烧碱、氢气
2.石材的放射性常用镭( Ra)作为标准,居里夫人(Marie Curie)因对Ra元素的研究曾两度获得诺贝尔奖。下列有关镭( Ra)的叙述中不正确的是 ( )
A. Ra原子核内有138个中子 B. Ra原子核外有88个电子
C. Ra原子核内有88个质子 D.Ra元素位于第六周期
3.石油裂化的目的是( )
A.除去石油中的杂质 B. 提高石油的年产量
C. 使直连烃转化为芳香烃 D. 提高汽油的产量和质量
4. NaCl是从海水中提取出来的一种重要物质,除食用外,它还是一种工业原料,下列以NaCl为原料的产品(或物质)是 ( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
A.全部B.①②③④
C.①②③⑤D.①②④⑤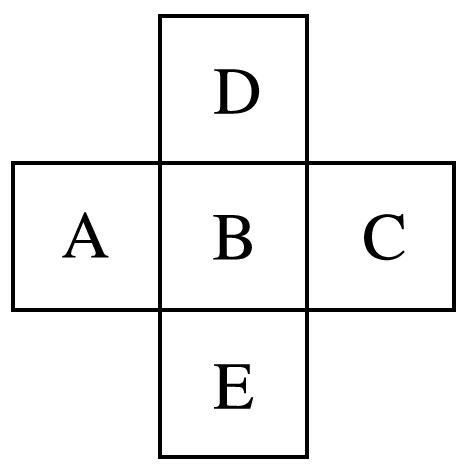
5. 如图为元素周期表中前四周期的一部分,若B元素的核电荷数为x,则这五种元素的核电荷数之和为 ( )
A.5x+10 B.5xC.5x+14D.5x+16
6. 四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的个数比为1:1的离子化合物,其水溶液呈中性。下列说法正确的是 ( )
A.简单离子半径:W
C.气态氢化物的热稳定性:W
7. 不能作为判断硫、氯两种元素非金属性强弱的依据是( )
2345667888 A.单质氧化性的强弱 B.单质与氢气化合的难易
C.单质沸点的高低 D.最高价氧化物对应的水化物酸性的强弱
8.设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 molN2与4 molH2反应生成的NH3分子数为2NA
C.铜-锌(稀硫酸)原电池,每转移数2NA电子则正极消耗1 mol铜
D.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
9.新浪科技网报道:美科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可能是人类最伟大的发现之一,有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
来源:A.共价键 B.离子键 C.一种静电引力 D.一种静电斥力
10. 下列化学用语正确的是( )
![]() A.H2O2的电子式: B.次氯酸的结构式:H—O—Cl
A.H2O2的电子式: B.次氯酸的结构式:H—O—Cl
C.中子数为10的氧原子:![]()
![]() D.乙酸乙酯的结构简式:C4H8O2
D.乙酸乙酯的结构简式:C4H8O2
11. 氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是( )
A.Q1+Q2>Q3B.Q1+Q2<2Q3
C.Q1+Q2<Q3D.Q1+Q2>2Q3
12.X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X、Y和稀硫酸组成原电池时,X电极上有气泡生成。X、Y、Z三种金属的活动性顺序为( )
A.X>Y>ZB.X>Z>YC.Y>X>ZD.Y>Z>X
13.研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是 ( )
A.正极反应式:Ag+Cl--e-=AgCl B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动 D.AgCl是还原产物
14.下列食品添加剂中,其试用目的与反应速率有关的是
A.抗氧化剂B.调味剂C.着色剂D.增稠剂
15. C、CO、CH4、C2H5OH是常用的燃料,它们每1 mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5 kJ、283.0 kJ、890.3 kJ、1 366.8 kJ。相同质量的这4种燃料,完全燃烧时放出热量最多的是 ( )
A、C B、CO C、CH4D、C2H5OH
16. 某气态烷烃20 mL,完全燃烧时,正好消耗同温同压下的氧气100 mL,该烃的化学式是( )
A.C2H6 B.C3H8 C.C4H10 D.C5H12
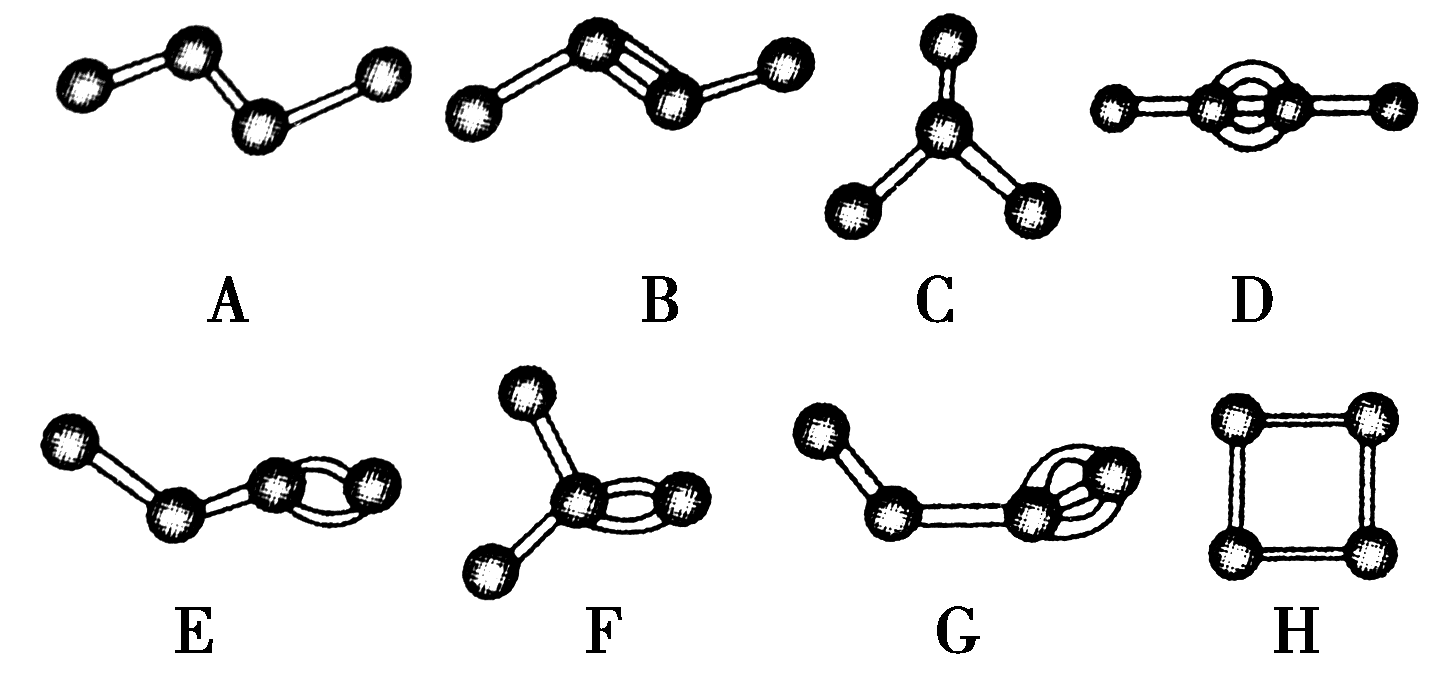 17.如下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合,则下列说法正确的是 ( )
17.如下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合,则下列说法正确的是 ( )
A.图中属于烷烃的是A、C、H B.图中C和F分子中氢原子数相同
C.图中物质碳元素的质量分数最大的是C
D.图中与B互为同分异构体的有E、F、H
18.下列反应中,光照对反应几乎没有影响的是( )
 A.只有①③ B.只有①②③
A.只有①③ B.只有①②③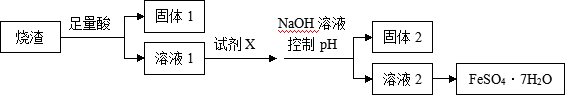
| 对二甲苯 | 邻二甲苯 | 间二甲苯 | 苯 | |
| 沸点/℃ | 138 | 144 | 139 | 80 |
| 熔点/℃ | 13 | 25 | 47 | 6 |
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(4)已知碳元素形成的物质种类最多,某烷烃A在同温同压下蒸气的密度是H2的36倍,A的分子式为______。烷烃B的分子中含有200个氢原子,B的分子式为__________。
(5)碳与镁形成的1mol化合物Mg2C3与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的分子式为__________ 其与水反应的化学方程式为__________。
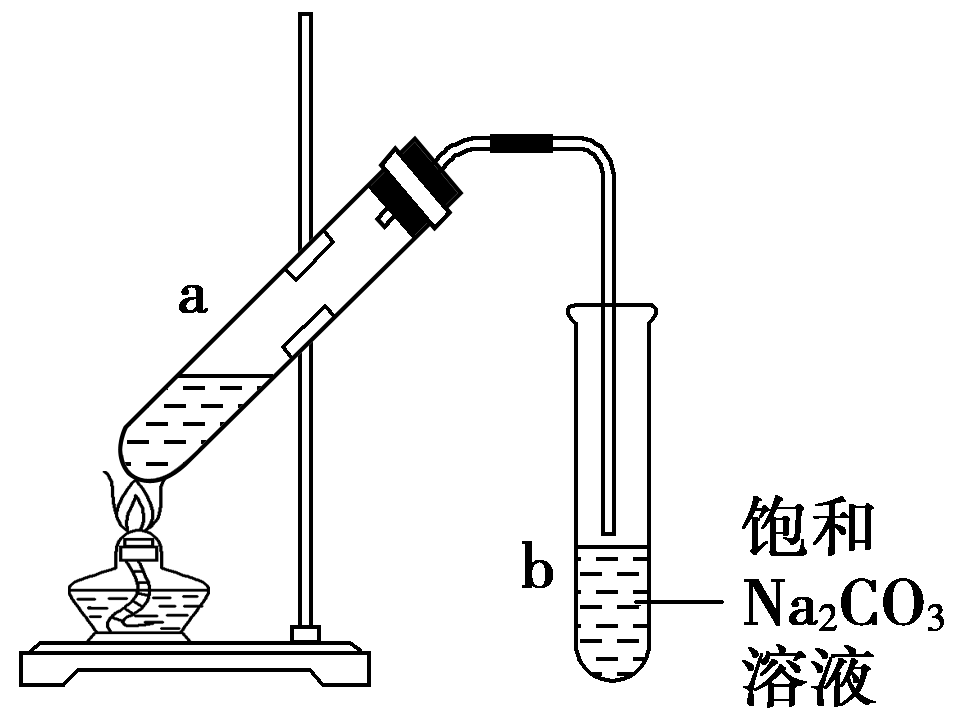
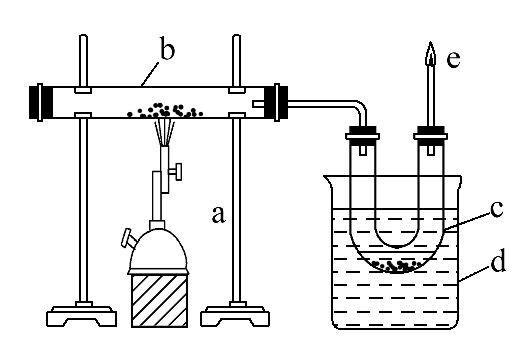 28.(14分)右图是实验室干馏煤的装置图,回答下列问题:
28.(14分)右图是实验室干馏煤的装置图,回答下列问题:
(1)图中仪器c的名称: , 仪器d的作用是 。
(2)c中液体有水层和有机层,其中水层里溶有 ,可用 检验出来。有机物可以通过 的方法使其中的重要成分分离出来。
(3)e处点燃的气体主要成分有 ,
火焰的颜色 。
29.(12分) 海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
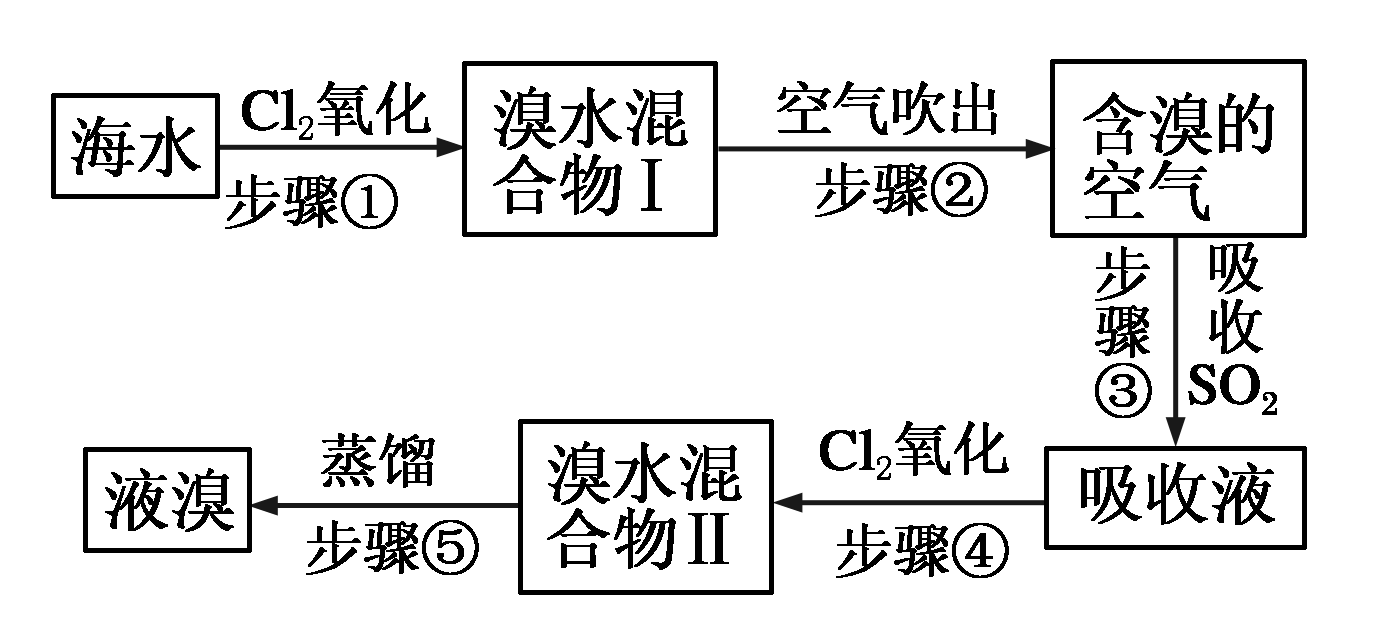 (1) 步骤①反应的离子方程式是____________。
(1) 步骤①反应的离子方程式是____________。
(2) 步骤③反应的化学方程式是___________,
(3)从理论上考虑,下列也能吸收Br2的是________。
A.NaOH B.FeCl2C.Na2SO3D.H2O
(4) 溴的原子序数为______________
(5)步骤⑤蒸馏的过程中,温度应控制在80℃~90℃。温度过高或过低都不利于生产,请解释原因____________________________
(6)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏而得到液溴?____________________________________。
30.(共8分)
373k时把0.125molN2O4气体通入体积500ml的真空容器中,发生N2O4(g) ![]() 2NO2(g) 反应,容器中立即出现红棕色。反应进行到2 s 时,NO2的含量为0.01 mol。进行到60 s 时达到平衡,此容器内混合气体的密度是氢气密度的28.75倍,则
2NO2(g) 反应,容器中立即出现红棕色。反应进行到2 s 时,NO2的含量为0.01 mol。进行到60 s 时达到平衡,此容器内混合气体的密度是氢气密度的28.75倍,则
(1)开始2 s内以N2O4表示的化学反应速率为多少?(g)
(2)达到平衡时,体系的压强为开始的多少倍?
(3)达到平衡时,体系中N2O4的物质的量为多少?
(4)N2O4的平衡转化率为多少?
西安市第一中学
2015-2016学年度第二学期期末考试
高一化学试题答案
命题人:刘宇蓉
可能用到的相对原子质量:C:12 0:16 N:14 CI:35.5
一.选择题(每小题只有一个选项符合题意,每小题2分;共52分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | C | D | D | A | A | B | C | A | A | B | D | C | B |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 |
| 答案 | A | C | B | D | C | B | D | A | D | B | C | C | A |
非选择题(共50分)
27.(共14分)(1)第三周期 第ⅦA族 (2)Si (3)ac
(4)C5H12 C99H200
(5)C3H4 Mg2C3 + 4H2O ==2Mg(OH)2 + C3H4
28.(共14分)(1)U形管 盛装冷水对蒸气进行冷却
(2) 粗氨水 酚酞溶液 蒸馏
(3)H2、CH4、CH2=CH2、CO 淡蓝色
29.(共12分)(1)2Br-+Cl2===Br2+2Cl- (2)SO2+Br2+2H2O===H2SO4+2HBr
(3)ABC (4) 35
(5)若温度过高,大量水蒸气随溴排出,溴气中水蒸气的含量增加,温度过低,溴不能完全蒸出,产率太低
(6)“溴水混合物Ⅰ”中虽然有溴单质,但浓度低,如果直接蒸馏,处理量大,生产成本高,而“溴水混合物Ⅱ”实际上将溴水浓缩了
30.(共8分)