
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
海南省国科园实验学校2015—2016学年度第一学期
高二年级化学期中考试试卷
(总分:100分 时间90分钟)
第Ⅰ卷(共36分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 S 32 Cu 64 Fe 56
一、选择题(本题共6小题,每小题2分共12分。只有一项是符合题目要求的)
1、下列说法不正确的是 ( )
A、放热反应不需加热即可发生
B、化学反应过程中的能量变化除了热能外,也可以是光能、电能等
C、需要加热才能进行的化学反应不一定是吸热反应
D、反应物的总能量大于生成物的总能量为放热反应
2、在四个不同的容器中,在不同的条件下进行合成氨反应N2(g)+ 3 H2(g)![]() 2NH3(g)。根据在相同时间内测定的结果判断,生成氨的速率最快的是 ( )
2NH3(g)。根据在相同时间内测定的结果判断,生成氨的速率最快的是 ( )
A、υ(H2)=0.1 mol·L-1·min-1B、υ(N2)=0.2 mol·L-1·min-1
C、υ(NH3)=0.15 mol·L-1·min-1D、υ(H2)=0.3 mol·L-1·min-1
3、在25℃和1. 01×105Pa时,2N2O5(g) = 4NO2(g) + O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是 ( )
A.是吸热反应 B.是放热反应 C.是熵减反应 D.是熵增效应大于能量效应
4、某温度下,反应H2(g)+I2(g)![]() 2HI(g);△H>0。在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是 ( )
2HI(g);△H>0。在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是 ( )
A、恒温,压缩体积,平衡不移动,混合气体颜色加深
B、恒压,充入HI(g),开始时正反应速率减小
C、恒容,升高温度,正反应速率减小
D、恒容,充入H2,I2(g)的体积分数降低
5、可逆反应:2NO2(g)![]() 2NO(g) + O2(g)在一固定容积的密闭容器中反应,达到平衡状态的标志是 ( )
2NO(g) + O2(g)在一固定容积的密闭容器中反应,达到平衡状态的标志是 ( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时,生成2n mol NO
③用NO2、NO、O2物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A、①④⑥ B、②③⑤ C、①③④D、①②③④⑤⑥
6、H2与O2发生反应的过程用模型图示如下(“﹣”表示化学键):下列说法不正确的是( )
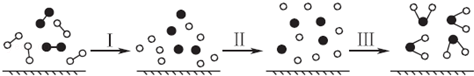
| A. | 过程Ⅰ是吸热过程 | |
| B. | 过程Ⅲ一定是放热过程 | |
| C. | 该反应过程所有旧化学键都断裂,且形成了新化学键 | |
| D. | 该反应的能量转化形式只能以热能的形式进行 |
二、选择题(本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意)
7、已知:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ•mol﹣1
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1 452kJ•mol﹣1
H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1下列说法正确的是( )
| A. | H2(g)的燃烧热为285.8 kJ•mol﹣1 | |
| B. | ||
| C. | 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | |
| D. | 3H2(g)+CO2(g)═CH3OH(l)+H2O(l)△H=+131.4 kJ•mol﹣1 |
8、常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两个实验:(已知N2O4![]() 2NO2 △H > 0)
2NO2 △H > 0)
(a)将两容器置于沸水中加热(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是 ( )
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
9、有一化学平衡:mA(g)+nB(g)![]() pC(g)+qD(g)右图表示的是
pC(g)+qD(g)右图表示的是
转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )
A、正反应吸热:m+n>p+q B、正反应放热:m+n
C、正反应放热:m+n>p+q D、正反应吸热:m+n
10、反应2A(g)![]() 2B(g) + E(g)(△H>0)达到平衡时,
2B(g) + E(g)(△H>0)达到平衡时,
要使正反应速率降低,A的浓度增大,应采取的措施是 ( )
A、加压 B、降温
C、减少E的浓度 D、减压
11、白磷在氧气中燃烧放热,反应为:P4+ 5O2== P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol—1、P—O b kJ·mol—1、P=O c kJ·mol—1、O=O d kJ·mol—1。
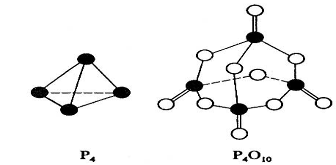
根据图示的分子结构和有关数据下列推断正确的是 ( )
A.6a+5d< 4c + 10b B.△H = (4c+12b-6a-5d) kJ·mol—1
C.6a+5d< 4c + 12b D.△H = (6a+5d-4c-12b) kJ·mol—1
12、已知298K时下述反应的有关数据:
C(s) + 1/2 O2(g) == CO(g) △H1 = -110.5kJ·mol-1
C(s) + O2 (g) == CO2(g), △H2= -393.5kJ/mol
则 C(s)+CO2(g)=2CO(g) 的△H为 ( )
A、+283. kJ·mol-1 B、+172.5 kJ·mol-1
C、-172.5 kJ·mol-1l D、-504 kJ·mol-1
第Ⅱ卷(非选择题,共64分)
13、(12分)(1) 固态硫加热形成气态硫要吸收能量:1mol固态硫燃烧生成二氧化硫气体的焓变为△H1;1mol气态硫燃烧生成二氧化硫气体的焓变为△H2,则△H1_____△H2
(2) 常温下1g CH4完全燃烧并生成液态水,放出55.64kJ的热量,写出CH4燃烧的热化学方程式:_____________________________________________________
(3)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16. 95 kJ热量,其热化学方程式为:_______ ____。
(4)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为________ _________________ 。
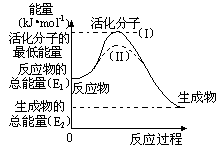 14、(12分)在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。
14、(12分)在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。
(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)环境先提供能量,该反应的△H= (用含E1、E2的代数式表示)。
(2)对于同一反应,图中虚线(II)与实线(I)相比,活化能 ,因此反应速率 ,你认为改变的条件是: 。
15、(12分)甲醇是一种很好的燃料,工业上用CH4和H2O(g) 为原料,通过反应Ⅰ和Ⅱ来制备甲醇.请回答下列问题:
(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L)中,在一定条件下发生 反应: CH4(g)+H2O(g)![]() CO(g)+3H2(g)(Ⅰ)
CO(g)+3H2(g)(Ⅰ)
达平衡时,CH4的转化率与温度、压强的关系如右下图所示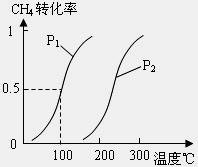
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为 .
②该反应的△H 0,△S 0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇: CO(g)+2H2(g)![]() CH3OH(g) △H<0 (Ⅱ)
CH3OH(g) △H<0 (Ⅱ)
若容器的容积不变,下列措施可增大甲醇产率的是 (填序号).
A.升高温度 B.将CH3OH(g)从体系中分离出来
C.恒容下充入He,使体系的总压强增大 D.再充入a mol CO和3a mol H2
16、(10分)现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为__________热反应,且m+n__________p(填“>”“=”或“<”).
(2)减压时,A的质量分数__________.(填“增大”“减小”或“不变”,下同)
(3)若容积不变加入B,则A的转化率__________,B的转化率__________.
(4)若升高温度,则平衡时B、C的浓度之比![]() 将__________.
将__________.
(5)若加入催化剂,平衡时气体混合物的总物质的量__________.
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________;而维持容器内压强不变,充入氖气时,混合物颜色__________(填“变深”“变浅”或“不变”).
| |温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(2)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变b.气体的密度不随时间改变
c.c(A)不随时间改变d.单位时间里生成C和A的物质的从相等
(3) 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
(4)某温度下平衡浓度符合下式c(A)·c(B)=c(C)·c(D)试判断此时的温度为 ℃
18、(8分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4 ===K2SO4 +2MnSO4 +10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/ mL | 室温下溶液颜色褪至无色所需时间/ min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 |
| 2.0 | 6.4 |
请回答:(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,用KMnO4表示的反应速率为:υ(KMnO4) = 。
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示,发现速度有突然变快的情况。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
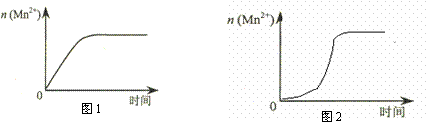
①该小组同学提出的假设是 。
②请你在表中空白处填上合适的物质帮助该小组同学完成实验方案。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/ min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
学校_______________________ 班级_______________________ 姓名________________________________ 考号_______________ ——————————密——————————封————————————线———————————内——————————禁止————————答题——
高二年级化学期中考试试卷答题卡
| 题号 | 选择题 | 13 | 14 | 15 | 16 | 17 | 18 | 总分 |
| 得分 |
选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 答案 | ||||||
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 |
13、(12分,每空3分)
(1)___ __
(2)__________________ _____________________________ ______。
(3)_______ ____。
(4)________ ______________ ___ 。
14、(12分,每空2分)
(1) , 。
(2) , , 。
15、(12分,每空3分)
(1)① . ② , .
(2)
16、(10分,第4题2分,其余每空1分)
(1)__________,__________。
(2)__________.
(3)__________,__________.
(4)__________.
(5)__________.
(6)__________;__________
17、(10分,每空2分)
(1) ,
(2) 。
(3) 。
(4) 。
18、(8分,每空2分)
(1) 。
(2) 。
(3)① 。
② 。
海南省国科园实验学校2015—2016学年度第一学期
高二年级化学期中考试试题答案
选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 答案 | A | B | D | C | A | D |
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | AC | D | D | B | CD | B |
13、(12分,每空3分)
(3)①N2(g)+2O2(g)===2NO2(g) ΔH=+67.8 kJ·mol-1
(4)B2H6(g)+3O2(g)===B2O3(s)+3H2O(l) ΔH=-2 165 kJ·mol-1
14.((12分,每空2分))
(1)放热; 需要; E2- E1
(2)降低;加快;使用了催化剂
| 15 | (12分,每空3分) (1)①0.0030mol•L﹣1•min﹣1;②>,>;(2)BD |
16、(10分,第4题2分,其余每空1分)
(1)放热,>(2)增大.(3)增大,减小.(4)减小.
(5)不变.(6)变深;变浅
18、(共8分)
(1)其他条件相同时,增大KMnO4浓度(或反应物浓度),反应速率增大
(2)1.5×10-2 mol / (L·min)
(3)①生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用)
[不指出MnSO4(或Mn2+)扣分]
②MnSO4