
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日

| 选项 | X | Y |
| A | SO2 | H2S |
| B | Cl2 | CO2 |
| C | NH3 | CO2 |
| D | SO2 | NO2 |

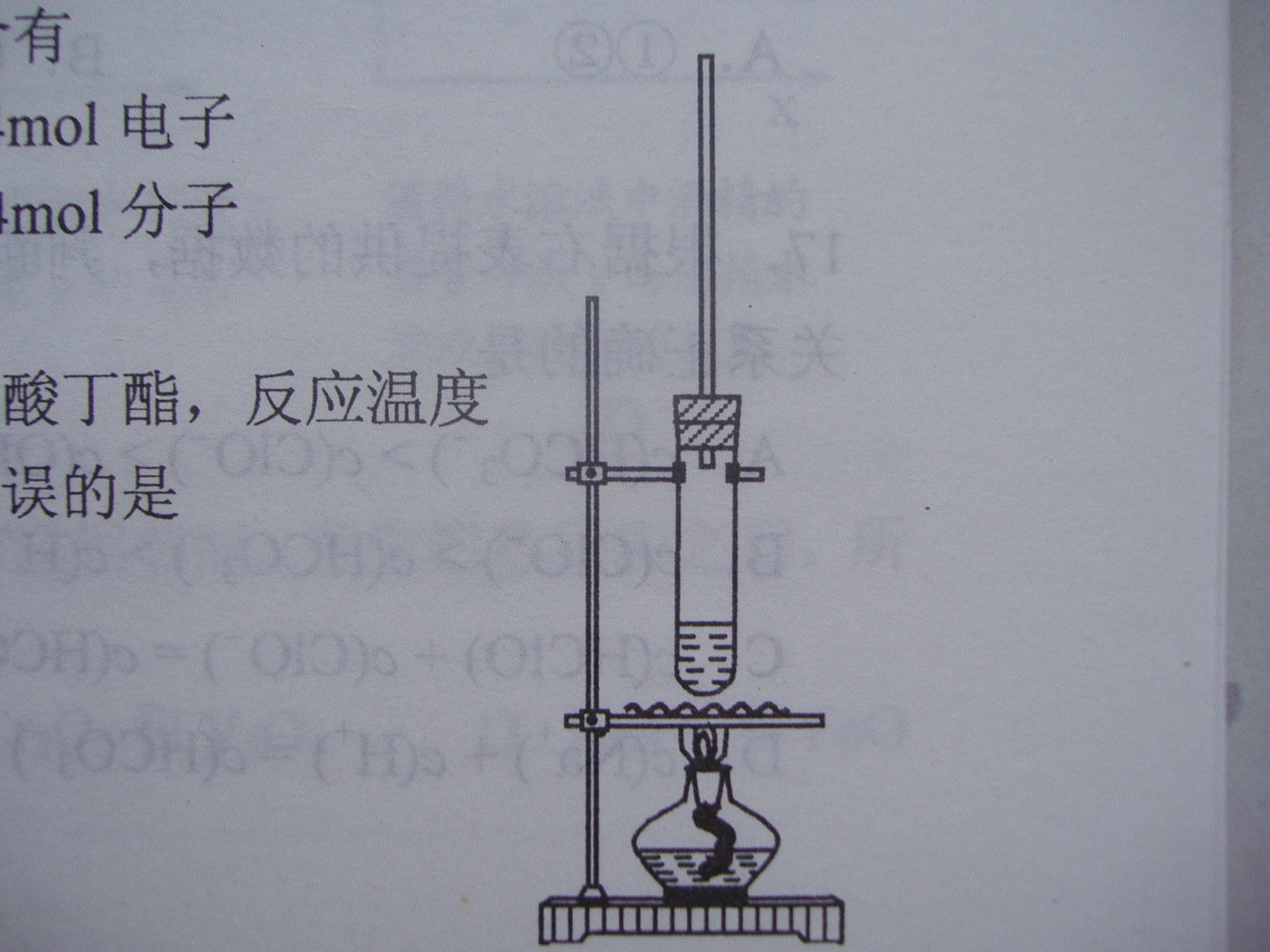 11. 醋酸溶液中存在电离平衡CH3COOH
11. 醋酸溶液中存在电离平衡CH3COOHC. 反应放热也是影响OA段反应速率的因素之一
D. 烘干时间过长,会导致测定结果偏小
15. 某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是
A.有1个氧原子B.有2个氧原子
C.有1个A原子D.有2个A原子
16. 已知,Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反。在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是
A.Al2S3、FeS和SB.Fe(OH)3和Al(OH)3
C.Fe2S3和 Al(OH)3 D. FeS、Al(OH)3和S
17. Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
则在pH=4的溶液中能够大量共存的离子组是
A.Fe3+、Cu2+、Cl-、NO3-B.Fe2+、K+、SO42-、NO3-
C.Cu2+、Na+、CO32-、SO42-D.Fe2+、K+、SO42-、Cl-
三、选择题(本题共20分,每小题4分,每小题有一个或两个正确选项。只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个,该小题不给分)
18. 向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的是
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液时,转移1mol电子时生成1mol白色沉淀
C.通入SO2时,SO2与I2反应,I2作还原剂
D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
19. 现有a mol/LNaX溶液和b mol/LNaY溶液,均显碱性,且HX酸性比HY强。下列说法正确的是
A.若a=b,则c(X-)<c(Y-) B.若pH(NaX) = pH(NaY),则a>b
C.若a<b,且c(X-)=c(Y-),则溶液中c(HX)<c(HY)
D.若两溶液等体积混合,则c(X-) + c(Y-) + c(HX) + c(HY) = a +b
20. 化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是
A.反应的正方向放热(t2时升温) B.H2S气体通入氯水中
C.t秒时合成氨反应达到平衡 D. NaOH溶液滴入Ba(HCO3)2溶液中
21. 下列离子方程式错误的是 ()
A.向碳酸氢镁溶液中加人过量氢氧化钠
Mg2++2HCO3-+2OH-→MgCO3↓+2H2O+ CO32-
B.Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+→2Fe3++3H2O
C.向NH4HSO4溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全
Ba2+ + 2OH- + NH4++H+ + SO42-→BaSO4↓+ NH3·H2O + H2O
D.大理石溶于醋酸:CaCO3 + 2CH3COOH →Ca2++ 2CH3COO—+ H2O + CO2↑
22. 将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/NaOH溶液至沉淀完全,测定生成沉淀的质量比合金的质量增加5.1克,则下列有关叙述中正确的是
A.加入合金的质量可能是6.4克 B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为100ml
D.溶解合金时收集到NO气体的体积为2.24升。
四、(本题共13分)
A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E顺序增大;C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A和气体物质EB4;EB4蒸气的密度是相同条件下空气密度的3.586倍。
23、指出A在元素周期表中的位置_________
24、写出D2A2的电子式_________________;写出CB与EA2反应的化学方程式_______________________________________
25、下表是不同物质中的键长和键能的数据,其中a、b、d未知,通过表中的数据分析,估计出a、b、c、d的大小顺序为______________________________
| 共价键 | C-C | C=C | C C | C-O | C=O | H-F | N=N | N N |
| 键长(nm) | 0.154 | 0.134 | 0.120 | 0.143 | 0.122 | 0.092 | 0.120 | 0.110 |
| 键能(kJ/mol) | A | b | 358 | c=805 | 569 | d |
氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
26、不能通过电解纯净的液态HF获得F2,其原因是_________;但电解液态KHF2时,两极分别得到F2和H2, 则F2在电解池的_____极产生。
 27、利用化学反应也能制取氟。请配平下列化学方程式:
27、利用化学反应也能制取氟。请配平下列化学方程式:
____K2MnF6+____SbF5→____KSbF6+____MnF3+____F2↑
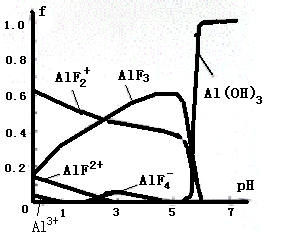
28、一定浓度的HF和Al2(SO4)3混合液中,铝的各种微粒含量f随
PH的分布曲线如图示。用NaOH使混合液的PH从5调整到7,
写出有关反应的离子方程式:__________________________。
五、(本题共11分)本题有2小题。
在一体积为2L的密闭容器中,气态物质A、B、E的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度A的转化率增大。
29、写出此反应的化学方程式
_________________________________;此
反应是___________热反应。
30、 根据图数据,从反应开始到第一次达到
平衡时平均速率v(E)为________________。n内曲线变化的原因可能是 _______(填编号)
A. 降低了温度 B. 使用了催化剂 C. 减小了容器的体积 D. 减少了A的物质的量
32、 设该反应达到平衡时的平衡常数为K1,保持温度不变,将容器体积减少一半,达到新的平衡后,测得B的平衡浓度为原来的2.2倍,平衡常数为K2,则_______(填编号)
A. 平衡向正反应方向移动,且K2>K1
B. 平衡移动过程中,正反应速率大于逆反应速率。
C. 达到新平衡时,A的浓度增大,且K1>K2
D. 达到新平衡时,E的浓度是原来的2倍多,且K1= K2
已知在25℃时,亚硝酸、次氯酸和氢硫酸的电离常数分别为:
亚硝酸 Ki = 4.6×10-4
次氯酸 Ki= 3.0×10-8
氢硫酸 Ki1= 9.1×10-8Ki2= 1.1×10-12
33、 写出氢硫酸的第一级电离平衡常数表达式:Ki1= _________________
34、在相同条件下,试比较H2S、HS-、HClO和HNO2的酸性强弱:
_________>__________>__________>__________
35、 保持温度不变,在氢硫酸溶液中加入少量盐酸,下列量会变小的是_____(填序号)
A.c(S2-)B.c(H+)C.Kw
D.氢硫酸电离平衡常数E.氢硫酸的电离度
六、(本题共12分)
用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:


36、在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发、_________、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________。
a. 蒸发的目的是得到热饱和溶液
b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液
d. 应蒸发至有较多晶体析出时为止
37、由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶
解度曲线,蒸发的目的是_________。
a. 得到热饱和溶液 b. 析出晶体
38、若在空气中加热MgCl2·6H2O,生成的是Mg(OH) Cl,写出反应的化学方程式:__________________________________________________________;用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_______________________________________________________________。
39、该流程产生的物质中,除Ca2+能被海洋生物利用外,还需综合利用的物质是_________。
40、MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和水,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a:b≈______________(取整数值)。
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

41、溴在元素周期表中位于_________周期,_________族。
42、步骤①中用硫酸酸化可提高Cl2的利用率,其原因是 。
43、步骤④的离子方程式:_______________________________________ 。
44、步骤⑥的蒸馏过程中,溴出口温度要控制在80—90℃。温度过高或过低都不利于生产 ,请解释原因:__________________________________________ 。
45、步骤⑧中溴气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是_____________,分离时液溴从分离器的_____(填“上口”或“下口”)排出。
46、不直接用步骤②后含Br2的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氧化”的原因是 。
47、下列有关溴单质的叙述正确的是
A.是易挥发的深红棕色液体
B.实验室少量液溴可保存在橡皮塞的棕色瓶中,并且加少量的水液封
C.可用酒精从溴水中萃取溴
D.溴可以与NaI溶液反应,置换出碘单质
八、(本题共10分)
有机物(C6H12)的两种异构体A和B和其他一些有机物之间有如图所示的转化关系。其中G的一氯取代物只有两种,A的分子结构中有3个甲基,B转变为F时只有一种产物。
请填写下列空白:
48、上述转化过程中,属于加成反应的是____________(填序号)
49、 有机物G的名称为_________________________,
50、 有机物A和C12H22O3结构简式分别为:A_________________、
C12H22O3_______________________________,
51、 写出②、③、两步反应的化学方程式:
②_______________________________________________________________________;
③_______________________________________________________________________,
52、A在一定条件下发生加聚反应的化学方程式:__________________________________。
胃复安是镇吐药及消化功能异常治疗药,其合成路线如下图:
已知:(1)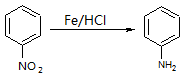
(2)R-NH2+(CH3CO)2OR-NHCOCH3+CH3COOH

请回答下列问题:
53、写出反应类型:反应①______________,反应③______________。
54、写出结构简式:M____________________________ E____________________________。
55、写出第⑥步除F外另一种产物的结构简式_______________________________。
56、B的含苯环结构的同分异构体G和H都能使FeCl3溶液变紫色,其中G只含3种不同化学环境的氢原子;H具有α—氨基酸的结构。
(1)写出2种G的同分异构体的结构简式________________________________。
(2)写出H(任一种)通过肽键连接形成高分子化合物的化学方程式
_____________________________________________________________。
57、已知:![]() ,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成
,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成![]() 的合成流程图(其它试剂自选)。
的合成流程图(其它试剂自选)。
十、(本题共14分)
科研人员发现,一些化学反应在固体之间发生和在水溶液中发生,产物不同。
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l 、+2。
将CuCl2·2H2O晶体和NaOH固体混合研磨,生成物中有一黑色的固体A。A不溶于水,但可溶于稀硫酸生成蓝色溶液B。
58、A的化学式为 ;A不同于CuCl2和NaOH在溶液中反应所得产物的可能原因是 。
59、在含0.02molB的溶液中加入适量氨水恰好完全反应,得到浅蓝色沉淀C和无色的溶液D;C溶于盐酸后,加入足量的BaCl2溶液,生成2.33g白色沉淀;无色的溶液D中加入足量的NaOH,加热收集到无色有刺激性气味的气体E。
①通过计算确定C的化学式为_____________。
②E是 (填物质名称),E在标准状况下的体积为 mL。
60、若向B中加过量氨水后再通入SO2至微酸性,最终得到白色沉淀F和无色的溶液。分析知,F是不含结晶水的复盐,其部分元素的质量分数为:Cu 39.31%、S 19.84%、N 8.67%。
①通过计算确定F的化学式。
②写出由B生成F的化学方程式。
61、将F与中等浓度的硫酸混合加热,会放出无色有刺激性气味的气体,析出紫红色沉淀,同时得到蓝色的溶液。写出该反应的化学方程式。
金山中学2014学年度第一学期高三年级化学学科期中考答案

二、(本题共36分,每小题3分,只有一个正确选项)
| 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
| C | C | B | A | C | B | D | C | B | A | D | D |
三、(本题共20分,每小题4分)。
| 18 | 19 | 20 | 21 | 22 |
| BD | BC | AC | AB | AC |

五、(本题共11分)
29、 2A + E ![]() 2B;放30、 0.05 mol/(L·min)(2分)
2B;放30、 0.05 mol/(L·min)(2分)
31、A32、D 33、![]()
34、HNO2>H2S>HClO>HS-(2分) 35、 A E(2分)

七(本题共12分)
41、第四VIIA(1分)42、酸化可抑制Cl2、Br2与水反应(1分)
43、Br2+SO2+2H2O→4H++2Br-+SO42-(2分,写成化学方程式不给分)
44、温度过高,大量水蒸气随水排出去,溴气中水分增加;(1分)温度过低,溴不能完全蒸出,吸收率低。(1分) 45、分液漏斗下口(2分)
46、氧化后的海水虽然含有溴单质,但浓度低;如果直接蒸馏原料,产品成本高; “空气吹出、SO2吸收、氧化”的过程实际上是一个Br2的浓缩过程。(2分) 47、AD(2分)
八、(本题共10分)
48、①⑤⑥(1分)
49、2,3-二甲基丁烷(1分)
50、(CH3)3CCH=CH2 、 (2分)

九(本题共12分)
53、(1)还原反应取代反应(2分);
54、
 (2分);
(2分);
55、 或CH3OH(1分)
或CH3OH(1分)
56、(1)
 (2分),
(2分),
-OH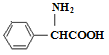
 +nH2O(2分);
+nH2O(2分);
57、 (2分)
(2分)
十、(本题共14分)
