
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
银川唐徕回民中学2016届高三8月月考化学试题
考试内容:1. 物质的量计算;2. 离子反应、离子方程式和氧化还原反应。
完成时间:100分钟满分:100分命题人:
可能用到的相对原子质量:H—1 O—16 Na—23 S—32 Cl—35.5 Fe—56 Ba—137
一、选择题(只有一个选项符合题意,2分/题,共50分)
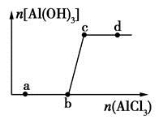
1.向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成Al(OH)3沉淀的量随AlCl3加入量的变化
关系如图所示。下列离子组在对应的溶液中一定能大量共存的是( )
 A.a点对应的溶液中:Na+、Fe3+、SO
A.a点对应的溶液中:Na+、Fe3+、SO![]() 、HCO3-
、HCO3-
B.b点对应的溶液中:Na+、S2-、SO![]() 、Cl-
、Cl-
C.c点对应的溶液中:Ag+、Ca2+、NO![]() 、F-
、F-
D.d点对应的溶液中:K+、NH4+、I-、CO32-
2. 下列有关溶液组成的描述合理的是( )
![]()

 1 mol Na2CO3晶体中含有的CO
1 mol Na2CO3晶体中含有的CO19.MnO2的一些性质或用途如右图所示。下列说法正确的是( )
A.①、②、③三个反应中MnO2均作氧化剂
B.足量MnO2与2 L 10 mol·L-1HCl共热,可生成5 mol C12
C.反应②若生成1 mol Al2O3,则反应过程中转移12 mol电子
D.反应③中K2CO3和KNO3的化学计量数均为1
20. 已知:还原性HSO![]() >I-,氧化性IO
>I-,氧化性IO![]() >I2。在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加
>I2。在含3mol NaHSO3的溶液中逐滴加入KIO3溶液。加
入KIO3和析出I2的物质的量的关系曲线如图所示。下列不正确的是( )
 A.0~
A.0~![]() 间的反应可用离子方程式表示:
间的反应可用离子方程式表示:
3HSO![]() +IO
+IO![]() =3SO
=3SO![]() +I-+3H+
+I-+3H+
B.![]() 点时消耗NaHSO3的物质的量为1.2 mol
点时消耗NaHSO3的物质的量为1.2 mol
C.![]() 点到
点到![]() 点,KIO3与NaHSO3反应生成I2
点,KIO3与NaHSO3反应生成I2
D. 当溶液中I-与I2的物质的量之比为5:2,加入的
KIO3为1.08 mol
21. 用密度为![]() g/cm3,质量分数是
g/cm3,质量分数是![]() 的浓盐酸,配制成体积为1:4的稀盐酸,密度为
的浓盐酸,配制成体积为1:4的稀盐酸,密度为
![]() g/cm3,则所配制的稀盐酸的物质的量浓度为( )
g/cm3,则所配制的稀盐酸的物质的量浓度为( )
A.![]() mol/LB.
mol/LB.![]() mol/L
mol/L
C.![]() mol/LD.
mol/LD.![]() mol/L
mol/L
22. 同温同压下,![]() g甲气体和2
g甲气体和2![]() g乙气体所占体积之比为1:2。根据阿伏加德罗定律判断,
g乙气体所占体积之比为1:2。根据阿伏加德罗定律判断,
下列叙述不正确的是( )
A.同温同压下甲和乙的密度之比为1:1
B. 甲与乙的相对分子质量之比为1:1
C. 同温同体积下等质量的甲和乙的压强之比为1:1
D. 等质量的甲和乙中的原子数之比为1:1
23. 设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A.0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA
B. 在25℃下,若CO与CO2的体积相等,则它们的物质的量相等
C.标准状况下,22.4L NO与CO2的混合气体中含有O原子数为3 NA
D.在常温常压下,22.4L氢气的质量为2 g
24. 已知溶质质量分数为98%的浓硫酸(![]() =1.84 g/mL),其物质的量浓度为18.4 mol/L,取
=1.84 g/mL),其物质的量浓度为18.4 mol/L,取
10 mL该硫酸与![]() mL水混合,配制成溶质质量分数为49%的硫酸溶液(
mL水混合,配制成溶质质量分数为49%的硫酸溶液(![]() =1.40 g/mL),
=1.40 g/mL),
其物质的量浓度为![]() mol/L。则
mol/L。则![]() 、
、![]() 分别为( )
分别为( )
A.![]() =10
=10 ![]() =9.2B.
=9.2B.![]() <10
<10 ![]() >9.2
>9.2
C.![]() >10
>10 ![]() =9.2D.
=9.2D.![]() >10
>10 ![]() <9.2
<9.2
25. 根据下列所给出的数据,得出的结论正确的是( )
A.在10%的NaOH溶液中,平均每9个水分子溶有1个OHˉ
B.将10g碳酸钙粉末加水配制成100mL溶液,CaCO3的物质的量浓度为1 mol/L
C.通入标准状况下11.2L HCl气体,可使1L 0.5 mol/L的盐酸的物质的量浓度增大一倍
D.已知某氢氧化钠溶液中Na+与H2O的个数之比为1:![]() ,则可求出此溶液中氢氧化钠的质
,则可求出此溶液中氢氧化钠的质
量分数20/(20+9![]() )
)
二、简答题(本题包括5道小题,10分/题,共50分)
26.(1)某一离子反应体系中反应物和生成物共有以下六种:MnO![]() 、H+、O2、H2O、H2O2、Mn2+。
、H+、O2、H2O、H2O2、Mn2+。
已知该反应中的H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是__________。
②该反应中,发生还原反应的过程是___________→___________。
③KMnO4溶液随着酸性的增强氧化性不断增强,应选择________(选填“稀硫酸”或“浓盐
酸”)进行KMnO4溶液的酸化。
(2)某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。已知K2S2O8的
氧化性比K2Cr2O7强。请将以上反应物与生成物编写成一个氧化还原反应方程式并配平
___________。
27.(1)某化学反应反应物和生成物如下:Al+NaNO3+H2O→Al(OH)3+N2↑+NaAlO2。
①该反应的氧化剂______,氧化产物是_______。
②反应过程中转移5 mol e-,生成标准状况下N2的体积________L。
③配平该反应的化学方程式:
___Al+___NaNO3+___H2O ═___Al(OH)3+___N2↑+___NaAlO2。
(2)氧化还原反应实际上包含氧化反应和还原反应两个过程,一个还原反应过程的离子方
程式为:NO![]() +4H++3e-═ NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中
+4H++3e-═ NO↑+2H2O。下列四种物质:KMnO4、Na2CO3、KI、Fe2(SO4)3中
的一种物质,滴加少量稀硝酸,能使上述反应过程发生。
①被还原的元素是_____;还原剂是_____。
②写出并配平该氧化还原反应方程式:_____。
③反应生成0.3mol H2O,则转移电子的数目为_____(用阿伏加德罗常数NA表示)。
④若反应后,氧化产物的化合价升高,而其他物质保持不变,则反应中氧化剂与还原剂的
物质的量之比将_____(填“增大”、“不变”、“减小”或“不能确定”)。
28.(1)在KI-淀粉溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝,这是因为
_________,其离子方程式是__________。在上述蓝色溶液中滴加足量Na2SO3溶液,蓝
色逐渐消失,这是因为(用离子方程式表示)________。以上实验条件下,ClO-、I2、
 SO
SO![]() 的氧化性由强到弱的顺序是______。
的氧化性由强到弱的顺序是______。
(2)右图表示的是向某NaOH和Na2CO3的混合溶液中
逐滴加入稀盐酸产生CO2的过程。
①依次写出![]() 点之前发生反应的离子方程式
点之前发生反应的离子方程式
____________、____________。
②写出![]() 点到
点到![]() 点发生反应的离子方程式_________。
点发生反应的离子方程式_________。
③若该NaOH和Na2CO3的混合溶液中含有![]() mol NaOH、
mol NaOH、![]() mol Na2CO3(
mol Na2CO3(![]() ),向其中滴
),向其中滴
入一定体积1 mol·L-1的稀盐酸,恰好使溶液中Cl-和HCO![]() 的物质的量之比为3:1,则滴
的物质的量之比为3:1,则滴
入稀盐酸的体积可能为___________L(用含![]() 的代数式表示)。
的代数式表示)。
29.(1)A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A,B的
物质的量之比为1:4。请回答:
①若Y是黄绿色气体,则该反应的离子方程式是___________;将Y与等物质的量的SO2充
分混合后通入品红溶液,未见其褪色,原因是________(请用化学方程式解释说明)。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液
为某浓酸,则反应所得的氧化产物的化学式为________,反应中氧化剂与还原剂的物
质的量之比是______。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,而且A可溶于X溶液中。
①A元素的元素符号为_____,则A与B的反应中氧化剂与还原剂的物质的量之比是_____。
②若含![]() mol X的溶液溶解了一定量A后,此时溶液中两种金属阳离子的物质的量恰好相
mol X的溶液溶解了一定量A后,此时溶液中两种金属阳离子的物质的量恰好相
等,则被还原的X的物质的量为________mol(用含![]() 代数式表示);为保证A与B充分
代数式表示);为保证A与B充分
反应后最终所得的溶液中同时含有上述两种金属阳离子,则此时B与A的物质的量应满
足的取值范围是_________<![]() <__________。
<__________。
30. 常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH![]() 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,
阴离子可能是Cl-、NO![]() 、SO
、SO![]() 、CO
、CO![]() ,已知:
,已知:
(1)五种盐均溶于水,水溶液均为无色;
(2)D的焰色反应呈黄色;
(3)A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
(4)若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
(5)若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中
沉淀消失。
(6)把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的白色沉淀。
请回答下列问题:
①五种盐中,一定没有的阳离子是_____;所含阴离子相同的两种盐的化学式是______。
②D的化学式为___________,D溶液显碱性的原因是__________(用离子方程式表示)。
③E和氨水反应的离子方程式是__________________。
④设计实验检验B中所含的阳离子________________。
高三8月月考化学参考答案

