
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
河北定州中学2016-2017学年第二学期高四化学开学考试
一、单项选择题
1.科学家开发出一种新型锂-氧电池,其能量密度极高,效率达90%以上.电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O![]() 2I2+4LiOH,对于该电池的下列说法不正确的是( )
2I2+4LiOH,对于该电池的下列说法不正确的是( )
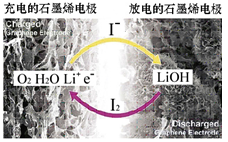
A.充电时Li+从阳极区移向阴极区
B.充电时阴极反应为LiOH+e-═Li+OH-
C.放电时负极上I-被氧化
D.放电时正极反应为O2+2H2O+4Li++4e-═4LiOH
2.下列物质属于纯净物的是
A.玻璃 B.蒸馏水 C.漂白粉 D.空气
3.反应2SO2+O2![]() 2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
2SO3,经过一段时间后,SO3的浓度增加了0.4 mol/L,在这段时间内用O2表示的反应速率为0.04 mol/(L·s),则这段时间为 ( )
A.5s B.2.5s C.0.1s D.10s
4.下列事实中,与电化学腐蚀无关的是
A.镀锡的铁制品,镀层部分受损后,露出的铁表面易被腐蚀
B.在空气中,光亮的银器表面逐渐变暗
C.埋在潮湿土壤里的铁管比埋在干燥土壤里的铁管更易被腐蚀
D.为保护海轮的船壳,常在船壳上镶入锌块
5.下列有关工业生产的叙述中,错误的是( )
A.制普通玻璃的主要原料是纯碱、石灰石、石英
B.氨是制作氮肥、硝酸、铵盐的重要原料
C.将二氧化硫催化氧化生成三氧化硫后,在吸收塔内用水吸收制得浓硫酸
D.炼铁的主要原理是在高温下,用还原剂从铁矿石中把铁还原出来
6.右图为元素周期表截取的短周期的一部分,即![]() 。四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
。四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
A.原子半径:W>Z>Y>X
B.气态氢化物的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物一定为强碱
7.在给定的条件下,下列选项所示的物质间转化均能实现的是
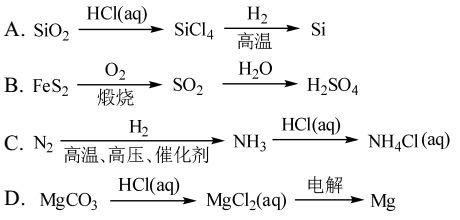
8.把0.6 mol X气体和0.4 mol Y气体混合于2 L容器中,使它们发生如下反应:3X(g)+Y(g)===nZ(g)+2W(g),在5 min时已经生成0.2 mol W,若测知以Z的浓度变化表示平均反应速率为0.01 mol·L-1·min-1,则上述反应中Z气体的化学计量数n的值是( )资*源%库
A.4 B.3 C.2 D.1
9.天然橡胶在硫化前受热易熔化、发粘,弹性差,硫化后硬度增大,弹性变好,不易老化。硫化前后,橡胶( )
A.由链状分子变成网状分子 B.由大分子变为小分子
C.由小分子变成大分子 D.由有机物变成无机物
10.下列化学反应的离子方程式正确的是
A.在稀氨水中通入过量SO2:NH3·H2O+SO2=NH4++HSO3-
B.硫酸氢钠溶液与足量氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O资*源%库
C.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O
D.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑
11.阿斯巴甜是目前使用最广泛的甜味剂.甜度约为蔗糖的200倍,其结构简式为:
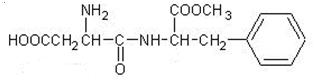
下列关于阿斯巴甜的说法正确的是( )
A.分子式为C14H19N2O5B.既能与酸反应又能与碱反应
C.不能发生水解反应 D.1mol该物质最多可与2molNaOH反应
12.下列说法正确的是
A.Na2O和Na2O2的化学键类型相同,其中阴、阳离子的个数比也相同
B.通过化合物在熔融状态下的导电性实验,可确定是离子化合物还是共价化合物
C.HClO和PCl3的分子结构中,每个原子最外层都具有8电子稳定结构
D.SO2水溶液能导电,是因为SO2分子中共价键破坏而发生电离资*源%库
13.离子方程式:RO3n—+F2+2OH-==RO4—+2F—+H2O,由此可知在RO3n—中,元素R的化合价是
A.+4 B.+5 C.+6 D.+7
14.下列物质中,既能与NaOH溶液又能与盐酸反应的氧化物是
A.Al2O3 B. Al C.Al(OH)3D.NaHCO3
15.下图是金属镁和卤素反应的能量变化图(反应物和生成物均为298 K时的稳定状态)。下列选项中不正确的是
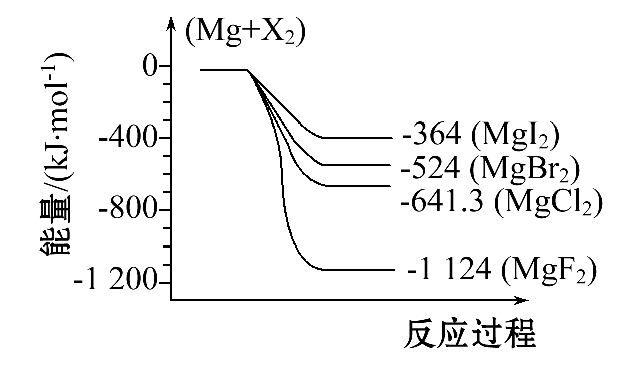
A.Mg与F2反应放热最多 B.MgF2(s)+Br2(l)![]() MgBr2(s)+F2(g)吸热
MgBr2(s)+F2(g)吸热
C.MgBr2与Cl2反应放热 D.化合物的热稳定顺序:MgI2>MgBr2>MgCl2>MgF2
16.下列有关物质的性质、应用或制取的说法正确的是
A.自来水厂可用明矾对水进行消毒杀菌
B.工业上将氯气通入澄清石灰水中,制取漂白粉
C.除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤
D.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸
17.将 4mol A气体和2mol B气体在2L 固定体积的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)![]() 2C(g).若经2s后测得 C 的浓度为 0.6 mol•L-1,现有下列几种说法,其中正确的是( )
2C(g).若经2s后测得 C 的浓度为 0.6 mol•L-1,现有下列几种说法,其中正确的是( )
A. 用物质A表示的反应的平均速率为0.2 mol•L-1•s-1
C. 2s时物质A的转化率为70%
B. 用物质B表示的反应的平均速率为0.1 mol•L-1•s-1
D. 2s时物质B的浓度为0.7 mol•L-1
18.在硫酸溶液中,NaClO3和Na2SO3能按物质的量之比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为( )
A.Cl2B.Cl2O7C.ClO2D.Cl2O
19.下列粒子不属于等电子体的是
A.CH4和NH3B.N2和CO
C.HCl和H2O D NH2-和H3O+
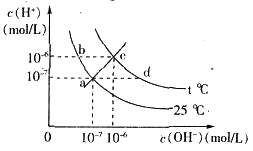
20. 在不同温度下,水溶液中c(![]() )与c(
)与c(![]() )有如图所示关系,下列有关说法正确的是
)有如图所示关系,下列有关说法正确的是
二、综合题
21.实验室由废铜屑制胆矾(CuSO4·5H2O)的实验流程如下:
(1)洗涤铜屑油污的试剂为5% Na2CO3溶液,这是利用了Na2CO3溶液的 性.
(2)溶解铜屑一种方案是:将铜屑加入到稀硫酸与双氧水的混和液中并用30~40℃水浴加热,一段时间后,铜完全溶解,得到硫酸铜溶液。
①该反应的化学方程式为 .
②反应温度不能超过40℃的原因是 .
(3)由硫酸铜溶液获得胆矾的操作依次为 、 、过滤、洗涤、干燥。
22.(15分)某化学探究小组拟用废铜屑制取Cu(NO3)2:,并探究其化学性质。
I.如图,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液。
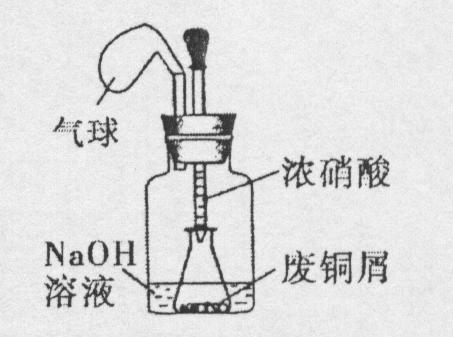
(1)写出铜与浓硝酸反应的离子方程式 。
(2)①装置中NaOH溶液的作用是 。
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、 、过滤。
③你认为此装置是否合理,并说明原因 。
如果不合理,同时在原装置上改进;如果合理,只需说明原因。
Ⅱ.为了探究![]() 的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
的热稳定性,探究小组按下图装置进行实验。(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
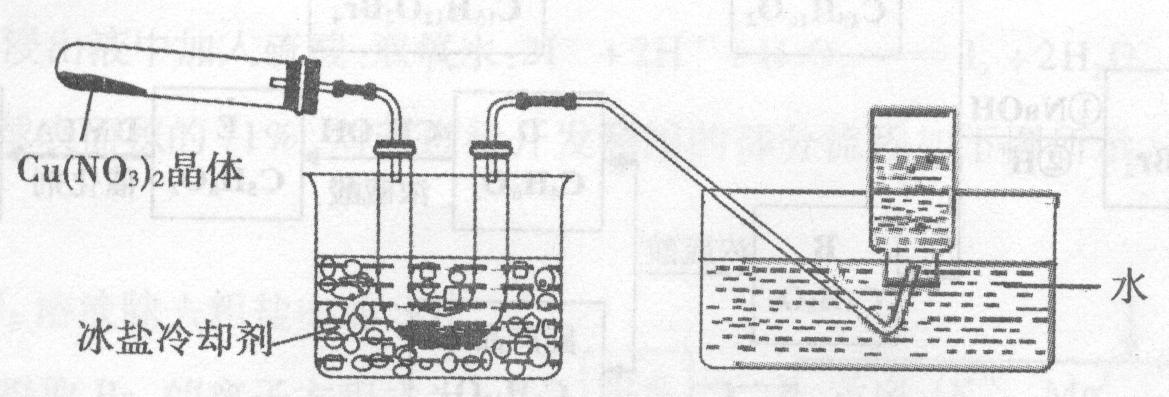
【实验操作及现象】往试管中放人研细的无水Cu(NO3)2:晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体。
【解释与结论】
(3)①红棕色气体是 。
②根据现象判断![]() 在加热条件下可以分解,其化学反应方程式为 。
在加热条件下可以分解,其化学反应方程式为 。
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3·Cu(OH)2]。
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4 mol/L的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品。
【实验数据】反应温度对样品的影响
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
| 样品中碱式碳酸铜 的质量分数/% | 90.9 | 92.7 | x | 92.0 |
(4)滤液中可能含有![]() ,写出检验
,写出检验![]() 的方法 。
的方法 。
(5)95℃时,样品颜色发暗的原因:____ 。
(6)70C时,实验得到2.38 g样品,取此样品加热至分解完全(杂质不分解),得到1.76 g固体,此样品中碱式碳酸铜的质量分数是 。
参考答案
BBABC CCDAA BBBAD CDDCC
21.
(1)碱 (2)①Cu+H2O2+H2SO4=CuSO4+2H2O (条件不写不扣分) ②防止H2O2分解
(3)蒸发浓缩、冷却结晶(各1分,共2分)
22.(15分)
I.(1) Cu+4H++2NO3一===Cu2++2NO2![]() +2H20(2分)
+2H20(2分)
(2)①吸收氮氧化物,防止污染空气(1分,合理即可)
②冷却结晶(1分)
③不合理,密闭体系中立即产生大量气体,会有安全隐患(1分)
(装置图如下,1分,合理即给分)或者合理,慢慢挤压胶头滴管控制反应速率,使NaOH溶液及时吸收NO2

II.(3)①NO2(1分)
②2Cu(N03)2![]() 2Cu0+4N02↑+02↑ (2分)
2Cu0+4N02↑+02↑ (2分)
III.(4)取少量滤液置于试管中,加入足量稀盐酸,将产生的气体通入澄清石灰水,溶液变浑浊,说明有C032-(2分,合理即给分)
(5)含有黑色的氧化铜(2分)
(6)93.3%(2分)