
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2015江苏高考压轴卷
化 学
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
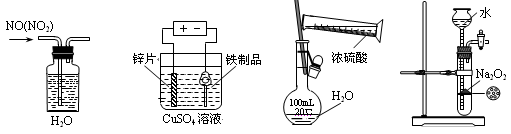 | 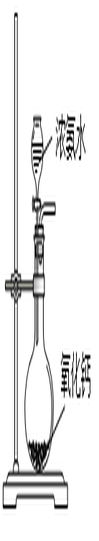 | 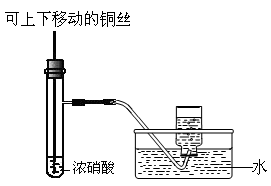 | 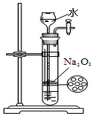 |
| B. 制备少量氨气 | C. 制备并收集少量NO2气体 | D. 制备少量氧气 |
| 甲 | 乙 | 丙 | 丁 | 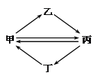 | |
| A | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 | |
| B | Cu | CuO | CuSO4 | CuCl2 | |
| C | NO | HNO3 | NO2 | NH3 | |
| D | Si | Na2SiO3 | SiO2 | SiF4 |
13. 下列叙述正确的是()
A.0.1mol·L-1Na2HPO4溶液中:c(Na+) + c(H+) = 2c(HPO42-) + c(OH-)
B.pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH>7
C.在pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,由水电离的c (H+) 后者大
D.25℃时,AgCl固体在20mL0.01mol·L-1氨水中的溶解度比在20mL0.01mol·L-1NaCl溶液中的溶解度大
14. 下列实验操作或结论正确的是 ( )
A.配制一定物质的量浓度的溶液时,将量取液态物质的量筒用水洗涤,洗涤液倒入容量瓶
B.用加热法可以分离KMnO4和碘单质的混合物
C.经氯气消毒的自来水,若用于配制Na2CO3溶液和FeSO4溶液均会使所配溶液变质
D.将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
15. 下列四个图像所反映的内容与相应反应符合的是(a、b、c、d均大于0)()
A.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)B.N2(g)+3H2(g)
4NO(g)+6H2O(g)B.N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
△H=-akJ·mol-1△H=-bkJ·mol–1
C.2SO3(g)![]() 2SO2(g)+O2(g)D.2N2O5(g)
2SO2(g)+O2(g)D.2N2O5(g)![]() 4NO2(g)+O2(g)
4NO2(g)+O2(g)
△H=+ckJ·mol–1△H=+dkJ·mol–1
非选择题
16.(12分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。
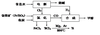
请填写下列空白:
⑴写出钛铁矿经氯化得到四氯化钛的化学方程式: 。
⑵由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
②若不考虑生产过程中物质的任何损失,该产业链中每合成19.2 t甲醇,至少需额外补充H2t。
⑶用甲醇-空气碱性(KOH)燃料电池作电源电解精炼粗铜(右图),在接通电路一段时间后纯Cu质量增加3.2 g。
①请写出燃料电池中的负极反应式: 。
②燃料电池正极消耗空气的体积是 (标准状况,空气中O2体积分数以20%计算)。
17.蓓萨罗丁是一种抗癌药物.其合成路线如图:
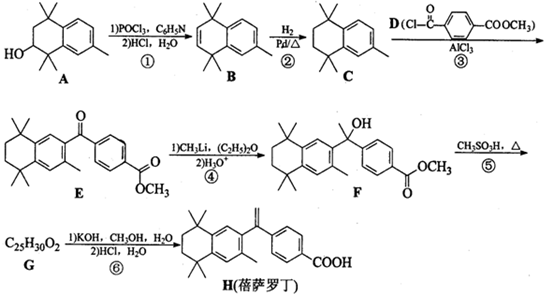
(1)化合物E的含氧官能团为和(填名称)。
(2)反应①→⑥中属于消去反应的是(填序号)。
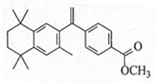
(3)合成路线中,化合物G的结构简式为。
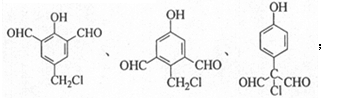
(4)写出同时满足下列条件的D的同分异构体的结构简式。
①能与FeCl3溶液发生显色反应;②1mol该物质与足量银氨溶液反应,能生成4mol Ag;③核磁共振氢谱显示有4种化学环境不同的氢
(5)已知:I.![]()
II.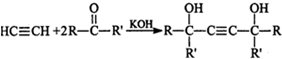
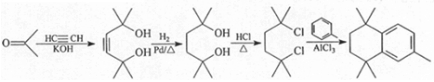
写出以甲苯、丙酮(![]() )和乙炔为原料,制备化合物C的合成路线流程图(无机试剂任用) 。
)和乙炔为原料,制备化合物C的合成路线流程图(无机试剂任用) 。
合成路线图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH。
CH3CH2OH。
18.(12分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下两种方法。
【方法一】还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下:
有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(1)写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。则在操作②中可用于调节溶液pH的试剂为: (填序号);
A.Na2O2B.Ba(OH)2C.Ca(OH)2D.NaOH
此时调节溶液的pH范围在 (填序号)最佳。
A.3~4 B.6~8 C.10~11 D.12~14
【方法二】电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(4)写出阴极的电极反应式 。
(5)电解法中加入氯化钠的作用是: 。
19. (15分)可利用下图中的实验装置测定足量铜与适量一定浓度的浓硝酸反应生成的NO气体和NO2气体的物质的量之比(用m表示),其中装置C由广口瓶和量气管组成,量气管由甲、乙两根玻璃管组成,用橡皮管连通,并装入适量水,甲管有刻度(0mL~50mL),乙管可上下移动。
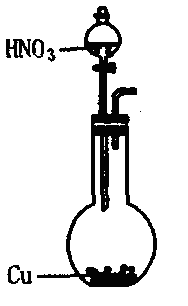
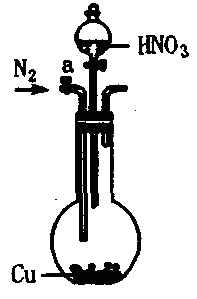
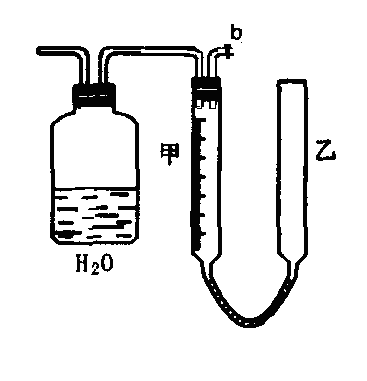
A B C
回答下列问题:
(1)实验中气体(NO和NO2)发生装置应选择 (填装置序号)。
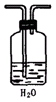
(2)实验中的气体(NO和NO2)通入C装置,请在下图的广口瓶中将导气管画出。
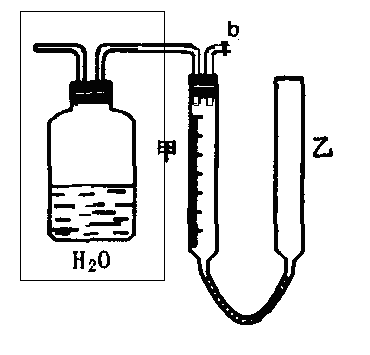
(3)要测定m值,需要将C中的溶液进行中和滴定,由于浓硝酸具有强氧化性,能把酸碱指示剂氧化褪色而影响实验。因此,中和滴定前必须进行的操作是 。
(4)连接好装置,检查气密性后,应进行两步必要的操作:
第一,打开b,向C装置的乙管中加适量水;
第二 。
(5)实验前甲、乙两管液面在同一水平面上,最后读数时乙管的液面高于甲管的液面。此时应进行的操作是 。
(6)实验后若量气管中气体的体积(换算成标准状况下)为V(L),C中硝酸的物质的量为nmol,则用含n和V的式子表示m= (结果可不必化简)。
20. (14分)S2Cl2是一种金黄色易挥发的液体(熔点:-76℃,沸点:138℃),易水解,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。向熔融的硫中通以干燥、纯净的C12即可生成S2C12。下图是实验室制备S2Cl2的装置(夹持装置、加热装置均已略去)。
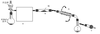
请回答下列问题:
⑴制取氯气的化学反应方程式(未配平)为:KMnO4+HCl(浓)—MnCl2 + KCl+ Cl2↑+H2O,请将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
+
⑵开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以下滴,经检查分液漏斗活塞没有堵塞,你认为应采取的措施是 。
⑶①在方框a中画出所缺装置图,并注明相关试剂的名称。
②图中c装置中应放置的试剂为碱石灰,其作用为 。
⑷某同学通过查阅资料发现:实验室常利用软锰矿(主要成分为MnO2和一些不溶性杂质)制取KMnO4晶体,其反应原理如下:
3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
3MnO42-+4H+=2MnO4-+MnO2↓+2H2O
请设计由软锰矿制备KMnO4晶体的实验步骤:① ;② ;③ ;④ 。
21. (12分)【选做题】本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质] 雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为:
化合物b中进行sp3杂化的原子有: 。
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是: (选填序号)。
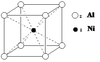
a.氯化钠 b.氯化铯 c.石英 d.金刚石
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni2+在基态时,核外电子排布式为: 。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。
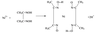
B.[实验化学] 以苯酚为原料合成对羟基苯乙酮的原理如下:

(1)乙酸苯酚酯制备:
将9.4 g苯酚溶解在60 mL10%的氢氧化钠溶液中,加入30g碎冰块,然后加入13.0 g乙酸酐,搅拌5 min。将反应后混合物倾入分液漏斗中,加入约4 mL CCl4。将有机相用试剂X和水洗涤然后无水CaCl2干燥,蒸馏收集193-197℃馏分。
①用碎冰块代替水可能的原因是:。
②乙酸酐过量的目的是:。
③有机相先用试剂X洗涤,X可能是。
(2)对羟基苯乙酮的制备:
将乙酰苯酚6.8 g,硝基苯20 mL 放在三口烧瓶中,搅拌下加入无水AlCl3 11 g(此时放热),加完后控制合适的温度,维持一定时间。然后冷却,倾入冰水中,用6mol/L HCl酸化分出硝基苯层,水层用氯仿萃取,蒸出氯仿得粗品。
①硝基苯的作用是。
②乙酸苯酚重排为对羟基苯乙酮反应条件对收率的影响关系如下表
| 反应温度/℃ | 反应时间(min) | 收率 |
| 30~35 | 180 | 10.0 |
| 20~25 | 60 | 18.0 |
| 20~25 | 120 | 26.0 |
| 20~25 | 180 | 58.5 |
适宜的温度是;反应时间是。
2015江苏高考压轴卷
化学答案
1. B 2. B 3.A 4.B 5.B 6. D 7. A 8.B 9. B 10. B 11. B 12.C 13. CD 14. C 15. AC
16.⑴ 2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO
⑵① 向逆反应方向进行
② 1.0
⑶① CH3OH-6e-+8OH-=CO32-+6H2O
② 2.8 L
17.(1)羧基 酯基
(2)①⑤
(3)
(4)
(5)
18.(1)Cr2O72― + 6 Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
(2)BD
(3)CD B
(4)2H+ + 2e― = H2↑或2H2O + 2e―= H2↑ + 2OH―
(5)增强溶液导电性或盐析
19.答案: (1)B
(2)
(3)将C中的溶液加适量水稀释
(4)第二,打开a,通足量N2,排净装置中的空气
(5)向下移动乙管,使甲、乙两管液面在同一水平面上
(6)(V-11.2n)/33.6n
20.
⑴ +
⑵将玻璃塞上的凹槽与漏斗口颈上的小孔对准(或拔去玻璃塞)
⑶①
②吸收尾气中的氯气,同时防止空气中的水进入使S2Cl2发生水解
⑷①将软锰矿与固体KOH和KClO3在高温下共熔,发生反应 ②冷却,加水溶解,滤去残渣 ③将滤液酸化,滤去MnO2沉淀 ④加热浓缩,冷却结晶
21. A.(1)<
(2)C、N、O
(3)b
(4)①1s22s22p63s23p63d8或[Ar] 3d8
②
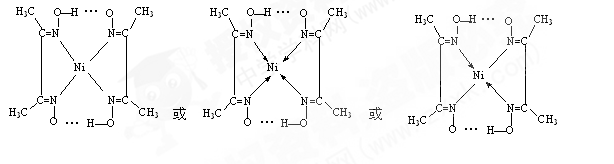
B.(1)①该反应是放热反应,碎冰温度低有利于酯的生成
②提高苯酚的转化率
③Na2CO3或NaHCO3溶液
(2)①作(极性)溶剂
②20~25;180min