
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016-2017学年北京市石景山区高三一模化学试卷(带解析)
满分:
班级:_________ 姓名:_________ 考号:_________
一、单选题(共7小题)
1.下列反应中能量变化与其它不同的是( )
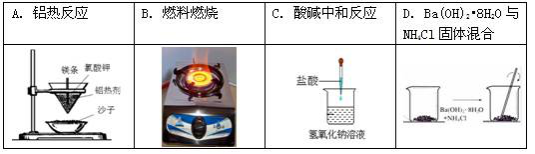
【答案】D
【考查方向】吸热反应和放热反应
【易错点】
本题考查化学反应与能量问题,题目难度不大,注意常见的放热反应和吸热反应有哪些。
【解题思路】
化学反应存在吸热反应和放热反应,一般来说,化合反应、活泼金属与酸的反应以及与水的反应属于放热反应,碳和二氧化碳的反应属于吸热反应。
【解析】由题意可知:铝热反应、燃料的燃烧、酸碱中和反应、活泼金属与酸的反应均是放热反应,而Ba(OH)2•8H2O与NH4Cl的反应是吸热反应,所以,本题正确答案是D。
故选D。
2.晋葛洪《抱朴子内篇·黄白》记载“曾青涂铁,铁赤色如铜”(“曾青”是指硫酸铜)。下列说法不正确的是( )
A.记载中的反应属于置换反应
B.记载中蕴含了湿法炼铜的原理
C.由记载得出铁单质是赤色(红色)
D.每生成1mol铜转移2mol电子
【答案】C
【考查方向】置换反应
【易错点】
铁单质不是赤色(红色),是银白色。
【解题思路】
A.该反应为置换反应;
B.因该反应在溶液中进行,所以记载中蕴含了湿法炼铜的原理;
C.赤色是铜单质的颜色;
D.铜元素的化合价由+2价降低到0价。
【解析】
A.因记载中的反应为Fe+CuSO4=FeSO4+Cu,该反应为置换反应,所以,A正确;
B.因该反应在溶液中进行,所以记载中蕴含了湿法炼铜的原理,因此,B正确;
C.由于铁赤色如铜是指覆盖在铁表面的铜单质,赤色是铜单质的颜色,因此,C错误;
D.根据化学反应Fe+CuSO4=FeSO4+Cu,铜元素的化合价由+2价降低到0价,所以每生成1mol铜转移2mol电子,因此,D正确。
故选C。
3.相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
A.若分子数相等,则体积相等
B.若原子数相等,则中子数相等
C.若质量相等,则质子数相等
D.若体积相等,则质量数相等
【答案】A
【考查方向】化学计量的计算、阿伏伽德罗定律
【易错点】
若分子数相等,则气体的物质的量相等,则体积相等。
【解题思路】
A.根据阿伏伽德罗定律,相同条件下,分子数与体积成正比;
B.由于中子数前者是16,后者是14,所以原子数相等,中子数不等;
C.由于12C18O和14N2两种气体的相对分子质量不同,若质量相等,则质子数不相等;
D.由于12C18O和14N2的质量数分别为30、28,所以质量数不相等。
【解析】
A.根据阿伏伽德罗定律,相同条件下,分子数与体积成正比,所以相同状况下的12C18O和14N2两种气体,若分子数相等,则体积相等,因此,A正确;
B.由于中子数前者是16,后者是14,所以原子数相等,中子数不等,因此,B错误;
C.由于12C18O和14N2两种气体的相对分子质量不同,若质量相等,则质子数不相等,因此,C错误;
D.由于12C18O和14N2的质量数分别为30、28,所以质量数不相等,因此,D错误。
故选A。
4.关于阿司匹林,下列说法正确的是( )
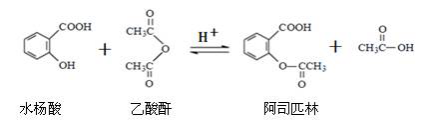
A.不能用FeCl3溶液鉴别水杨酸和阿司匹林
B.服用阿司匹林出现水杨酸反应时,可静脉注射NaHCO3溶液
C.1 mol阿司匹林最多可消耗2 mol NaOH
D.该反应不属于取代反应
【答案】B
【考查方向】有机化合物的结构及其化学反应。
【易错点】
本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力。
【解题思路】
A.由于水杨酸中有酚羟基,而阿司匹林中没有酚羟基;
B.由于水杨酸中含有羧基,可静脉注射NaHCO3溶液;
C.由于阿司匹林中有1个羧基、一个酯基,酯基水解后生成酚羟基;
D.根据反应特征,该反应为取代反应。
【解析】
A.由于水杨酸中有酚羟基,而阿司匹林中没有酚羟基,所以能用FeCl3溶液鉴别水杨酸和阿司匹林,因此,A错误;
B.由于水杨酸中含有羧基,所以服用阿司匹林出现水杨酸反应时,可静脉注射NaHCO3溶液,因此,B正确;
C.由于阿司匹林中有1个羧基、一个酯基,酯基水解后生成酚羟基,所以1 mo阿司匹林最多可消耗3molNaOH,因此,C错误;
D.根据反应特征,该反应为取代反应,所以,D错误。
故选B。
5.高炉炼铁的主要反应为:![]() ,已知该反应在不同温度下的平衡常数如下:
,已知该反应在不同温度下的平衡常数如下:
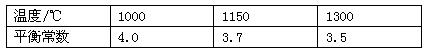
下列说法正确的是( )
A.增加Fe2O3固体可以提高CO的转化率
B.该反应的ΔH<0
C.减小容器体积既能提高反应速率又能提高平衡转化率
D.容器内气体密度恒定时,不能标志反应达到平衡状态
【答案】B
【考查方向】化学平衡的计算
【易错点】
本题考查化学平衡的有关计算、化学反应速率计算、平衡常数等,难度中等,注意掌握化学平衡常数的应用:1、用来判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、用来计算物质的转化率。
【解题思路】
A.增加固体的量平衡不移动;
B.K值减小,所以该反应为放热反应;
C.气体体积不发生变化的可逆反应,减小容器的体积,平衡不移动;
D.根据ρ=m/V,体积不变,当气体密度恒定时,标志反应达到平衡状态。
【解析】
A.由于Fe2O3是固体,增加固体的量平衡不移动,不会提高CO的转化率,因此,A错误;
B.根据表格提供的数据,升高温度,K值减小,所以该反应为放热反应,则ΔH<0,因此,B正确;
C.由于该反应是气体体积不发生变化的可逆反应,所以减小容器的体积,平衡不移动,所以不会提高平衡转化率,因此,C错误;
D.根据ρ=m/V,体积不变,随着反应的进行,气体的质量发生变化,即气体的密度发生变化,当气体密度恒定时,标志反应达到平衡状态,所以,D错误。
故选B。
6.下列解释事实的反应方程式正确的是( )
A.亚硫酸钠水溶液显碱性:![]()
B.SO2的水溶液显酸性:![]()
C.燃煤时加入石灰石减少SO2排放:![]()
D.浓NaOH溶液处理少量二氧化硫:![]()
【答案】C
【考查方向】离子方程式的书写
【易错点】
本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,注意电极反应方程式的书写,题目难度中等。
【解题思路】
A.多元弱酸的阴离子分步水解;
B.由于亚硫酸是多元弱酸,分步电离;
C.由于燃煤时加入石灰石减少SO2排放;
D.由于少量的SO2与NaOH溶液反应生成Na2SO3和水。
【解析】
A.由于多元弱酸的阴离子分步水解,离子方程式为SO32-+H2O![]() HSO3-+OH-、HSO3-+H2O
HSO3-+OH-、HSO3-+H2O![]() H2SO3+OH-,因此,A错误;
H2SO3+OH-,因此,A错误;
B.由于亚硫酸是多元弱酸,分步电离,方程式为SO2+H2O![]() H2SO3
H2SO3![]() H++ HSO3-,因此,B错误;
H++ HSO3-,因此,B错误;
C.由于燃煤时加入石灰石减少SO2排放,发生反应的方程式为2CaCO3+2SO2+O2![]() 2CaSO4+2CO2,因此,C正确;
2CaSO4+2CO2,因此,C正确;
D.由于少量的SO2与NaOH溶液反应生成Na2SO3和水,离子方程式为SO2+2OH-===H2O+SO32-,因此,D错误。
故选C。
7.下列实验装置不能达到实验目的的是( )
A.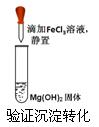 B.
B.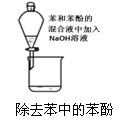 C.
C.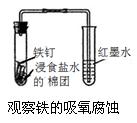 D.
D.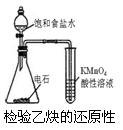
【答案】D
【考查方向】考查常见的基本实验操作
【易错点】
课本知识的迁移应用,牢固地掌握基础即可从中找到突破点理清思路。
【解题思路】
A.Fe(OH)3的溶解度比Mg(OH)2的溶解度小;
B.苯酚能与NaOH溶液反应生成溶于水的苯酚钠,而苯与水溶液互不相溶;
C.食盐水是中性溶液,所以铁钉插入浸食盐水的棉团中发生吸氧腐蚀;
D.电石中含有杂质,电石与饱和食盐水反应,除生成乙炔外,还有H2S、PH3等还原性气体。
【解析】
A.Fe(OH)3的溶解度比Mg(OH)2的溶解度小,向Mg(OH)2固体中滴加FeCl3溶液能实现沉淀的转化,A能达到目的;
B.苯酚能与NaOH溶液反应生成溶于水的苯酚钠,而苯与水溶液互不相溶,可以分液除去苯中的苯酚,B能达到目的;
C.食盐水是中性溶液,所以铁钉插入浸食盐水的棉团中发生吸氧腐蚀,氧气消耗导致气压降低,导气管中出现一段水柱,C能达到目的;
D.电石中含有杂质,电石与饱和食盐水反应,除生成乙炔外,还有H2S、PH3等还原性气体,它们也能使酸性高锰酸钾溶液褪色,D不能达到目的。
故选D。
第II卷(非选择题)
本试卷第二部分共有4道试题。
二、实验题(共1小题)
8.“张-烯炔环异构化反应”被《Name Reactions》收录。该反应可高效合成五元环状化合物:

(R1代表氢原子或烃基,X代表氧原子或氮原子)
某五元环状化合物I(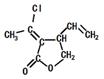 )的合成路线如下:
)的合成路线如下: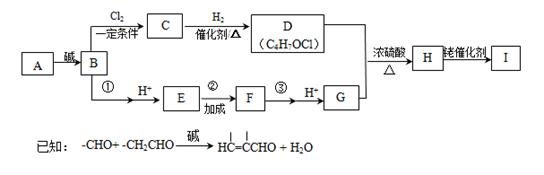
(1)烃的含氧衍生物A的相对分子质量为44,核磁共振氢谱显示分子中含有两种氢,则A的名称为_______。
【答案】乙醛
【考查方向】核磁共振氢谱、相对分子质量
【易错点】
根据流程图和已知信息,判断物质的化学式。
【解题思路】
根据流程图和已知信息,A为醛,核磁共振氢谱显示分子中含有两种氢。
【解析】
根据流程图和已知信息,A为醛,设A的通式为CnH2nO,A的相对分子质量为44,14n+16=44,解得n=2,核磁共振氢谱显示分子中含有两种氢,则A的结构简式为CH3CHO,名称为乙醛。
(2)A→B的化学反应方程式为____________________________________________。
【答案】2CH3CHO![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
【考查方向】有机化学方程式的书写
【易错点】
根据已知信息,判断常见的化学反应。
【解题思路】
根据已知信息,判断常见的化学反应。
【解析】
根据已知信息,A→B的化学反应方程式为2CH3CHO![]() CH3CH=CHCHO+H2O。
CH3CH=CHCHO+H2O。
(3)写出D顺式结构的结构简式_______________,B→C的反应类型为________。
【答案】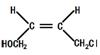 ,取代反应
,取代反应
【考查方向】结构式、常见的有机化学反应类型
【易错点】
有机化合物结构式的书写。
【解题思路】
根据上述分析,B为CH3CH=CHCHO,B与氯气在一定条件下发生取代反应生成C,D的分子式为C4H7OCl,D与G反应生成H,H发生“张-烯炔环异构化反应”生成I,说明D含有碳碳双键,所以C为CH2ClCH=CHCHO,D为CH2ClCH=CHCH2OH,据此判断。
【解析】
根据上述分析,B为CH3CH=CHCHO,B与氯气在一定条件下发生取代反应生成C,D的分子式为C4H7OCl,D与G反应生成H,H发生“张-烯炔环异构化反应”生成I,说明D含有碳碳双键,所以C为CH2ClCH=CHCHO,D为CH2ClCH=CHCH2OH,D的顺式结构的结构简式为![]() ;B到C的反应类型为取代反应。
;B到C的反应类型为取代反应。
(4)写出H的结构简式 _____________________________________________________________________。
【答案】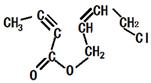
【考查方向】结构简式的书写
【易错点】
根据五元环状化合物可以逆推得出H的结构简式。
【解题思路】
根据五元环状化合物I(![]() ),可以逆推得出H的结构简式。
),可以逆推得出H的结构简式。
【解析】
根据五元环状化合物I(![]() ),可以逆推得出H的结构简式为
),可以逆推得出H的结构简式为![]() 。
。
(5)①的化学试剂是__________________________________________________ 。
【答案】银氨溶液(或新制氢氧化铜悬浊液)
【考查方向】常见的有机化学反应
【易错点】
根据H的结构简式推断。
【解题思路】
根据H的结构简式可知,该分子中含有酯基,是酸与醇发生酯化反应制得,D中含有羟基,则G中含有羧基,所以B与银氨溶液发生反应,![]() 然后酸化生成E,E为CH3CH=CHCOOH,E与氯气发生加成反应生成F,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应生成CH3C≡CCOONa,然后酸化得到G,G为CH3C≡CCOOH。所以①的化学试剂是银氨溶液(或新制氢氧化铜悬浊液)。
然后酸化生成E,E为CH3CH=CHCOOH,E与氯气发生加成反应生成F,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应生成CH3C≡CCOONa,然后酸化得到G,G为CH3C≡CCOOH。所以①的化学试剂是银氨溶液(或新制氢氧化铜悬浊液)。
【解析】
根据H的结构简式可知,该分子中含有酯基,是酸与醇发生酯化反应制得,D中含有羟基,则G中含有羧基,所以B与银氨溶液发生反应,![]() 然后酸化生成E,E为CH3CH=CHCOOH,E与氯气发生加成反应生成F,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应生成CH3C≡CCOONa,然后酸化得到G,G为CH3C≡CCOOH。所以①的化学试剂是银氨溶液(或新制氢氧化铜悬浊液)。
然后酸化生成E,E为CH3CH=CHCOOH,E与氯气发生加成反应生成F,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应生成CH3C≡CCOONa,然后酸化得到G,G为CH3C≡CCOOH。所以①的化学试剂是银氨溶液(或新制氢氧化铜悬浊液)。
(6)写出③的化学方程式_____________________________________________________________________ 。
【答案】![]()
【考查方向】有机化学方程式的书写
【易错点】
推断出相关物质的化学式。
【解题思路】
根据上述(5)分析,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应。
【解析】
根据上述(5)分析,F为CH3CHClCHClCOOH,F与NaOH的醇溶液在加热的条件下发生消去反应,则③的化学方程式为![]() 。
。
(7)下列说法正确的是__________。
a.H→I的过程中涉及到单键、双键和三键的断裂以及单键和双键的形成
b.C、D、E、F均能使溴的四氯化碳溶液褪色
c.与F含有相同官能团的同分异构体有8种(不含F本身)
【答案】a c
【考查方向】官能团、有机化学反应、同分异构体
【易错点】
同分异构体种类的判断。
【解题思路】
a.根据合成五元环状化合物的化学方程式推理;
b.F为CH3CHClCHClCOOH,不能使溴的四氯化碳溶液褪色;
c.F为CH3CHClCHClCOOH,与F含有相同官能团的同分异构体有C(1)-C(2)-C(3)- COOH,1、1,1、2,1、3,2、2,2、3,3、3共6种;C(1)-C(2)(COOH)-(3)有1、1,1、2,1、3共三种。
【解析】
a.根据合成五元环状化合物的化学方程式可知,H→I的过程中涉及到单键、双键和三键的断裂以及单键和双键的形成,a正确;
b.根据上述分析,F为CH3CHClCHClCOOH,F分子不能使溴的四氯化碳溶液褪色,b错误;
c.根据上述分析F为CH3CHClCHClCOOH,与F含有相同官能团的同分异构体有C(1)-C(2)-C(3)- COOH,1、1,1、2,1、3,2、2,2、3,3、3共6种;C(1)-C(2)(COOH)-(3)有1、1,1、2,1、3共三种,所以不含F本身,一共有8种,c正确。
三、综合题(共3小题)
9.中药在世界医学界越来越受到关注。中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注。
(1)As的原子结构示意图为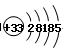 ,则其在周期表中的位置是_____________。
,则其在周期表中的位置是_____________。
【答案】第四周期,VA族
【考查方向】元素周期表结构
【易错点】
掌握元素周期表的基本结构及常见元素的位置。
【解题思路】
根据As的原子结构示意图可知,有4个电子层,最外层有5个电子。
【解析】
根据As的原子结构示意图可知,有4个电子层,在第四周期,最外层有5个电子,位于VA族。
(2)N元素非金属性比As强,下列说法正确的是_______。
①NH3的热稳定性比AsH3差
②HNO3的酸性比H3AsO4强
③N的原子半径比As的原子半径小
【答案】②③
【考查方向】元素周期表的结构及元素非金属性比较
【易错点】
非金属性越强,气态氢化物热稳定性越强。
【解题思路】
非金属性越强,气态氢化物热稳定性越强,最高价含氧酸的酸性越强,对同族元素来说,原子半径越小。
【解析】
非金属性越强,气态氢化物热稳定性越强,最高价含氧酸的酸性越强,对同族元素来说,原子半径越小,答案选②③。
(3)根据下图写出As2O5分解为As2O3的热化学方程式________________________。
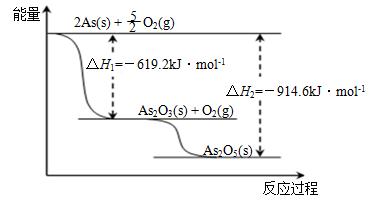
【答案】As2O5(s) = As2O3(s) + O2(g) △H= + 295.4 kJ·mol-1
【考查方向】热化学方程式的书写
【易错点】
掌握化学反应热的计算方法。
【解题思路】
根据图给数据,由As2O5分解为As2O3吸收热量为914.6-619.2= +295.4 kJ·mol-1。
【解析】
根据图给数据,由As2O5分解为As2O3吸收热量为914.6-619.2= +295.4 kJ·mol-1,所以反应的热化学方程式为As2O5(s) = As2O3(s) + O2(g) △H= +295.4 kJ·mol-1。
(4)查文献得知,可以从硫化砷(As2S3)废渣中提取As2O3,提取的工艺流程简图如下: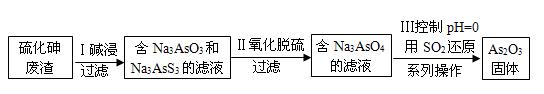
①As2S3、Na3AsS3中的S均为-2价,碱浸过程中发生的反应_______(填“是”或“不是”)氧化还原反应。
②过程Ⅲ的系列操作包括_________________________。
③写出过程Ⅲ的离子方程式______________________,过程Ⅲ中,酸性越强,As2O3的产率越高,请解释其原因_________________。
【答案】①不是 ②浓缩结晶,过滤,洗涤,烘干 ③ 2AsO43-+2SO2+2H+=As2O3+2SO42-+H2O;酸性越强,物质的氧化性或者还原性可能增强;增加氢离子浓度平衡正向移动促进反应的进行,有利于提高As2O3的产率。
【考查方向】氧化还原反应、离子方程式的书写、化学反应原理
【易错点】
酸性越强,物质的氧化性或者还原性可能增强;增加氢离子浓度平衡正向移动促进反应的进行,有利于提高As2O3的产率。
【解题思路】
①所有元素的化合价没有发生变化,碱浸过程中发生的反应不是氧化还原反应。
②过程Ⅲ是由滤液得到固体的过程,所以系列操作包括浓缩结晶,过滤,洗涤,烘干。
③在过程Ⅲ中,Na3AsO4具有氧化性,SO2具有还原性。酸性越强,物质的氧化性或者还原性可能增强;增加氢离子浓度平衡正向移动促进反应的进行,有利于提高As2O3的产率。
【解析】
①As2S3、Na3AsS3中的S均为-2价,As为+3价,Na为+1价,生成物Na3AsO3中Na的化合价为+1价,As的化合价为+3价,S的化合价为-2价,所以所有元素的化合价没有发生变化,碱浸过程中发生的反应不是氧化还原反应。
②过程Ⅲ是由滤液得到固体的过程,所以系列操作包括浓缩结晶,过滤,洗涤,烘干。
③在过程Ⅲ中,Na3AsO4具有氧化性,SO2具有还原性,在酸性溶液中发生氧化还原反应,反应的离子方程式为2AsO43-+ 2SO2 + 2H+===As2O3 + 2SO42- + H2O。酸性越强,物质的氧化性或者还原性可能增强;增加氢离子浓度平衡正向移动促进反应的进行,有利于提高As2O3的产率,所以过程Ⅲ中,酸性越强,As2O![]() 3的产率越高。
3的产率越高。
10.氰化物在冶金等行业应用广泛,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以 [Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
I.电解处理法
用图1所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。
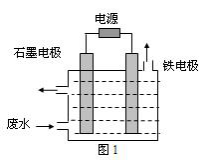
(1)铁电极为___________(填“阴极”或“阳极”),阳极产生ClO-的电极反应为______________________。
【答案】阴极 2OH-+Cl--2e- = ClO-+H2O
【考查方向】电解池原理、电极反应式的书写
【易错点】
根据题意,在一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去来进一步判断。
【解题思路】
根据题意,在一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去,所以活性电极铁为阴极。阳极Cl-失电子生成ClO-。
【解析】
根据题意,在一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去,所以活性电极铁为阴极。阳极Cl-失电子生成ClO-,用OH-平衡电荷,阳极的电极反应为2OH-+Cl--2e- = ClO-+H2O。
II.UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
(2)废水中的CN一经以下反应实现转化:CN一+H2O2+H2O=A+NH3↑,则A是___ (用符号表示)。
【答案】 HCO3-
【考查方向】质量守恒定律
【易错点】
根据化学反应中质量守恒定律判断。
【解题思路】
离子反应CN一+H2O2+H2O=A+NH3↑,根据原子守恒定律判断。
【解析】
离子反应CN一+H2O2+H2O=A+NH3↑,根据原子守恒定律,则A是HCO3-。
(3)K3[Fe(CN)6]在中性溶液中有微弱水解,用方程式表示水解反应___________________。
【答案】[Fe(CN)6]3-+3 H2O![]() Fe(OH)3 + 3HCN + 3CN-(或K3[Fe(CN)6] +3 H2O
Fe(OH)3 + 3HCN + 3CN-(或K3[Fe(CN)6] +3 H2O![]() Fe(OH)3 + 3HCN + 3KCN)
Fe(OH)3 + 3HCN + 3KCN)
【考查方向】化学方程式的书写
【易错点】
水解反应的表示方法。
【解题思路】
K3[Fe(CN)6]在中性溶液中有微弱水解,水解反应方程式为[Fe(CN)6]3-+3H2O![]() Fe(OH)3+3HCN+3CN-。
Fe(OH)3+3HCN+3CN-。
【解析】
K3[Fe(CN)6]在中性溶液中有微弱水解,水解反应方程式为[Fe(CN)6]3-+3H2O![]() Fe(OH)3+3HCN+3CN-。
Fe(OH)3+3HCN+3CN-。
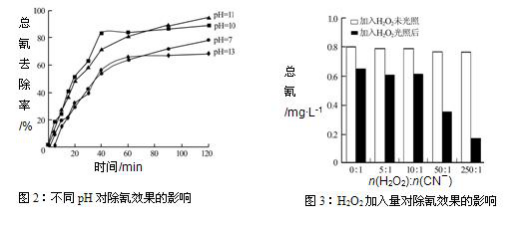
(4)含氰废水在不同pH下的除氰效果如图2所示,pH选择的最佳范围应为______(a.7-10;b.10-11;c.11-13),解释选择该pH范围的原因______________________________。
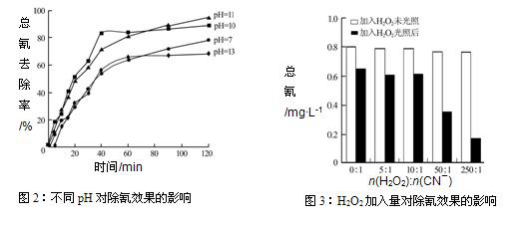
【答案】b 碱性适中,有利于[Fe(CN)6]3-转变为CN-而被氧化,碱性太强溶液中4[Fe(CN)6]3-+4OH-= 4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去,碱性太弱[Fe(CN)6]3-难以水解释放出CN-(且水解产生少量HCN有毒)
【考查方向】pH对化学反应的影响
【易错点】
碱性适中,有利于[Fe(CN)6]3-转变为CN-而被氧化,碱性太强溶液中4[Fe(CN)6]3-+4OH-= 4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去,碱性太弱[Fe(CN)6]3-难以水解释放出CN-。
【解题思路】
碱性适中,有利于[Fe(CN)6]3-转变为CN-而被氧化,碱性太强溶液中4[Fe(CN)6]3-+4OH-= 4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去,碱性太[Fe(CN)6]3-难以水解释放出CN-(且水解产生少量HCN有毒),所以pH选择的最佳范围应为10-11。
【解析】
碱性适中,有利于[Fe(CN)6]3-转变为CN-而被氧化,碱性太强溶液中4[Fe(CN)6]3-+4OH-= 4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去,碱性太[Fe(CN)6]3-难以水解释放出CN-(且水解产生少量HCN有毒),所以pH选择的最佳范围应为10-11,答案选b。
(5)图3表示某pH时,加入不同量H2O2,处理30min后测定的样品含氰浓度。由图可知:n(H2O2):n(CN-)=250:1时,剩余总氰为0.16 mg·L-1,除氰率达80%,计算0-30 min时间段反应速率v(CN-)= ________mg·L-1min-1(结果保留两位有效数字)。
【答案】 0.021
【考查方向】化学反应速率的计算
【易错点】
掌握化学反应速率的计算方法。。
【解题思路】
根据图3,加入H2O2未光照时,总氰为0.8mg/L,设溶液为1L,则消耗的氰为0.8mg/L×1L-0.16 mg·L-1×1L=0.64mg,据此求解。
【解析】
根据图3,加入H2O2未光照时,总氰为0.8mg/L,设溶液为1L,则消耗的氰为0.8mg/L×1L-0.16 mg·L-1×1L=0.64mg,所以0-30 min时间段反应速率为v(CN-)=![]() 0.64mg ÷(1L×30min)=0.021mg·L-1min-1。
0.64mg ÷(1L×30min)=0.021mg·L-1min-1。
11.某兴趣小组利用文献资料设计方案对氯及其化合物进行探究。
Ⅰ.用高锰酸钾和浓盐酸反应制取氯气
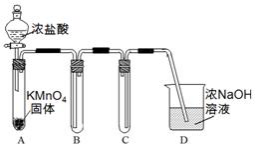
【答案】收集氯气; 防止D中的溶液进入B
【考查方向】气体的制取及其收集
【易错点】
了解常见实验装置及其作用。
【解题思路】
氯气的密度比空气大,用向上排空气法收集,所以装置B的作用为收集氯气,氯气有毒,用NaOH溶液进行尾气吸收,为防止倒吸,装置C的作用是防止D中的溶液进入B。
【解析】
氯气的密度比空气大,用向上排空气法收集,所以装置B的作用为收集氯气,氯气有毒,用NaOH溶液进行尾气吸收,为防止倒吸,装置C的作用是防止D中的溶液进入B。
(2)制得的氯气中加入适量水,得到饱和氯水,饱和氯水中含氯元素的微粒有____________(写出全部微粒)。
【答案】 Cl- Cl![]() 2 ClO- HClO
2 ClO- HClO
【考查方向】氯气及其性质
【易错点】
掌握氯气和水的之间的化学反应。
【解题思路】
氯气溶于水并与水发生反应,Cl2+H2O![]() H++Cl-+HClO,得到的氯水呈黄绿色,说明含有Cl2等。
H++Cl-+HClO,得到的氯水呈黄绿色,说明含有Cl2等。
【解析】
氯气溶于水并与水发生反应,Cl2+H2O![]() H++Cl-+HClO,得到的氯水呈黄绿色,说明含有Cl2,所以饱和氯水中含氯元素的微粒有 Cl- Cl
H++Cl-+HClO,得到的氯水呈黄绿色,说明含有Cl2,所以饱和氯水中含氯元素的微粒有 Cl- Cl![]() 2 ClO- HClO。
2 ClO- HClO。
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
①滤液漂白性增强的原因是_________________________(用化学平衡移动原理解释)。
②饱和氯水与石灰石反应生成HC1O的方程式是_______________________________。
Ⅱ.ClO3-、Cl-和H+反应的探究
【答案】
①Cl2 + H2O![]() HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强
HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强
②CaCO3+2Cl2 +H2O =2HC1O + CO2 + CaCl2
【考查方向】化学平衡移动原理、化学方程式的书写
【易错点】
增大HClO的浓度,漂白效果增强。
【解题思路】
①Cl2 + H2O![]() HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强。
HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强。
②根据上述现象,得饱和氯水与石灰石反应生成HC1O的方程式。
【解析】
①Cl2 + H2O![]() HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强,所以在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
HClO+HCl;CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强,所以在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
②根据上述现象,饱和氯水与石灰石反应生成HC1O的方程式是CaCO3+2Cl2 +H2O =2HC1O + CO2 + CaCl2。
(4)KClO3、KCl与硫酸可以反应。该小组设计了系列实验研究反应条件对反应的影响,实验记录如下(实验在室温下进行):
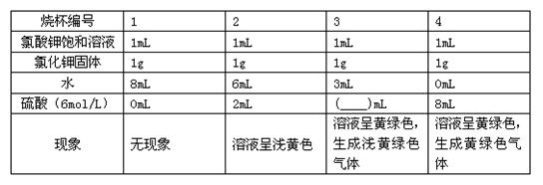
①该系列实验的目的_________________________。
②烧杯3取用硫酸的体积应为______________ mL。
【答案】①其他条件相同时,氢离子浓度不同对化学反应速率的影响; ② 5
【考查方向】实验探究
【易错点】
根据表格提供的信息,混合溶液的总体积均为9mL,烧杯3取用硫酸的体积应为5mL。
【解题思路】
①根据表格提供的信息,该反应在常温下进行,温度相同,每次试验时,氯酸钾溶液和氯化钾溶液的浓度相同,只有硫酸的用量不同,即氢离子浓度不同;
②根据表格提供的信息,混合溶液的总体积均为9mL。
【解析】
①根据表格提供的信息,该反应在常温下进行,温度相同,每次试验时,氯酸钾溶液和氯化钾溶液的浓度相同,只有硫酸的用量不同,即氢离子浓度不同,所以该系列实验的目的是其他条件相同时,氢离子浓度不同对化学反应速率的影响;
②根据表格提供的信息,混合溶液的总体积均为9mL,所以烧杯3取用硫酸的体积应为9-1-3=5mL。
(5)该小组同学查资料得知:将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色。设计最简单的实验验证Cl2中含有ClO2________________________________。
【答案】收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化
【考查方向】氯气及其化合物的性质
【易错点】
利用ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色加以判断。
【解题思路】
因为ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色,所以要验证Cl2中是否含有ClO2,可以根据此性质判断。
【解析】
因为ClO2沸点为10℃,熔点为-59℃,液体为红色;Cl2沸点为-34℃,液态为黄绿色,所以要验证Cl2中是否含有ClO2,简单的操作为收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化即可。