
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
7.明代《天工开物》记载“火法”冶炼锌: “炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭)。下列说法不正确的是
A.倭铅是指金属锌和铅的混合物
B.煤炭中起作用的主要成分是C
C.冶炼Zn的反应方程式为:ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D.该冶炼锌的方法属于热还原法
8.下列化学用语表示正确的是
A.中子数为20的氯原子:![]() B.二氧化硅的分子式:SiO2
B.二氧化硅的分子式:SiO2
C.硫化氢的结构式:H—S—HD.氯化铵的电子式:![]()
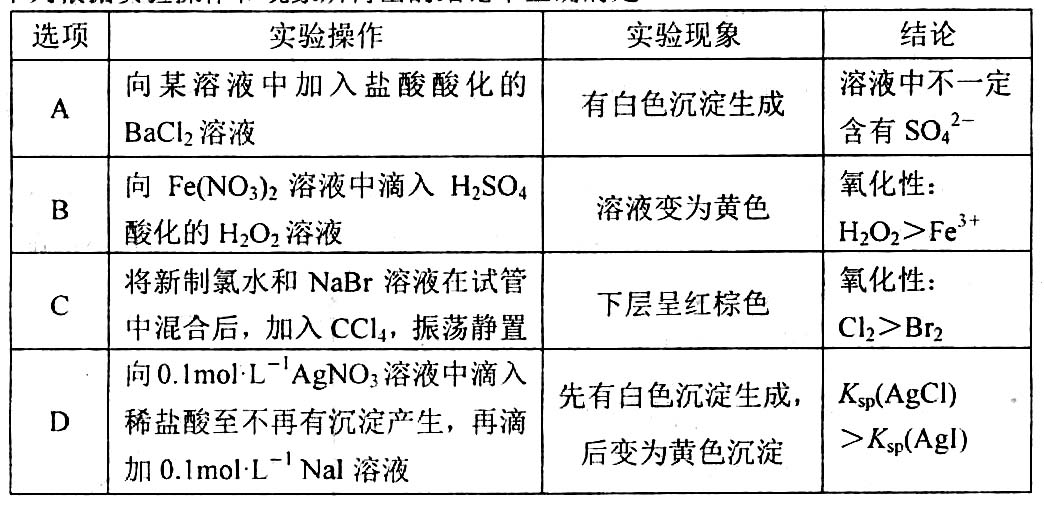 9.下列根据实验操作和现象所得出的结论不正确的是
9.下列根据实验操作和现象所得出的结论不正确的是
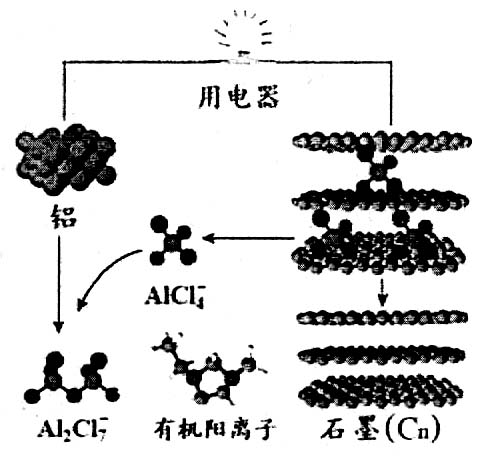 10.2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,分别以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如右图所示。下列说法不正确的是
10.2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,分别以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如右图所示。下列说法不正确的是
A.放电时,铝为负极、石墨为正极
B.充电时的阳极反应为:
Cn+ AlCl4--e-= CnAlCl4
C.放电时的负极反应为:
Al-3e-+7 AlCl4-===4A12C17-
D.放电时,有机阳离子向铝电极方向移动
11.下列有关电解质溶液中粒子浓度关系正确的是
A.pH=a的醋酸溶液,稀释10倍后,其pH=b,则a=b-1
B.含等物质的量的NaHSO3和Na2SO3的溶液:
2c(Na+)=3[c(HSO3-)+c(SO32-)+c(H2SO3)]
C.0.1mol·L-1盐酸与0.2mol·L-1氨水等体积混合:
C(NH3·H2O)>c(Cl-)>c(NH4+)>c(OH-)
D.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-)
 12.已知:(HF)2(g)
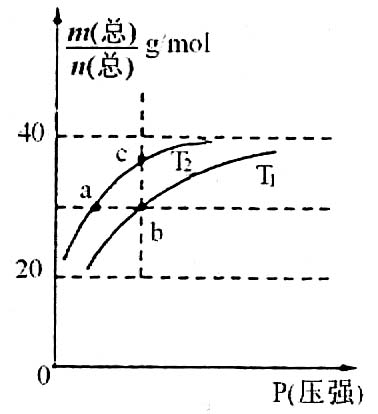
12.已知:(HF)2(g)![]() 2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
A.温度:T1< T2
B.平衡常数:K(a)=K(b) C.反应速率:v(b)>v(a) D.当 13.常温下向1L 0.1mol·L-1NH4C1溶液中,不断加入NaOH固体后,NH4+与NH3·H2O浓度的变化趋势如右图所示(不考虑溶液体积变化和氨气的挥发),下列说法不正确的是 A.M点溶液中水的电离程度比原溶液小 B.在M点时,n(OH-)-n(H+)=(a-0.05)mol C.随着NaOH的加入, D.当n(NaOH)=0.1mol时, c(OH-)>c(Cl-)>c(NH3·H2O) 26.(14分)I.已知C1O2是易溶于水难溶于有机溶剂的气体,常用于自来水消毒。实验室制备C1O2是用亚氯酸钠固体与氯气反应:2NaClO2+C12==2C1O2+2NaCl,装置如下图所示: 已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等; ②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表: 则该流程中所用(NH4)2C2O4溶液的pH_____7(填“>”或“<”或“=”) 28.(14分)I.“低碳经济”时代,科学家利用“组合转化”等技术对CO2进行综合利用。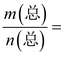 30g·mol-1时,n(HF):n[(HF)2]=2:1
30g·mol-1时,n(HF):n[(HF)2]=2:1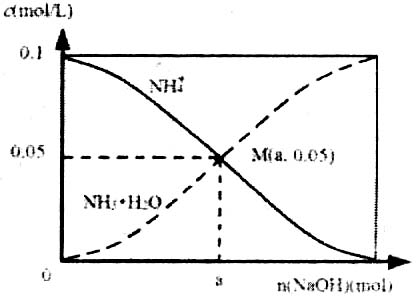
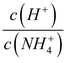 不断减小
不断减小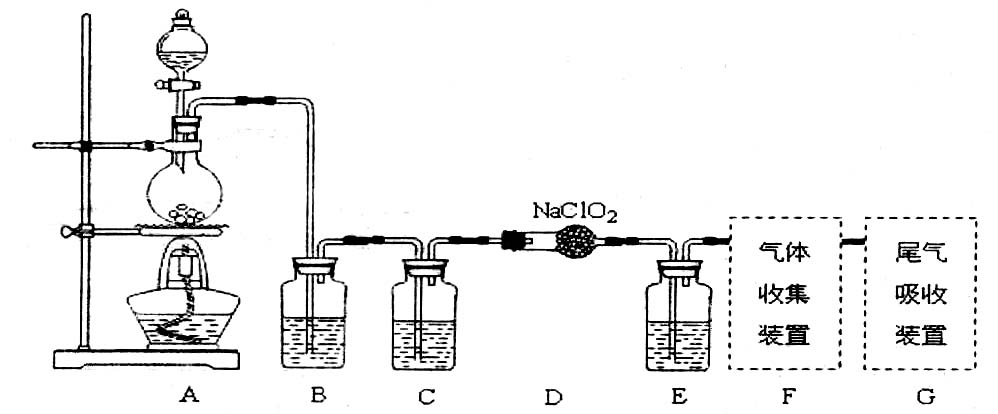 烧瓶内可发生的反应的化学方程式:________________________。
烧瓶内可发生的反应的化学方程式:________________________。
a、NaOH溶液 b、浓硫酸 c、饱和食盐水 d、CCl4e、饱和石灰水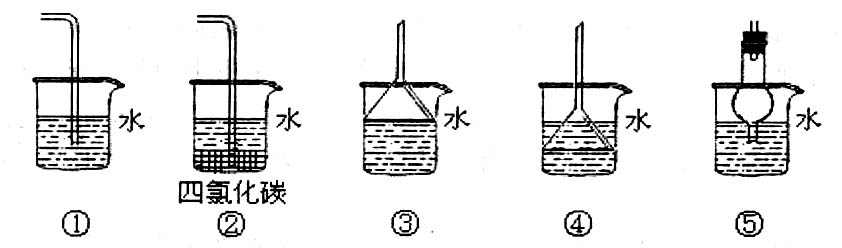
II.用C1O2处理后的自来水中,C1O2的浓度应在0.10~0.80mg·L-1之间。用碘量法检测水中C1O2浓度的实验步骤如下:取100mL的水样加稀硫酸调节pH至1~3,加入一定量的碘化钾溶液,振荡,再加入少量指示剂后,用1.0×10-4mol·L-1的Na2S2O3溶液滴定(己知:2S2O32-+I2==S4O62-+2I-)。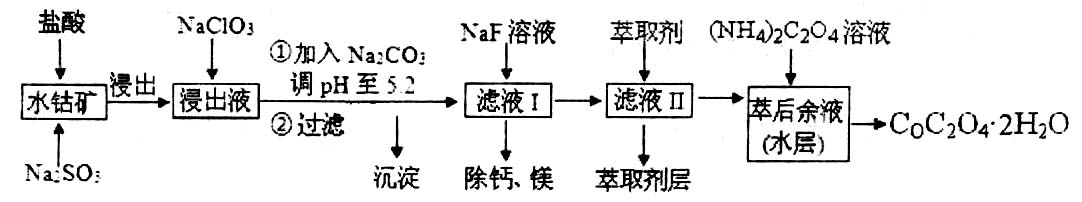 27.(15分)草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取COC2O4·2H2O工艺流程如下:
27.(15分)草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取COC2O4·2H2O工艺流程如下:
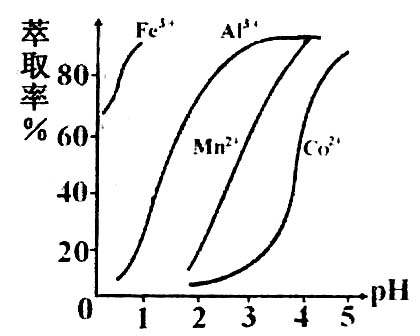 滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液
滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液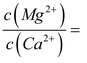 ______。
______。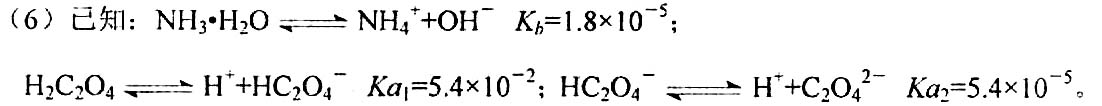 a.1 b.2 c.3 d.4
a.1 b.2 c.3 d.4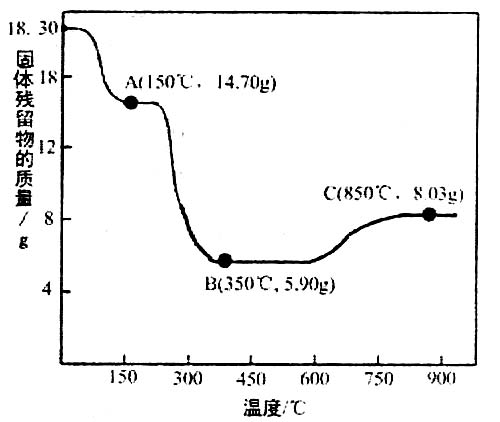 (7)CoC2O4·2H2O热分解质量变化过程如右图所示(其中600℃以前是隔绝空气加热, 600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是________________________________
(7)CoC2O4·2H2O热分解质量变化过程如右图所示(其中600℃以前是隔绝空气加热, 600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是________________________________
6H2(g)+2CO2(g)![]() CH2==CH2(g)+4H2O(g) △H=a kJ·mol-1
CH2==CH2(g)+4H2O(g) △H=a kJ·mol-1
已知:H2(g)的燃烧热为285.8 kJ·mol-1,CH2=CH2(g)的燃烧热为1411.0 kJ·mol-1,H2O(g)= H2O(l) △H=-44.0 kJ·mol-1,则a=______kJ·mol-1。
上述生成乙烯的反应中,温度对CO2的平衡转化率及催化剂的催化效率影响如图,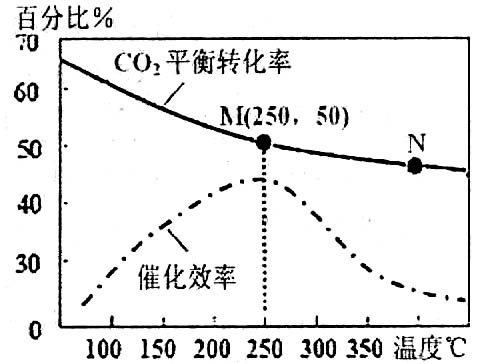 下列有关说法不正确的是_______(填序号)
下列有关说法不正确的是_______(填序号)
①温度越高,催化剂的催化效率越高
②温发低于250℃时,随着温度升高,乙烯的产率增大
③M点平衡常数比N点平衡常数大
④N点正反应速率一定大于M点正反应速率
⑤增大压强可提高乙烯的体积分数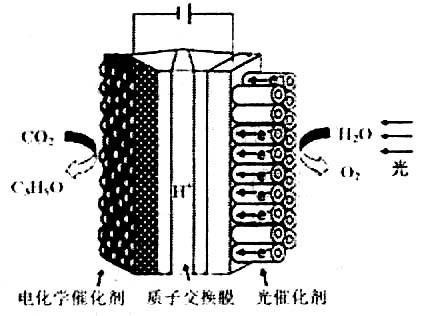 2012年科学家根据光合作用原理研制出“人造树叶”。右图是“人造树叶”的电化学模拟实验装置图,该装置能将H2O和CO2转化为O2和有机物C3H8O。
2012年科学家根据光合作用原理研制出“人造树叶”。右图是“人造树叶”的电化学模拟实验装置图,该装置能将H2O和CO2转化为O2和有机物C3H8O。
阴极的电极反应式为:_________________________
II.为减轻大气污染,可在汽车尾气排放处加装催化转化装置,反应方程式为:
2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。
2CO2(g)+N2(g)。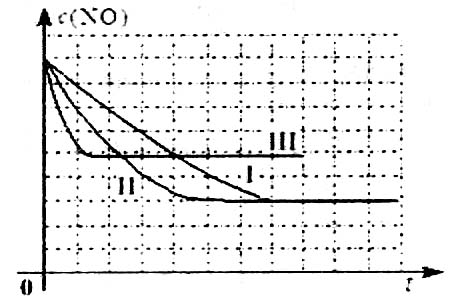
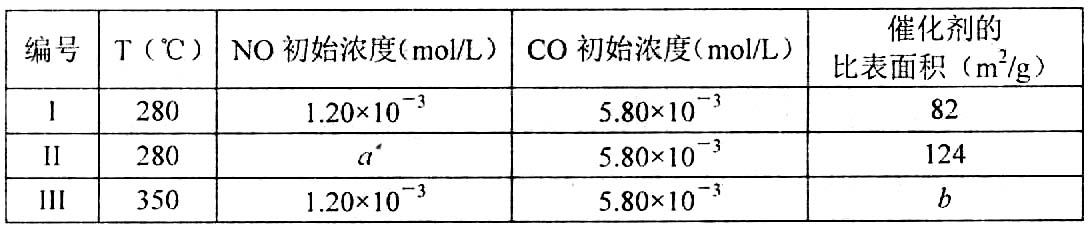 ①表中a=___________。
①表中a=___________。
②实验说明,该反应是__________反应(填“放热”或“吸热”)。
③若在500℃时,投料![]() NO的转化率为80%,则此温度时的平衡常数K=_____。
NO的转化率为80%,则此温度时的平衡常数K=_____。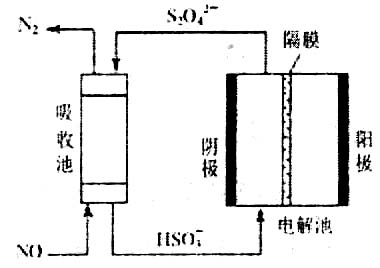 使用电化学法也可处理NO的污染,装置如右图。已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_____________。吸收池中除去NO的离子方程式为:__________________________________。
使用电化学法也可处理NO的污染,装置如右图。已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_____________。吸收池中除去NO的离子方程式为:__________________________________。
36.[化学—选修2:化学与技术](15分)(略)
37.[化学—选修4物质结构与性质](15分)
H2O和CS2分子中的原子都达到稳定结构。
 ②硫氰酸(H—S—C≡N)的熔点_____异硫氰酸(H—N=C=S)的熔点
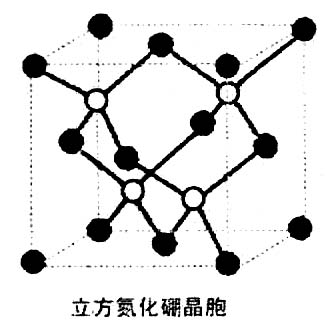
②硫氰酸(H—S—C≡N)的熔点_____异硫氰酸(H—N=C=S)的熔点①晶胞内的四个原子(如白球所示)所形成的空间结构为______形
②硼原子的杂化方式为_________。
③晶胞边长为anm则其密度为____g·cm-3(设阿伏加德罗常数的值为NA)
38、[化学—选修5:有机化学基础](15分)
工业上可由A和环己烯(![]() )为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
)为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
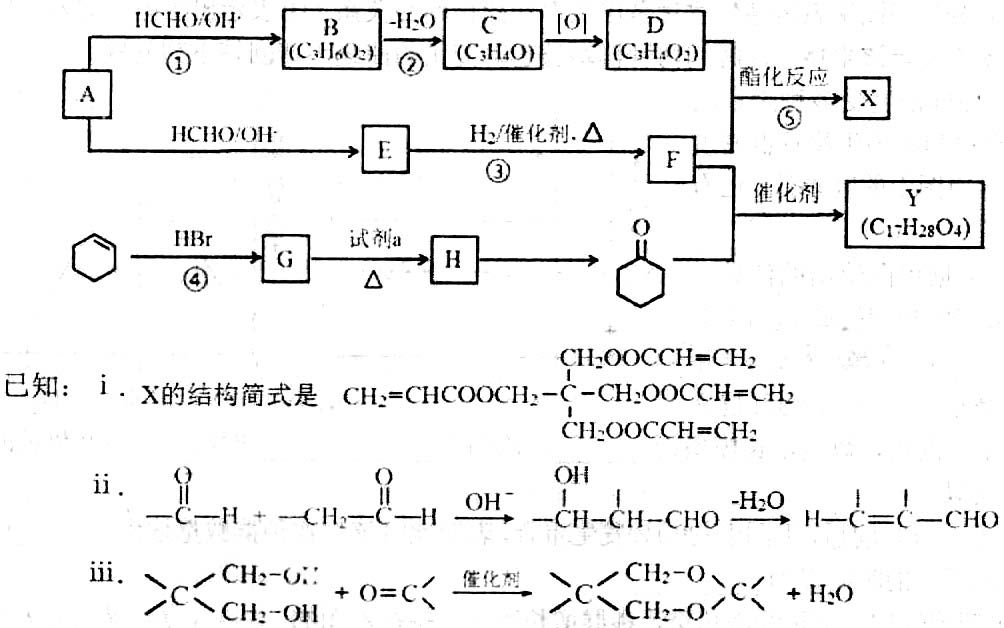 B中含氧官能团的名称是___________。
B中含氧官能团的名称是___________。
2016年淄博市高三第一次模拟考试
化学试题参考答案及评分标准
选择题(本题包括7小题,每题只有一个选项符合题意,每小题6分,共42分。)
7.A 8.C 9.B 10.D 11.B 12.C 13.D
26.(每空2分,共14分)
(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O(2分,有错无分,↑不扣分。KMnO4、KClO3等书写正确的也给分。)
(2)c b d(2分,有错无分)
(3)②③⑤(2分,有错无分,少一个扣1分)
(4)淀粉溶液(2分,有错无分),滴入最后一滴Na2S2O3溶液后,溶液的蓝色变为无色(或蓝色褪去),半分钟内不恢复原来的颜色(2分,蓝色变为无色1分,半分钟内不恢复原色1分)。
(5)2ClO2+8H++10I-=2Cl-+4H2O+5I2(2分,有错无分)
(6)0.22(2分)
27.[除(3)3分外,其余每空皆2分,共15分]
(1)还原Fe3+、Co3+为Fe2+、Co2+(2分,还原1分,Fe3+和Co3+共1分,)
(2)ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O (2分,有错无分)
(3)加入的碳酸钠(或CO32-)与H+反应,c(H+)降低(1分),使Fe3+和Al3+(用
M3+代替)的水解平衡M3++3H2O![]() M(OH)3+3H+(1分),向右移动,而产生氢氧
M(OH)3+3H+(1分),向右移动,而产生氢氧
化物沉淀(1分)(注:水解的离子方程式任写一个就给分1分,共3分)
(4)0.7(2分)[Ksp(MgF2)÷Ksp(CaF2)= 7.35×10-11÷1.05×10-10=0.7]
(5)c(2分)
(6)<(2分)
(7)Co3O4(2分)(写成CoO·Co2O3亦给分,但Co2O3·CoO不给分)
28.(14分)
(1)-127.8 (2分)(有错无分)
(2)①②④ (2分) (少一个扣1分,有错无分)
(3)3CO2+18H++18e-=C3H8O+5H2O (2分)(有错无分)
(4)①1.20×10-3 (1分) ② 放热 (1分)(只写“放”不给分)
③主要有三种情况,书写正确的均给2分。
第一种情况:设c(NO)=1mol·L-1,则K=160(2分)―――阅卷切块的(5)
第二种情况:设c(NO)=amol·L-1,则K=(2分)―――阅卷切块的(5)
第三种情况:设n(NO)=amol,容器的容积为V L,则K=(2分)――阅卷切块的(5)
(5)2HSO3-+2H++2e-=S2O42-+2H2O(2分)―――阅卷切块的(6)
2NO+2S2O42-+2H2O=N2+4HSO3-(2分)―――阅卷切块的(6)
37.(15分)
(1)O>S>C>H(1分)(不写大于号,但顺序正确就给分)
(2)O、S(2分)(每个1分,有错无分)
(3)1:1(2分)
(4)①大于(2分) ②小于(2分)
(5)分子(1分)
(6)①正四面体(2分) ②sp3(1分)
③(2分)――第③部分是阅卷切块的(7)
38.(15分)
(1)羟基(2分)醛基(2分)
(2)CH3CHO(2分)
(3)![]() (2分,其它合理答案均给分)
(2分,其它合理答案均给分)
(4)③④(3分)
(5)![]() -Br+NaOH
-Br+NaOH![]() -OH+NaBr(2分)
-OH+NaBr(2分)
(6)(HOCH2)3C-CHO(2分)