
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
曲周县第一中学2015-2016学年高三第二次摸底考试
化学试卷
可能用到的相对原子质量:
H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5
K:39 Ca:40 Fe:56 Cu:64 Zn:65 Ba:137
第Ⅰ卷(选择题 共54分)
一、单项选择题(每小题3分,共54分)
1.化学与生产、生活、社会密切相关。下列有关说法中不正确的是( )
A.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰。
D.氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料。
B.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物。
D.食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质。
2、下列关于Li、Na、K、Rb、Cs的叙述均正确的一组是 ( )
① 金属性最强的是铯 ② 氧化性最强的是锂离子
③ 在自然界中均以化合态形式存在 ④ Li的密度最小
⑤ 铯与水反应十分剧烈,甚至会发生爆炸 ⑥ 它们的氧化物都只有M2O和M2O2两种形式
⑦ 粒子半径:Rb+>K+>Na+,Cs>Cs+
A.①②③④ B.①②③④⑤⑦ C.②⑥ D. ④⑤⑥⑦
3、下列叙述正确的是( )
A.将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2,产生沉淀
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
C.向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失
D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO4固体,速率不改变快
4、下列溶液一定显酸性的是( )
A.含H+的溶液 B.c(OH-)<c(H+)的溶液
C.pH<7的溶液 D.能与金属Al反应放出H2的溶液
5、科学的假设与猜想是科学探究的先导和价值所在。在下列假设或猜想引导下的探究肯定没有意义的是( )
A.探究SO2和Na2O2可能化合生成Na2SO4
B.探究NO和N2O可能化合生成NO2
C.探究NO2可能被NaOH溶液完全吸收生成NaNO2和NaNO3
D.探究红色酚酞试液通入Cl2褪色,原因是溶液酸碱性改变或被漂白
6. 下列说法正确的是( )
A.由于H2O分子间存在氢键,所以H2O比H2S稳定。
B.11.2 L O2和CO2的混合气体中含有6.02×1023个氧原子。
C.固态NaCl不导电,是由于NaCl晶体中不存在阴、阳离子。
D.可逆反应达平衡状态后,化学反应速率发生变化,平衡不一定移动。
7、如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
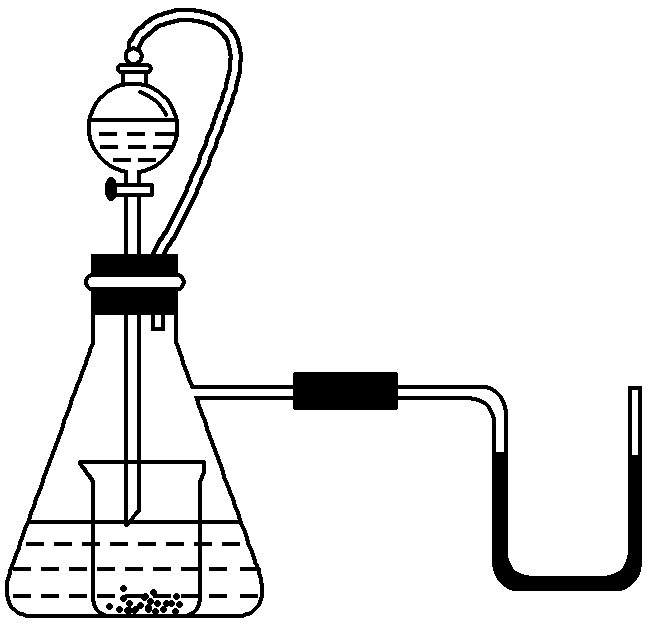 A.过氧化钠 B.氧化钠 C.钠D.钾
A.过氧化钠 B.氧化钠 C.钠D.钾
8、从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;
④将得到的产物熔融电解得到镁。
下列说法不正确的是( )
A.此法的优点之一是原料来源丰富 B.第④步电解时阴极产生氯气
C.①②③步骤的目的是从海水中提取MgCl2
D.以上提取镁的过程中涉及化合、分解和复分解反应
9.某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组为( )
A.OH-、Na+、K+、MnO4-B.H+、Cl-、Ba2+、NO3-
C.K+、Cl-、Na+、SO42-D.NH4+、Mg2+、Cl-、HCO3-
10.化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是( )
A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e- = 4OH-
B.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol
![]() C.纯碱水解的离子方程式:CO32- + H2O HCO3- + OH-
C.纯碱水解的离子方程式:CO32- + H2O HCO3- + OH-
D.Ca(HCO3)2溶液中加入过量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
11. 设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,11.2L氧气所含的原子数为NA
B.1.7g的NH+4离子中含有的电子数为NA
C.常温常压下,48gO3含有的氧原子数为3NA
D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
12.下列实验操作,正确的是 ( )
A.中和滴定时,用标准液润洗滴定管,用待测液润洗锥形瓶,并滴入l mL指示剂
B.配制物质的量浓度溶液时,将称量好的溶质溶于盛有适量水的烧杯中,溶解后立即倾入容量瓶中,继续进行洗涤和定容
C.制取Fe(OH)2时,吸取NaOH溶液的胶头滴管的末端应插入FeSO4溶液中,再缓缓将NaOH溶液挤出
D.溴乙烷和烧碱溶液共热后,将硝酸银溶液滴入水解液中,即可见到淡黄色沉淀
13.用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如右图所示。则下列说法正确的是( )
A.构成原电池时b极反应为: Cu﹣2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b 极质量可能减少也可能增加
D.构成的原电池或电解池工作后就可能产生大量气体
14.金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,
下列有关绿原酸的说法正确的是 ( )

A.绿原酸的分子式为C16H8O9
B.1mol绿原酸最多与7molNaOH反应
C.1个绿原酸分子中含有4个手性碳原子
D.绿原酸分子中有4种化学环境不同的氢原子
15、下列化学实验事实及其解释不正确的是( )
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水 蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
16、已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0_5 | 4.9×l0_10 | K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是
高三化学试题共6页第4页
B.amol·L—1HCN溶液与bmol·L—1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO3-) +2c(CO32-)
17、取一定质量的某物质在ag氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后容器内有b g氧气,测得b>a。下列物质中满足上述结果的是( )
A、HCOOH B、HCHO C、CH4D、C6H12O6
18、甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,将丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是 ( )
A、Al2(SO4)3 B、NaOH C、BaCl2D、FeSO4
(第Ⅱ卷、共46分)
19. (每空2分、共14分)
已知FeSO4·7H2O晶体在加热条件下发生如下反应:
2FeSO4·7H2O![]() Fe2O3 + SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3 + SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
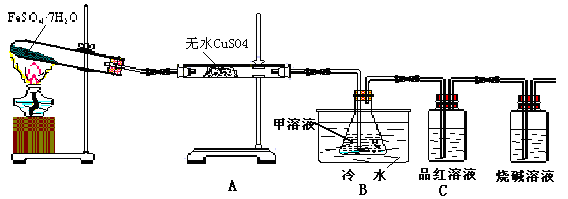
(1)用于检验SO2气体的装置是 (填装置的字母),确认水蒸气存在的现象是 ;
(2)利用装置B可以确认的产物是 ,装置B中的甲溶液可选(填序号) ,
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是 ;
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为 ,检验该分散系的最简方法为 。
20.(每空2分、共10分)A、B、C、D、E、F为六种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;C是地壳中含量最高的元素;在元素周期表中,F和C是周期不同、族相邻的关系,且F和E的原子序数之和为30,它们两两形成的化合物为甲、乙、丙、丁、戊、,这五种化合物中原子个数比如下表:(用元素符号作答)
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 化合物中各元 素原子个数比 | A:C=1:1 | A:B=1:1 | D:C=1:1 | E:F=1:3 | B:F=1:4 |
(1)写出F在周期表中的位置: ;
(2)向甲的水溶液中加入MnO2,氧化产物是(填化学式);已知有机物乙的分子为直线结构,乙的分子式为 ;
(3)若E单质可以与D的最高价氧化物的水化物溶液发生反应,请写出该反应化学方程式
。
(4)以E单质为阳极,在H2 S O4溶液中电解,可以在E表面形成致密氧化膜保护E材料不被腐蚀,写出阳极电极反应式为 。
21.(每空2分、共14分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量的 SiO2、Fe2O3杂质)生产铵明矾晶体NH4Al(SO4)2•12H2O,其工艺流程图如下:
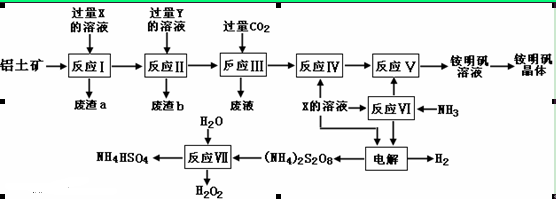
(1)废渣a、b 的成分分别是_____________、_____________(写名称)。
(2)流程图中X的化学式为_________________。
(3)反应Ⅲ的离子方程式为____________________________________________;从铵明矾溶液中获得铵明矾晶体的操作依次为(填操作名称)_____________、冷却结晶、过滤、洗涤。
(4)反应Ⅶ的化学方程式为 ;
NH4HSO4溶液中离子浓度由大到小顺序为 。
22.(每空2分、共8分)
(1)实验室制备氢氧化铁胶体化学方程式: 。
(2)能证明Na2SO3溶液中存在SO32-+H2O![]() HSO3-+OH-水解平衡的事实是 (填选项字母)。
HSO3-+OH-水解平衡的事实是 (填选项字母)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色退去
B.滴入酚酞溶液变红,再加入氯水后红色退去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
(3)现有可逆反应:2A(g)+2B(g)![]() C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
A.Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同
B.达到平衡时,途径Ⅱ所得混合气密度为途径Ⅰ所得混合气密度的2倍
C.达到平衡时,途径Ⅱ中C的平衡浓度大于途径Ⅰ中C的平衡浓度的2倍
(4)在恒容绝热(不与外界交换能量)条件下进行2A (g)+ B(g)![]() 2C(g)+ D(s)反应,
2C(g)+ D(s)反应,
按下表数据投料,反应达到平衡状态,测得体系压强升高。简述该反应的平衡常数与温度的变
化关系: 。
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
化学答题纸(第Ⅱ卷、共46分)
19. (每空2分、共14分)
(1) (填装置的字母), ;
(2) , ,
;
(3) , 。
20.(每空2分、共8分)
(1) 。
(2) (填选项字母)。
(3) (填选项字母)。
(4) : 。
21.(每空2分、共14分)
(1) ____________、_____________(写名称)。
(2) _________________。
(3) ___________________________________________;
_________ ____ 。
(4) ;
。
22.(每空2分、共10分)
(1) : ;
(2)(填化学式); ;
(3) 。
(4) 。
曲周县第一中学2015-2016学年高三第二次摸底考试
化学答题纸(第Ⅱ卷、共46分)
19. (每空2分、共14分)
(1) (填装置的字母), ;
(2) , ,
;
(3) , 。
20.(每空2分、共8分)
(1) 。
(2) (填选项字母)。
(3) (填选项字母)。
(4) : 。
21.(每空2分、共14分)
(1) ____________、_____________(写名称)。
(2) _________________。
(3) ___________________________________________;
_________ ____ 。
(4) ;
。
22.(每空2分、共10分)
(1) : ;
(2)(填化学式); ;
(3) 。
(4).