
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
季延中学2017届一模理科综合能力测试
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分300分,考试时间150分钟。中·华.资*源%库
可能用到的原子量: H 1 C 12 N 14 O 16 S32 Na 23 Fe 56
第Ⅰ卷(选择题共126分)
一、单项选择题(本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是最符合题意)
7.化学与生活、社会发展息息相关,下列有关说法不正确的是
A.“时气错逆,霾雾蔽日”,雾所形成的气溶胶能产生丁达尔效应
B.“青蒿一握,以水二升渍,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化
C.“熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应
D.“外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定中利用了焰色反应
8.设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A.标准状况下,22.4L己烷含有的共价键总数为19NA
B.1mol Cu与足量FeCl3溶液反应,转移的电子数为2NA
C.1L 0.1mol·L-1Na2CO3溶液中CO32-和HCO3-离子数之和为0.1NA
D.密闭容器中l.5mol H2与0.5mol N2充分反应,得到NH3的分子数为NA
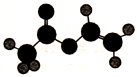 9.法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是
9.法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是
A.该化合物的名称为乙酸乙酯
B.该化合物与Br2的四氯化碳溶液不反应
C.该化合物既能发生水解反应,又能发生氧化反应
D.该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种
10.下列叙述不正确的是
A.钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
B.探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏高
C.蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置
 D.为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度
D.为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度
线下1~2cm时,改用滴管滴加蒸馏水至刻度线
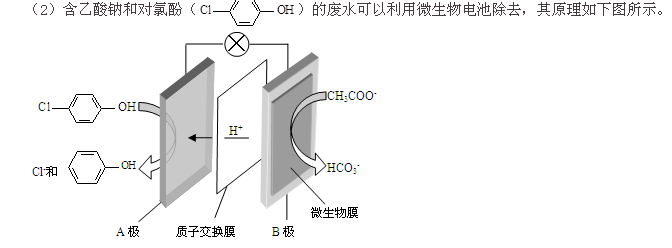
11.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如图所示。下列说法正确的是
),其原理如图所示。下列说法正确的是
![]() A.电流从B极沿导线经小灯泡流向A极
A.电流从B极沿导线经小灯泡流向A极
B.A极的电极反应式为
C.当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA
D.B极为电池的正极,发生还原反应
12.基于以下实验现象,下列实验操作和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的饱和HCOONa 溶液、CH3COONa溶液的pH | HCOONa的pH<CH3COONa的pH | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向5ml 2mol·L-1NaOH溶液中加入1ml 1mol·L-1CuSO4溶液,振荡后加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯, 然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
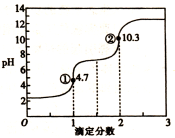 13.滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。用0.10 mol•L-1NaOH溶液滴定0.10 mol•L-1H2C2O4(草酸)溶液的滴定曲线如图所示。下到说法不正确的是
13.滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。用0.10 mol•L-1NaOH溶液滴定0.10 mol•L-1H2C2O4(草酸)溶液的滴定曲线如图所示。下到说法不正确的是
A.H2C2O4属于二元弱酸
B.若用NaOH标准溶液滴定NaHC2O4溶液,可用酚酞作指示剂
C.图中②处:c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-)>c(H+)
D.图中①处:c(Na+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
26.(14分)SO2的防治与利用对于环境保护意义重大。某小组在实验室中对SO2的性质及回收利用等相关问题进行探究。
(1)用下图装置制备纯净的SO2,发生装置中反应的化学方程式为____________________,装置的连接顺序为:a→ ______________(按气流方向,用小写字母表示)。
g f c b
e d
(2)用右图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、FeCl3溶液、淀粉-KI溶液、新制H2S溶液
| 操作步骤 | 实验现象 | 解释原因 |
| 用注射器将新制H2S溶液注入充满SO2的烧瓶 | 产生乳白色浑浊 | +4价S有①性 |
| 用注射器将②溶液注入充满SO2的烧瓶 | ③ | +4价S有还原性,反应的离子方程式为④ |
(3)工业上回收利用SO2的一种途径是:![]()
该小组在实验室探究步骤Ⅱ时,一定条件下向100mLc0mol·L-1的(NH4)2SO3溶液通入空气后,欲测定溶液中(NH4)2SO3的氧化率(α),设计了如下实验方案:向反应后的溶液中加入过量(填试剂名称),再加入足量(填化学式)溶液,将沉淀过滤、洗涤、干燥、称量,质量为mg。则α=________×100%。
27.(15分)氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一。SCR法是工业上消除氮氧化物的常用方法,反应原理为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H<0
4N2(g)+6H2O(g)△H<0
(1)氮氧化物破坏臭氧层原理为:①NO+O3![]() NO2+O2②NO2+O
NO2+O2②NO2+O![]() NO+O2
NO+O2
常温下反应①的平衡常数为K1,反应②的平衡常数为K2,则反应O3+O![]() 2O2的平衡常数K=________(用K1、K2表示)。氮氧化物在该反应中的作用是________。
2O2的平衡常数K=________(用K1、K2表示)。氮氧化物在该反应中的作用是________。
(2)SCR法除NO时,投料比一定时有利于提高NO平衡转化率的反应条件是________、________。该法可能发生副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
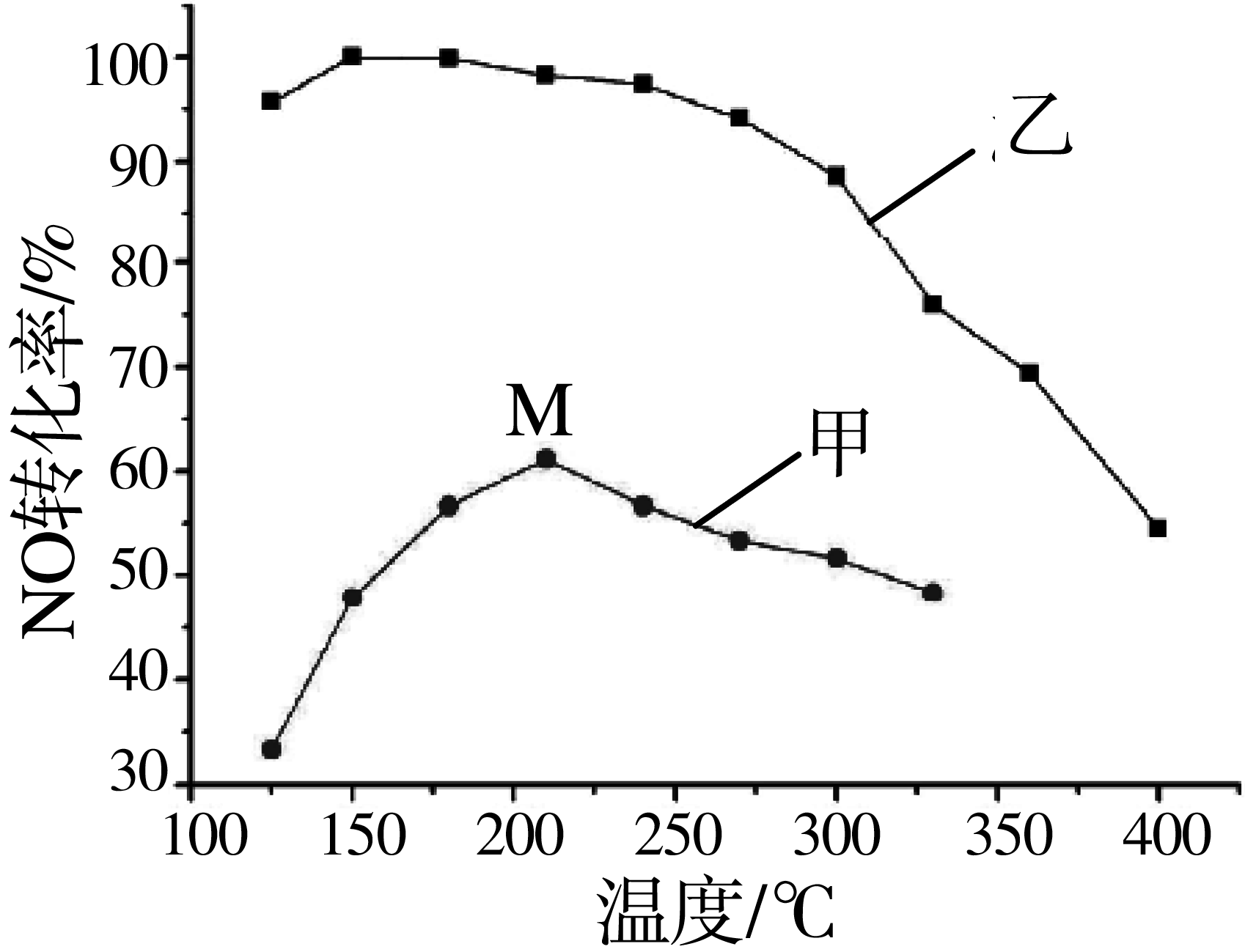 (3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
①工业上选择催化剂乙的原因是________;
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率_________(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是________。
(4)消除汽车尾气中的NO时,可用尿素还原NO,既安全又高效,且产物都是空气中含有的成分。与SCR法相比,等物质的量的尿素与氨气可消除的NO物质的量之比为________。(不考虑副反应)
28.(15分)二氧化钛(TiO2)广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用钛铁矿作原料,制取二氧化钛及绿矾,其生产流程如下:
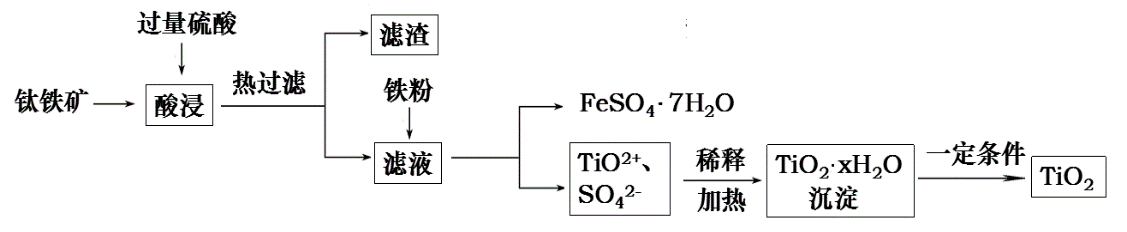
回答下列问题:
(1)FeTiO3溶于过量硫酸的离子方程式。$来&源:
(2)若向所得滤液中加入铁粉,此时0.5 L的溶液中含有2.5molTiO2+,5.75molSO42-,3mol某种阳离子和H+,则常温下其溶液的pH =。
(3)流程中生成TiO2•xH2O的离子方程式为。
(4)从溶液中获得绿矾的操作是,过滤,洗涤。过滤后得到的绿矾常用乙醇
洗涤该晶体,优点是。
(5)以TiO2为原料制取金属钛的其中一步反应为TiO2+Cl2+C→TiCl4+(),已知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为。
(6)为测定溶液中TiO2+的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3TiO2++Al+6H+=3Ti3++Al3++3H2O。过滤后,取出滤液20mL,向其中滴加2~3滴KSCN溶液作指示剂,用滴定管滴加0.2mol•L-1FeCl3溶液,当溶液出现红色且半分钟不褪色时达到滴定终点,用去了20mLFeC13溶液,则待测钛液中TiO2+的物质的量浓度是mol•L-1。
35.(15分)铁及其化合物在生产生活及科研中应用广泛。
(1)聚合硫酸铁的化学式为[![]() ]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有______个未成对电子。
]m,是常用的水处理剂。基态铁原子的核外电子排布式为___________,聚合硫酸铁中铁元素阳离子有______个未成对电子。
(2)Fe3+、Co3+与N3-、CN-等可形成络合离子。
①K3可用于检验Fe2+,配体CN-中碳原子杂化轨道类型为______,1mol3-离子中含有σ键的数目为______。
②SO4中Co的配位数为______,C、N、O的第一电离能最大的为______,其原因是____________________________________。
③已知N3-与CS2为等电子体,则N3-的空间构型为____________。
 (3)化合物FeF3熔点高于1000℃,而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的可能原因是____________。
(3)化合物FeF3熔点高于1000℃,而Fe(CO)5的熔点却低于0℃,FeF3熔点远高于Fe(CO)5的可能原因是____________。
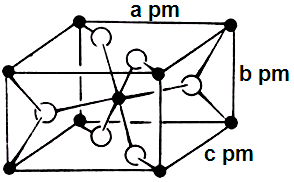
(4)氟化亚铁晶胞属于四方晶系,其长方体结构如图所示,根据
图中所示数据计算该晶体密度ρ= ______ g·cm-3。(列出计算式)
36.(15分)
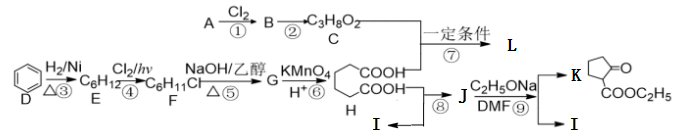 以下为合成2-氧代环戊羧酸乙酯K和聚酯L的路线:已知如下信息:
以下为合成2-氧代环戊羧酸乙酯K和聚酯L的路线:已知如下信息:
Ⅰ.链烃A可生产多种重要有机化工原料,在标准状况下的密度为1.875 g·L-1。
 Ⅱ.
Ⅱ.
请回答以下问题:
(1)A的名称是,K中含氧官能团名称为:。
(2)②的反应类型是,⑥的反应类型是。
(3)写出反应⑤、⑦的化学方程式:;
。
(4)与H官能团的种类和数目完全相同的同分异构体有种,其中核磁共振氢谱为4组峰,且峰面积之比为1:2:3:4的是(写结构简式)。
(5)利用以上合成路线中的相关信息,请写出以乙醇为原料制备![]() ,(其他试剂任选)的合成路线流程图。
,(其他试剂任选)的合成路线流程图。
化学
7. B 8. B 9. C 10. B 11. C 12. B 13. D
26.(14分)(1)H2SO4+2NaHSO3![]() 2SO2↑+2H2O+Na2SO4或H2SO4+NaHSO3
2SO2↑+2H2O+Na2SO4或H2SO4+NaHSO3![]() SO2↑+H2O+NaHSO4(2分)(漏气体符号、配平错误扣1分);b→c→g→f→d(2分)
SO2↑+H2O+NaHSO4(2分)(漏气体符号、配平错误扣1分);b→c→g→f→d(2分)
(2)①氧化(1分)②FeCl3(1分)③溶液由黄色变成浅绿色(2分)(答溶液褪色/颜色变浅也给分)④SO2+2Fe3++2H2O![]() SO42—+2Fe2++4H+(2分)(配平错误扣1分)
SO42—+2Fe2++4H+(2分)(配平错误扣1分)
(3)盐酸(1分)、BaCl2(1分)、![]() (2分)
(2分)
27.(15分)(1)K1·K2(2分)催化剂(1分)(2)降低温度、减小压强(2分)
选择合适的催化剂、控制O2用量(各1分、共2分)(提高催化剂的专一性/改良催化剂、减小O2用量/浓度、增大NH3与O2的投料比给分。)
(3)①低温下有很强的催化活性(或在较大的温度范围内有较高催化活性)(2分)
(催化剂乙的活性//效率高于催化剂甲、催化剂乙作用下NO转化率更高给1分)
②一定不是(2分)催化剂活性降低、副反应增多(任写一个)(2分)(只要答对一个合理原因就给2分。从平衡移动角度回答,得0分)(4)3:1(2分)
28.(14分)(1)FeTiO3+ 4H+== Fe2++ TiO2++2H2O(2分)(2)0(2分)
利用乙醇的挥发,除去晶体表面附着的水分,减少晶体的损失(1分)
(5)CO(2分)(6)酸式(1分)2 (2分)
35.(15分)
(1)1s22s22p63s23p63d64s2或3d64s2(1分)5(1分)
(2)①Fe2+(1分)sp(1分)12NA(2分)②6(1分)N(1分)
氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子(2分)③直线型(1分)
(3)FeF3是离子晶体,Fe(CO)5是分子晶体,离子键的作用远比分子间作用力强,故FeF3熔点远高于Fe(CO)5(2分)
(4)![]() (2分)
(2分)
![]() 36.(15分)(1)丙烯 (1分)羰基、酯基(2分)(2)取代(水解)反应(1分)氧化反应(1分)(3)(4分,每个方程式2分)
36.(15分)(1)丙烯 (1分)羰基、酯基(2分)(2)取代(水解)反应(1分)氧化反应(1分)(3)(4分,每个方程式2分)

![]()
(4) 8 (2分);(1分)
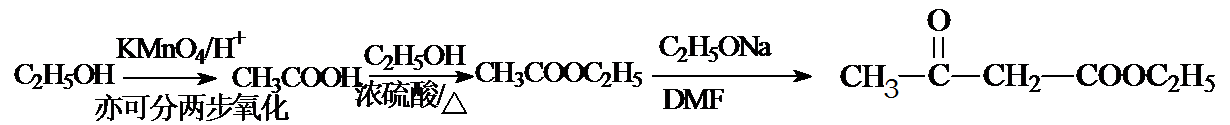 (5)(3分)
(5)(3分)