
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]()
![]() 云南省师范大学附属中学2018届高三第七次月考试卷理综
云南省师范大学附属中学2018届高三第七次月考试卷理综
化学
7.2017年CCTV-3制作了一档文物节目《国家宝藏》,全面展示了很多非常有价值的文物。从化学角度看文物,下列对文物情况的化学解释错误的是
| 选项 | 文物 | 化学知识 |
| A | 乾隆年间“各种釉彩大瓶",其纹饰是用各种彩料绘制而成的 | 形成黄金色所用彩料的主要成分是氧化铁 |
| B | 北宋《千里江山图》颜料来自于矿物质,经研磨、溶解、过滤几道工序 | 这些工序涉及的是物理变化 |
| C | 春秋时期“越王勾践剑”经历两千多年依旧锋利,被称“千年不腐” | “千年不腐” 与其所处环境几乎无氧有关 |
| D | “云梦睡虎地秦简”是在湖北出土的秦代竹筒。其中有记录保护 | 自然环境的案例日常生活中垃圾分类、电池回收等属于环保行为 |
8.下列说法不正确的是
A.炒菜时,加一点酒和醋酸能使菜味香可口
B.蔗糖在酸性条件下水解的产物互为同分异构体
C.CuSO4·5H2O可用于检验酒精中是否含有水
D.利用油脂在碱性条件下的水解,可以制甘油和肥皂
9.设NA为阿伏加德罗常数的值,下列叙述正确的是
A.0.1mol/LNaClO溶液中含有的Cl0-数为0.1NA
B.一定条件下,2molSO2和ImolO2发生反应,转移的电子数为4NA
C.1L0.1mol/L葡萄糖溶液中分子总数为0.1 NA
D.60g石英晶体中含有的Si-O键数目为4 NA
10.短周期元素X、Y、Z、W的原子序数依次增大,其原子的最外层电子数之和为14,X 与Z同主族,Y 与W同主族,且X的原子半径小于Y。下列叙述正确的是
A.简单离子半径:Y
B.W 元素的氧化物对应的水化物可能是弱电解质
C.X2Y2 加入酸性高锰酸钾溶液中,还原产物为X2Y
D.X、Z都能分别与Y 形成含非极性键的分子
11.下表各组物质之间不能通过一步反应实现如图1所示转化关系的是
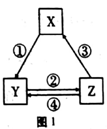
| 选项 | X | Y | Z | 对应箭头上所标数字的反应试剂 |
| A | Fe | FeCl3 | FeCl2 | ①④可用相同试剂 |
| B | Al2O3 | NaAlO2 | Al(OH)3 | 加氨水 |
| C | NO | NO2 | HNO3 | ②气体通入水中 |
| D | Cl2 | HClO | NaClO | ③加浓盐酸 |
12.某温度下,已知醋酸的电离常数Ka= 1.6×10-5,醋酸银的溶度积Ksp(CH3COOAg)= 3.7×10-3。下列有关说法正确的是
A.醋酸溶液中,c(CH3COO-)>c( H+)>c(OH-)
B.将相同浓度的CH3COOH 溶液与CH3COO Na 溶液等体积混合,所得溶液呈碱性
C.该温度下,1mol/L的醋酸溶液中,醋酸的电离度为0.4%
D.该温度下,浓度均为0.02mol/L的CH3COONa溶液和AgNO3溶液等体积混合(忽略混合后溶液体积的变化),有CH3COOAg 沉淀生成
13.下列实验、现象及有关结论不正确的是
| 选项 | A | B | C | D |
| 实验 |  | 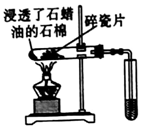 |  |  |
| 现象 | 加热铝箔,铝箔熔化却不滴落 | 石蜡油分解产生的气体能使试管中溴的四氯化碳溶液褪色 | 食盐水浸泡过的铁钉放入试管中,一段时间后,导管口形成一段水柱 | 向蔗糖中加人浓硫酸时,蔗糖变黑,体积膨胀 |
| 结论 | 氧化铝的熔点比铝的高 | 石蜡油的分解产物中含不饱和烃 | 铁钉发生吸氧腐蚀 | 浓硫酸具有吸水性和强氧化性 |
26.(14 分) NH3是一种重要的化工原料。
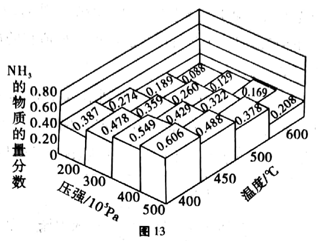
反应I: NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l) △H1=akJ/mol;
反应II :NH2Cl(aq)+HClO(aq)=NHCl(aq)v △H2=bkJ/mol;
反应III: 2NHCl2(aq) +H2O(l)=N2(g)+HClO( aq)+3HCl( aq) △H3=ckJ/mol。
①2NH3(aq)+3HClO(aq)==N2(g)+ H2O(l) △H=________kJ/mol
②已知在水溶液中NH2Cl较稳定,NHCl2不稳定易转化为氮气。在其他条件不变的情况下,改变![]() 对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。
对溶液中次氯酸钠去氨氮效果与余氯(溶液中+1价氯元素的含量) 的影响如图l4所示。a点之前溶液中发生的主要反应为_______(填序号)。
A.反应I、I I B.反应I
③除氨氮过程中最佳的![]() 值约为______________。
值约为______________。
27.(15分) 钼是一种重要的过渡金属元素,通常用作合金及不锈钢的添加剂,可增强合金的强度、硬度、可焊性等。钼酸钠晶体(Na2MoO4·2H2O) 可作为无公害型冷却水系统的金属腐蚀抑制剂,如图15 是化工生产中以辉钼矿(主要成分为硫化钼MoS2) 为原料来制备金属钼、钼酸钠晶体的主要流程图。
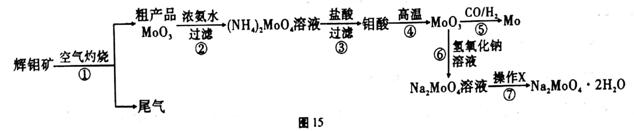
回答下列问题:
| 温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
| 析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | Na2MoO4 | ||||||
| 溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
28.(14分)“结晶玫瑰”是具有强烈玫瑰香气的结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。其化学名称为“乙酸三氯甲基苯甲酯”,目前国内工业上主要使用以下路径来合成结晶玫瑰:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶政瑰”。
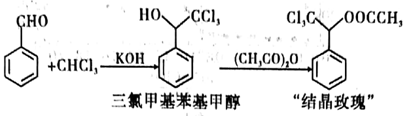
已知:
| 三氯甲基苯基甲醇 | 相对分子质量: 225.5。无色液体。不溶于水,密度比水大,溶于乙醇 |
| 乙酸酐 | 无色液体。与水反应生成乙酸,溶于乙醇 |
| “结晶玫瑰” | 相对分子质量: 267.5。白色晶体。熔点: 88℃。不溶于水,溶于乙醇 |
具体实验步骤如下:
I.由苯甲醛和氯仿合成三氯甲基苯基甲醇。
步骤一: 装置如图16所示。依次将苯甲醛、氯仿加入三颈烧瓶中,仪器A 中加入KOH和助溶剂。滴加A中试剂并搅拌,开始反应并控制在一定温度下进行。
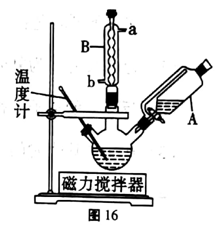
步骤二: 反应结束后,将混合物依次用5%的盐酸、蒸馏水洗涤。
步骤三: 将洗涤后的混合物蒸馏,除去其他有机杂质,加无水琉酸镁,过滤。滤液即为粗制三氯甲基萃基甲醇。
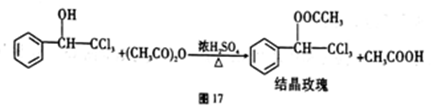
Ⅱ.三氯甲基苯基甲醇与乙酸酐发生乙酰化反应制得“结晶玫瑰”。
步骤四: 向另一三颈瓶中加入制备的三氯甲基苯基甲醇、乙酸酐,并加入少量浓硫酸催化反应,加热控制反应温度在90℃~110℃之间。
步骤五: 反应完毕后,将反应液倒入冰水中,冷却结晶获得“结晶玫瑰”。
请回答下列问题:
35.【化学-选修3: 物质结构与性质】(15分)
20世纪末,科学家发现海底存在大量天然气水合物晶体。在天然气水合物晶体中,有甲烷、氧气、二氧化碳、硫化氢、稀有气体等,它们在水合物晶体里是装在几个水分子构成的笼内,因而又称为笼状化合物。
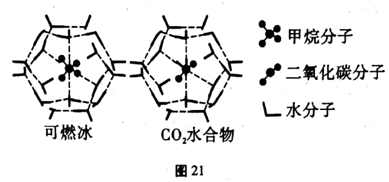
| 物质 | 分子直径(nm) | 分子与H2O 的结合能(kJ/mol) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
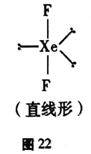
36.【化学-选修5:有机化学基础】(15分)
聚合物F筒称PETA,可利用于新型的普适无卤阻燃体系。图23是以A为原料合成聚合物F的路线:
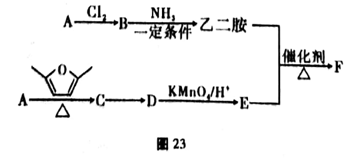
已知: ①A为与氢气的相对密度是14的烃;
②![]() ;
;
③D、E均为芳香化合物,它们的核磁共振氢谱显示均为2组峰。
回答下列问题:
| 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| A | C | D | B | B | C | D |
26.(每空2分,共14分)
(1)①减小 ②D ③41%
(2)2NH3 − 6e− + 6OH−=N2 + 6H2O
(3)①![]() ②B ③1.5
②B ③1.5
27.(除特殊标注外,每空2分,共15分)
(1)+6(1分)
(2)MoO3+2OH−=![]() +
+![]()
(3)2MoS2+7O22MoO3+4SO2
(4)蒸发浓缩、冷却结晶 C
(5)9︰1
(6)Lix(MoS2)n−xe−=nMoS2+xLi+
(7)28.8g
28.(除特殊标注外,每空1分,共14分)
(1)恒压滴液漏斗 b
(2)除去未反应完的KOH C(2分)
(3)除水干燥 低 若不干燥,乙酸酐会与水反应生成乙酸,使“结晶玫瑰”的合成反应平衡逆向移动,产品产率降低(合理均给分)(2分)
(4)防止放热过快而迸溅(2分) 油浴加热(2分)
(5)80%
36.(除特殊标注外,每空2分,共15分)
(1)碳碳双键(1分) 1,2−二氯乙烷
(2)取代反应(1分)
(3)![]()
(4)H2O(1分)
(5)![]() ;缩聚反应(1分)
;缩聚反应(1分)
(6)10
(7)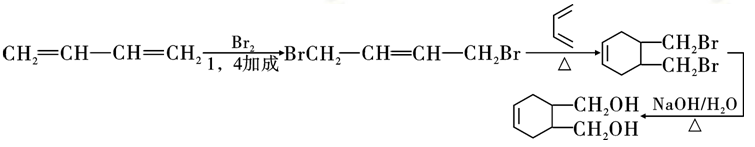 (3分)
(3分)