
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
阳八中2017届高三实验班第六次月考试卷资*源%库
理科综合(试题卷)
注意事项:
1.本卷为衡阳八中高三实验班第六次月考试卷,分两卷。其中共31题,满分300分,考试时间为150分钟。
2.考生领取到试卷后,应检查试卷是否有缺页漏页,重影模糊等妨碍答题现象,如有请立即向监考老师通报。开考15分钟后,考生禁止入场,监考老师处理余卷。
3.请考生将答案填写在答题卡上,选择题部分请用2B铅笔填涂,非选择题部分请用黑色0.5mm签字笔书写。考试结束后,试题卷与答题卡一并交回。
第I卷 选择题(每题6分,共126分)
本卷共21题,每题6分。其中物理部分为不定项选择题,全部选对得6分,部分选对得3分,错选,多选不得分。化学部分和生物部分后面所给的四个选项中,只有一个是正确的。
9.设NA为阿伏加德罗常数的值,下列说法不正确的是
A.4.6g金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA
B.1L 0.5 mol/L的FeCl3溶液充分水解后,所得Fe(OH)3胶粒的数目为0.5NA
C.2.0g H218O与D2O的混合物中所含中子数为NA
D.1L含NA个Al3+的Al(NO3)3液中,NO3﹣物质的量浓度大于3 mol/L
10.已知常温下在溶液中可发生如下两个离子反应Ce4++Fe2+=Fe3++ Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Fe2+、Ce3+、Sn2+ 三种离子的还原性最强和最弱的离子分别是
A.Sn2+ 和Ce3+ B.Sn2+ 和Fe2+ C.Ce3+和Sn2+ D.Fe2+和Ce3+
11.在一定温度下,容积固定的密闭容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
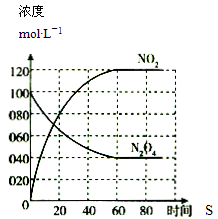
A.若温度升高,混合气体的颜色变深
B.在该温度下反应2NO2(g) ![]() N2O4(g)的平衡常K为25/9
N2O4(g)的平衡常K为25/9
C.反应达平衡后,将反应容器的容积减少一半,平衡向正反应方向移动
D.反应达平衡后,向此容器中通入NO2气体,则c(NO2)增大
12.短资*源%库周期主族元素X、Y、Z、W的原子序数依次增大,原子半径:r(W)>r(Y)>r(Z)>r(X)。X与W同主族,Z原子最外层电子数是其内层电子总数的3倍,Z原子的核电荷数等于X、Y原子核电荷数之和。下列说法正确的是
A.元素Z、W的简单离子的电子层结构不同
B.元素Y的简单气态氢化物的热稳定性比Z的强
C.仅由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性
D.化合物X2Z2与W2Z2所含化学键类型完全相同
13.向含Na+、Al3+、Fe3+、Fe2+、Cl﹣、SO42﹣的水溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,所得溶液与起始溶液相比,上述离子数目没有变化的有
A.2种 B.3种 C.4种 D.5种
14.下列反应中属于加成反应的是
A.CH4+Cl2![]() CH3Cl+HCl B.CH2=CH2+Br2→CH2BrCH2Br
CH3Cl+HCl B.CH2=CH2+Br2→CH2BrCH2Br
C.2CH3CH2OH+O2![]() 2CH3CHO+2H2O D.
2CH3CHO+2H2O D.![]()
15.下列实验方案中,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别溴蒸气和NO2 | 分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸汽 |
| B | 证明氧化性:H2O2比Fe3+强 | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| C | 证明盐类水解是吸热反应 | 在醋酸钠溶液中滴入酚酞试液,加热后红色加深 |
| D | 证明难溶物存在沉淀溶解平衡 | 往黄色固体难溶物PbI2加水中振荡,静置取上层清液加入NaI固体产生黄色沉淀 |
第II卷 非选择题(共174分)
26.(本题满分18分)我国有广阔的海岸线,海水综合利用大有可为.海水中Br﹣含量为65mg•L﹣1,从海水中提取溴的工业流程如下:
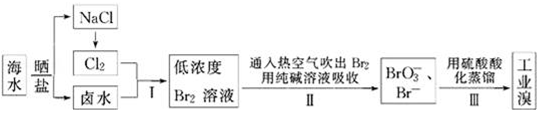
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是: .
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的 (填序号).
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
Br2+ CO32﹣═ BrO3﹣+ Br﹣+ CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴蒸气与二氧化硫水溶液反应的离子方程式: .
(5)实验室从溴水中分离出溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是 (填序号).
A.乙醇 B.四氯化碳 C.裂化汽油 D.苯
(6)用上述流程制得含Br265%的工业溴1t,至少需要海水 m3.
(7)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的离子方程式: .
27.(本题满分18分)工业生产中产生的SO2、NO直接排放将对大气造成严重污染,利用电化学原理吸收SO2和NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如下(Ce为铈元素).
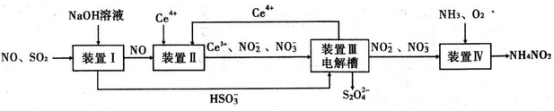
请回答下列问题.
(1)装置Ⅱ中NO在酸性条件下生成NO2﹣的离子方程式 .
(2)含硫各微粒(H2SO3、HSO3﹣和SO32﹣)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω与溶液pH的关系如图1所示.
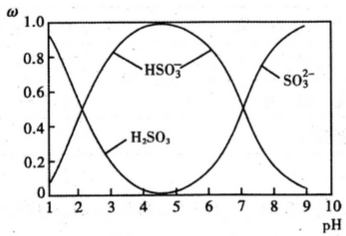 图1
图1
 $来&源:图2
$来&源:图2
①下列说法正确的是 (填标号).
A.pH=7时,溶液中c(Na+)<c(HSO3﹣)+c(SO32﹣)
B.由图中数据,可以估算出H2SO3的第二级电离平衡常数Ka2≈10﹣7
C.为获得尽可能纯的 NaHSO3,应将溶液的pH控制在 4~5为宜
D.pH=9时的溶液中c(OH﹣)=c(H+)+c(HSO4﹣)+c(H2SO4)
②若1L1mol/L的NaOH溶液完全吸收13.44L(标况下)SO2,则反应的离子方程式为 .
③取装置Ⅰ中的吸收液vmL,用cmol/L的酸性高锰酸钾溶液滴定.酸性高锰酸钾溶液应装在 (填“酸式”或“碱式”)滴定管中,判断滴定终点的方法是 .
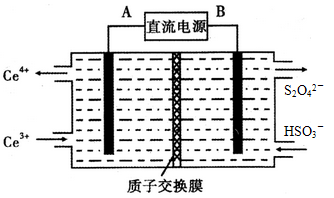
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图2所示.
图中A为电源的 (填“正”或“负”)极.右侧反应室中发生的主要电极反应式为 .
(4)已知进人装置Ⅳ的溶液中NO2﹣的浓度为0.4mol/L,要使1m3该溶液中的NO2﹣完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的 O2的体积为 L.
28.(本题满分22分)乙二酸(HOOC﹣COOH,可简写为H2C2O4)俗称草酸,在100℃开始升华,157℃时开始分解.
(1)探究草酸的酸性
①已知:25℃H2C2O4 的电离常数 K1=5.4×102,K2=5.4×105;H2CO3的电离常数 K1=4.5×107,K2=4.7×1011则下列化学方程式正确的是 (填选项序号,下同)
A.H2C2O4+CO32=HCO3+HC2O4
B.HC2O4+CO32=HCO3+C2O42
C.H2O+CO2+C2O42=HC2O4+HCO3
D.C2O42+CO2+H2O=H2C2O4+CO32$来&源:
②向1L 0.02mol/L H2C2O4溶液中滴加1L 0.01mol/L NaOH溶液.混合溶液中c(H+)>c(OH﹣),下列说法中正确的是 .
A.c(H2C2O4)>c(HC2O4)
B.c(Na+)+c(H+)=2c(C2O42)+c(HC2O4)+c(OH﹣)
C.c(OH﹣)=c(H+)+2c(H2C2O4)+c(HC2O4)
D.c(H2C2O4)+c(C2O42)+c(HC2O4)=0.02mol/L
(2)用酸性KMnO4溶液滴定含杂质的Na2C2O4样品(已知杂质不与KMnO4和H2SO4溶液反应).
实验步骤:
准确称取1g样品Na2C2O4固体,配成100mL溶液,取出20.00mL于锥形瓶中.再向瓶中加入足量稀H2SO4溶液,用0.016mol/L高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL.
(已知:5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O)
①高锰酸钾溶液应装在 滴定管中.(填“酸式”或“碱式”)资*源%库
②滴定至终点时的实验现象是: .
③下列操作可能使测量结果偏高的是 ;
A.盛装的Na2C2O4的滴定管没润洗
B.盛装高锰酸钾溶液的滴定管滴定前尖嘴处有气泡,滴定后气泡消失
C.读数时滴定前仰视,滴定后俯视
D.锥形瓶中残留少量水
④计算样品中Na2C2O4的纯度 .
衡阳八中2017届高三实验班第六次月考理科综合参考答案
| 题号 | 9 | 10 | ||||
| 答案 | B | A | ||||
| 题号 | 11 | 12 | 13 | 14 | 15 | |
| 答案 | C | C | A | B | B | |
26.
(1)富集溴元素;
(2)C;
(3)3;3;1;5;3;
(4)SO2+Br2+2H2O=4H++2Br﹣+SO42﹣;
(5)BD;
(6)2.0×104;
(7)SO2+Br2+2H2O=4H++2Br﹣+SO42﹣.
27.
(1)NO+H2O+Ce4+=Ce3++NO2﹣+2H+;
(2)①ABC;
②3SO2+5OH﹣=2SO32﹣+HSO3﹣+2H2O;
③酸式;滴入最后一滴溶液呈紫红色且半分钟颜色不变;
(3)正;2HSO3﹣+2H++2e﹣=S2O42﹣+2H2O;
(4)4480.
28.(1)①B;
②B;
(2)①酸式;
②无色变为紫色(紫红色),且半分钟内不褪色;
③B;
④67%.