
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 甘肃省张掖市2018届高三第一次质量检测
甘肃省张掖市2018届高三第一次质量检测
理综化学
可能用到的相对原子质量:H-1 C-12 N-14 0-16 F-19 C1-35.5 K-39 Zn-65
一、选择题:本题共13小题,每小题6分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7.“保护环境”是我国的基本国策。下列做法不应该提倡的是( )
A.大力推广燃煤发电以满足工业发展的用电需求
B.实施化石燃料脱硫脱硝技术,减少大气污染物的排放
C.加强生活污水的除磷处理,遏制水体的富营养化
D.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
8.下列关于有机物的说法中错误的是( )
A.以苯甲醇为原料可制取苯甲酸B.苯不能与溴水发生加成反应
C.糖类、油脂和蛋白质都可水解D.分子式为C5H12O的醇共有8种结构
9.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.1.0mol·L-1的CH3COONa溶液中所含CH3COO-的数目一定小于NA
B.46g二氧化氮(NO2)所含的电子数为23NA
C.标准状况下,2.24 LCCl4中所含C-Cl键的数目为0.2NA
D.将0.1mol H2和0.2molI2充入密闭容器中充分反应后,生成HI的分子数为0.2NA
10.短周期元素a、b、c、d的原子序数依次增大,由以上四种元素组成的一种化合物m在加热时完全分解为三种产物,其中一种产物n是能使湿润的红色石蕊试纸变蓝的气体,另一种产物q是能使品红溶液褪色的气体。下列说法正确的是( )
A.原子半径:a
B.m、n、q三种物质中均含有非极性共价键
C.a、b、c三种元素形成的化合物一定会抑制水的电离
D.d的最高价氧化物对应的水化物是强酸
11.一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是( )
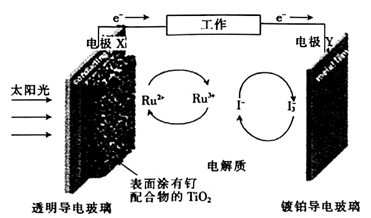
A.镀铂导电玻璃的作用是传递I-B. 电池工作时,光能转变为电能,X 为电池的正极
C.电解质溶液中发生反应:2Ru3++3I-=2Ru2++I3-D.电池的电解质溶液中I-和I3-的浓度均不断减小
12.25 ℃时,体积均为20 mL、浓度均为0.1mol·L-1的两种酸HX、HY 分别与0.1mol·L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是( )
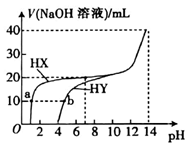
A.Ka(HY)的数量级约为10-3B.a点c(X-)>b点c(Y-)
C.HX发生反应的离子方程式为HX +OH-=X-+H2OD.pH=7时,两种反应后的溶液中c(Y- )>c(X-)
13.下列实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通人紫色石蕊试液中,观察溶液颜色查化 | 证明二氧化硫具有漂白性 |
| B | 向2mL1mol·L-1NaOH溶液中先加入3滴1mol·L-1 FeCl3溶液.再加入3滴1mol·L-1MgCl2溶液 | 证明 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2 分解速率的影响 |
| D | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴含NaClO的“84”消毒液,观察红色褪色快慢 | 证明随溶液ph减小,“84”消毒液的氧化能力增强 |
26.(15 分)纳米碳酸钙是一种广泛应用于塑料、食品、医药、饲料等行业的重要无机填料。以磷石膏钙渣为原料制取高品质纳米碳酸钙的工艺流程如下:
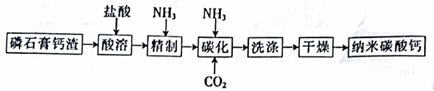
已知某磷石膏钙渣的主要成分及其含量如下表所示。
| CaO | P2O5 | SO3 | Fe2O3 | Al2O3 | SiO2 | 烧失量 |
| 47.70% | 1.60% | 1.77% | 0.041% | 0.0027% | 9.85% | 37.69% |
请回答下列问题:
(1)对磷石膏钙渣进行醋溶的目的是获得机制CaCl2溶液,为了提高溶出率,可以采取的措施
有 (填字母)。
A.粉碎磷石膏钙渣 B.增大盐酸浓度 C.适当降低温度 D.缩短酸溶时间
(2)为了探究醋溶的工艺条件,称取6 份各50g磷石膏钙渣,分别用不同浓度盐酸进行溶解,反应时间为30 min,测得滤液中钙溶出率的结果如图所示,最适宜的盐酸浓度为 。
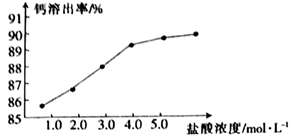
(3)精制是向粗制CaCl2溶液中通入氨气,控制溶液的pH,主要除去 (填金属阳离子)。
(4)碳化时,先将精制CaCl2溶液稀释至一定体积,控制反应温度以及NH3和CO2 的通入量,此过程中,通入气体有先后顺序,应先通入气体的化学式 (填化学式);碳化时发生反应的化学方程式为 。
(5)把CaCO3浊液滴入1.0mol·L-1 的Na2SO3溶液中,能否产生CaSO3沉淀? 。若不能,说明原因;若能,请从定量的角度简述判断依据: 。
[已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9
(6)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级: 。
27.(14 分)镁、硫、氮的化合物在工业上用途非常广泛。
(1)硝酸厂尾气中含有大量的NO,可用氢气催化还原法除去NO,发生的主要反应如下:
2NO(g)+4H2(g)+O2(g)=N2(g)+4H2O(g) △H=-1143 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1
则2NO(g)+2H2(g)=N2(g)+2H2O(g) △H= kJ·mol-1。
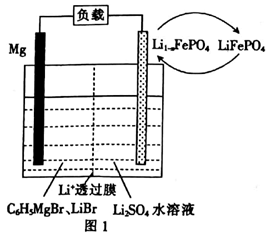
(2)一种镁一锂双离子二次电池的装置如图1所示。
①放电时, Mg 电 极 为 (填“ 正极”或“负极” ), Li +迁 移 至 (填“正极区”或“负极区”)。
②充电时,阳极的电极反应式为 。
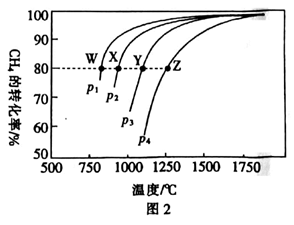
(3)在一定条件下,反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)平衡时CH4的转化率与温度和压强的关系如图2所示。
①图中p1、p2、p3、p4 代表不同压强,压强最大的是 。该反应的△H (填“>"“<”或“=”下同)0。
②压强为p4时,在Y点:v(正) v(逆)。
③图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、k3、K4由大到小的顾序为 。
28.(14 分)实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2→CCl3CHO+5HCl可能发生的副反应是C2H5OH+HCl→C2H5Cl+H2O。某探兖小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。回答下列问题:
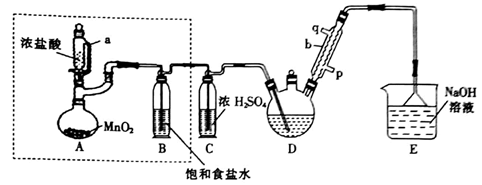
(1)仪器a的名称是 。
(2)装置A中发生反应的离子方程式为 。
(3)仪器b中冷凝水从_(填“p”或“q”,下同)口进, 口出。
(4)若撤去装置B,对实验的影响是 。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是 。
(6)已知:CCl3CHO+OH-→CHCl3+HCOO- ;
HCOO-+I2-=H++2I-+CO2↑;
I2+2S2O32-=2I-+S4O62-。
称取0.40g产品,配成待测溶液,加入20.00mL0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00mL。滴定时所用指示剂是 ,达到滴定终点的现象是 ,测得产品的纯度为 。
35.[化学——物质结构与性质](15分)
钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为 ;K、F、Zn的电负性从大到小的顺序为 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与佛点均比锌高,其原因是 。
(3)OF2分子的几何构型为 ,中心原子的杂化类型为 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3 中除σ键外,还存在 ;与O3-互为等电子体的分子为 (任 写一种 )。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
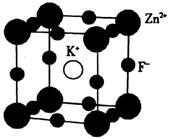
①晶胞中Zn2+的配位数为 个。
②晶胞中紧邻的两个F-间的距离为 (列出算式即可)nm。
③该晶体的密度为 (列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
36.[化学——有机化学基础](15 分)
双-(对烷氧基苯甲酸)-2,3-二氯-1,4-苯二酚酯(G)是一种新的液晶化合物,在液晶显示领城里有广泛的应用,其合成路线如下:
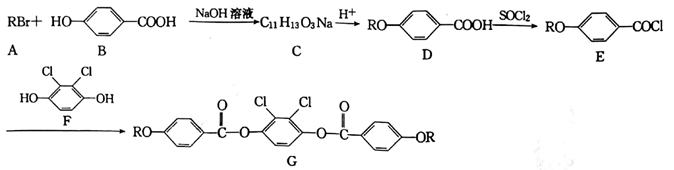
已知:R为烷烃基,D的核磁共振氢谱为四组峰,且峰面积之比为9∶2∶2∶1。
回答下列问题:
(1)A的结构简式为 。
(2)B的化学名称为 。
(3)A 与B生成C的化学方程式为 。
(4)由E生成G的反应类型为 。
(5)G 的分子式为 。
(6)H是D的同分异构体,H的苯环上只有两个对位的取代基,H可与FeCl3溶液发生显色反应,且能发生水解反应和银镜反应,则H共有 种;其中核磁共振氢谱为六组峰,且峰面积之比为
1∶2∶6∶2∶2∶1的结构简式为 。

7-10 ACBD 11-13 CBD
26.(1)AB(2 分)
(2)4.0 mol·L-1 (填4.0 mol·L-1左右均可)(2分)
(3)Fe3+、Al3+(2 分)
(4) NH3( 1分);CaCl2+H2O+2NH3+CO2=CaCO3↓+2NH4Cl (2分)
(5)能(1分);由![]() =50 可知,当CaSO3与CaCO3 的混合液中c(SO32-)>50c(CO32-)时.即发生由CaCO3向CaSO3的转变(3分)
=50 可知,当CaSO3与CaCO3 的混合液中c(SO32-)>50c(CO32-)时.即发生由CaCO3向CaSO3的转变(3分)
(6) 取少最样品和水混合形成分散系.用一束光照射,若11现一条光亮的通路,则是纳米级.否则不是(2 分)
27.(1)-659(2分)
(2)①负极(1分);正极区(1分)
②LiFePO4-xe-=Li1-xFePO4+xLi+ (2分)
(3)①p4(2 分);>(2 分)
②<(2 分)
③K4>K3>K2>K1 (2 分)
28.(1)(恒压)分液漏斗(1分)
(2)MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O( 2分)
Mn2++Cl2↑+2H2O( 2分)
(3)p(1分);q(1分)
(4)会有氯化氢杂质与乙醇反应,生成氯乙烷。导致三氯乙醛的纯度降低(2 分)
(5)停止对A加热或控制滴加盐酸的量(2分)
(6)淀粉溶液(1分);蓝色变为无色,且半分钟内不变色(2分);66.4%(或66.375%)(2分)
35.[化学——物质结构与性质]
(1)3d104s2(1分); F>Zn>K(2分)
(2)锌的原子半径较大,金属键较弱(2 分)
(3)V形(1分);sp3(1分)
(4)离子键和π键(2分);ClO2(或其他合理答案)(1分)
(5)①6(1分)
②![]() ×0.4058(2 分)
×0.4058(2 分)
③![]() (2 分)
(2 分)
36.[化学——有机化学基础]
(1)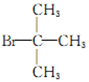 ;(2 分)
;(2 分)
(2)对羟基苯甲酸(或4-羟基苯甲酸)(2分)
(3)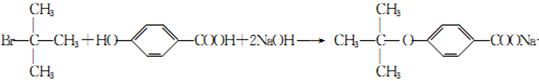 +NaBr+2H2O(3 分)
+NaBr+2H2O(3 分)
(4)取代反应(1分)
(5)C28H28Cl2O5(2 分)
(6)12(2 分);  、
、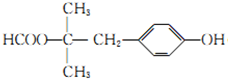 (写出一个得2分,两个全写对得3 分)
(写出一个得2分,两个全写对得3 分)