巴市中学2015-2016学年第一学期10月月考试卷高一年级 化学试题
试卷类型:A 出题人:王艳红
说明:1.本试题分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.本试题满分100分,考试时间90分钟。
附可能用到的相对原子质量:
H 1 He 4 C 12 N 14 O 16 S 32 Cl 35.5 Ca 40 Na 23
Fe 56 Ba 137 Cu 64
第Ⅰ卷 选择题(共55分)
- 单项选择题(每题2分,共2×20=40分)
- 下列分离物质的方法中,根据沸点不同进行分离的是
A.蒸馏 B.萃取 C.重结晶 D.蒸发 - 运输汽油的车上,贴有的危险化学品标志是
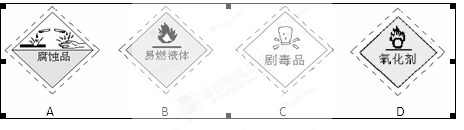
- 容量瓶上需标有以下六项中的①温度②浓度③容量④压强⑤刻度线⑥酸式或碱式
A.②④⑥B.③⑤⑥C.①②④D.①③⑤ - 萃取碘水中的碘,可用的萃取剂是 ①四氯化碳 ②苯 ③酒精
A.只有① B.①和② C. ①和③ D. ①②③A - 2molCl2和2molCO2相比较,下列叙述中正确的是
A.分子数相等B.原子数相等C.体积相等D.质量相等 - 实验中的下列操作正确的是
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B.Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 - 下列叙述正确的是
A.1 mol H2O的质量为18g/molB.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4L - 用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是( )
A.实验使用的主要仪器是分液漏斗
B.碘在四氯化碳中的溶解度比在水中的溶解度大
C.碘的四氯化碳溶液呈紫红色
D.分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出 - 下列有关阿伏加德罗常数(NA)的说法错误的是( )
A.32 g O2所含的原子数目为NA
B.0.5 mol H2O含有的原子数目为1.5 NA
C.1 mol H2O含有的H2O分子数目为NA
D.0.5 NA个氧气分子的物质的量是0.5 mol - 气体的体积主要由以下什么因素决定的:①气体分子的直径 ②气体物质的量的多少③气体分子间的平均距离 ④气体分子的相对分子质量
A.①② B.①③ C.②③ D.②④ - 实验室中需要配制1mol/L的NaCl溶液970mL,配制时应选用的容量瓶的规格是
A.950mL 容量瓶 B.500mL容量瓶
C.1000mL 容量瓶 D.任意规格的容量瓶 - 能够用来鉴别BaCl2 、NaCl 、Na2CO3三种物质的试剂是( )
A.AgNO3溶液 B.稀硫酸 C.稀盐酸 D.稀硝酸 - 有一种气体的质量是14.2g,体积是4.48升(标况),该气体的摩尔质量是 ( )
A.28.4B.28.4g·mol-1C.71D.71g·mol-1 - 下列有关气体摩尔体积的描述中正确的是( )
A.单位物质的量的气体所占的体积叫做气体摩尔体积
B.通常状况下的气体摩尔体积约为22.4L
C.标准状况下的气体摩尔体积约为22.4L
D.相同物质的量的气体摩尔体积也相同 - 在一定条件下,2体积XY3气体分解生成1体积Y2和2体积气态化合物甲。则甲的化学式为
A.XY B.XY2C.XY3D.X2Y3 - 关于2mol CO2的叙述中,正确的是
A.体积为44.8L B.质量为88g
C.分子数为6.02×1023D.含有4mol原子 - 配制2L 1.5mol/LNa2SO4溶液,需要固体Na2SO4( )
A.213g B.284g C.400g D.426g - 0.5mol Na2SO4中( )
A.含0.5个Na2SO4分子 B.含3.01×1023个SO42-
C.含0.5molNa+D.含1mol氧原子 - 将50ml 0.5 mol/LNaOH溶液加水稀释到500ml,稀释后溶液中NaOH的物质的量浓度为
A.0.5mol/L B. 0.05mol/L C.0.04 mol/L D. 0.03 mol/L - 含相同分子数的H2O和NH3具有相同的( )
- 体积 B. 原子个数 C.质量 D. 物质的量
二、单项选择题(每小题3分,共3×5=15分)
- 瓦斯中甲烷与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积比为( )
A.1:2 B.1:4 C.2:1 D.1;1 - 在相同的温度和压强下,二氧化碳和笑气(化学式为N2O)的体积相同,则下列它们的( )一定相同。
(1)分子数 (2)原子数 (3)密度 (4)质量 (5)物质的量
A.只有(1)(5) B.只有(1)(2)(4)(5)
C.只有(2)(3)(4)(5) D.(1)(2)(3)(4)(5) - 下列各组物质中,所含分子数相同的是( )
A.10g H2和10g O2 B.5.6LN2(标准状况)和11gCO2
C.9g H2O和1mol Br2 D.224ml H2(标准状况)和0.1mol N2 - 下列溶液中的Cl-离子的物质的量浓度与50mL1mol/LFeCl3溶液中的Cl-离子的物质的量浓度 相同的是 ( )
A.150mL1 mol/L NaCl溶液 B.75mL2 mol/L NH4Cl溶液
C.150mL3 mol/L KCl溶液 D.75mL3 mol/L AlCl3溶液 - 关于0.1 mol·L-1Na2CO3溶液的叙述错误的是
- 0.5 L该溶液中钠离子的物质的量浓度为0.2 mol·L-1
- 1 L该溶液中含Na2CO3的质量为10.6 g
- 从1 L该溶液中取出100 mL,则取出溶液中Na2CO3的物质的量浓度为0.01 mol·L-1
D .取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01 mol·L-1
第Ⅱ卷 非选择题 (共45分)
- 填空题(共31分)
- (共13分)
- 混合物分离的方法在生产、生活和科学实验中有着广泛的应用。请指出下列做法中分别应用了哪些分离方法?
A、分液 B、过滤 C、萃取 D、蒸馏 E、蒸发结晶 F、加热分解
①除去Ca(OH)2 溶液中悬浮的 CaCO3 ; ②从碘水中提取碘 ;
③用自来水制取蒸馏水 ; ④分离植物油和水 ;
⑤海水淡化 ; ⑥除去 KCl 中少量 KClO3;
⑦熬煮中药 ; ⑧用海水晒盐 。
- 某同学要配制100mL 1mol·L-1NaCl溶液,配制时需选用的仪器主要有 , , , , 和试剂瓶。
- (共18分)
(1)在同温同压下,等质量的CO和CO2,其体积之比为 ,电子数之比为 ,密度之比为 。
(2)9.5gMgCl2固体溶于水配成500mL溶液,其浓度为 mol·L-1,从中取出100mL溶液,其中Cl-的浓度为 mol·L-1;再把取出的溶液加水稀释成500mL,则此时MgCl2溶液的浓度为 mol·L-1。
(3)某金属氯化物MCl227g ,含有0.40molCl- ,则该氯化物的物质的量为_ _____,摩尔质量为 ,金属M的相对原子质量为 。
四、实验题(14分) - 用密度为1.84g/mL,质量分数为98%的浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④转移 ⑤洗涤 ⑥定容 ⑦摇匀
(1)所需浓硫酸的体积是 。
(2)第③步实验的操作是 。
(3)第⑥步实验的操作是 。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用字母填写a.偏高 b.偏低 c.无影响)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.量取浓硫酸时仰视量筒上的刻度取用浓硫酸
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(5)本实验最浪费时间的地方是将稀释后的硫酸冷却至室温,为了节约时间,简单易行的加
快稀硫酸冷却的方法是_______________________________________。
巴市一中2015~2016学年第一学期 10月考试
高一化学答题卡
姓名_________________
准考证号 | 缺考
违纪 |
| 注意事项
1.答题前,考生先将自己的姓名、准考证号填写清楚,并认真在规定位置贴好条形码。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米及以上黑色字迹的签字笔书写,要求字体工整,笔迹清楚。
3.严格按照题号在相应的答题区域内作答,超出答题区域书写的答案无效;
4.保持卡面清洁,不装订,不要折叠,不要破损。 | | 填涂样例 | 正确填涂
错误填涂
 |
|
| |
第I卷. 选择题(共55分,其中1-20每小题2分,21-25每小题3分)
1abcd
2abcd
3abcd
4abcd
5abcd | 6abcd
7abcd
8abcd
9abcd
10abcd | 11abcd
12abcd
13abcd
14abcd
15abcd | 16abcd
17abcd
18abcd
19abcd
20abcd |
21abcd
22abcd
23abcd
24abcd
25abcd | | | |
第II卷. 非选择题(共45分)
26.(13分)
(1)① ② ③ ④
⑤ ⑥ ⑦ ⑧
(2),,,, |
27.(18分)
(1)
(2)
(3) |
28.(14分)
(1)
(2)
(3)
(4)A. B. C. D. E. F.
(5) |
巴市中学2015-2016学年第一学期10月份月考高一年级化学试题答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | A | B | D | B | A | D | C | D | A | C | C | B | D |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答案 | A | B | B | D | B | B | D | A | D | B | C | C | |
26.(1) B; C; D; A; D; F; C; E
(2) 100ml容量瓶, 托盘天平,烧杯, 玻璃棒, 胶头滴管
27.(1) 11:7, 1:1, 7:11
(2) 0.2 0.4 0.04
(3) 0.2 mol ,135 g/mol ,64
28.(1)16.3mL ;(2)将浓硫酸沿烧杯内壁缓缓注入水中,边倒边搅拌;(3)定容,沿玻璃棒往容量瓶中加蒸馏水至刻度线1-2cm处,改用胶头滴管滴至凹液面与刻度线水平相切;(4)b;c;b;a;b;b;(5)把烧杯放入盛有冷水的水槽中

