
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016-2017学年度第一学期
高一级化学科期末考试试题
本试卷分选择题和非选择题两部分,共8页,满分100分。考试用时90分钟。
注意事项:1、答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和学号填写在答题卡和答卷密封线内相应的位置上,用2B铅笔将自己的学号填涂在答题卡上。
2、选择题每小题选出答案后,有2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案;不能答在试卷上。
3、非选择题必须用黑色字迹的钢笔或签字笔在答卷纸上作答,答案必须写在答卷纸各题目指定区域内的相应位置上,超出指定区域的答案无效;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4、考生必须保持答题卡的整洁和平整。
本试题可能用到的相对原子质量是:H-1,C-12,N-14,O-16,Na-23,
S-32, Fe-56, Zn-65
第一部分 选择题
一.单选题(15小题,每小题只有一个选项符合题意,各3分,共45分)
1、化学与生产、生活密切相关。下列物质用途不正确的是
D. 将足量Na2O2投入FeCl2溶液中, 有气泡产生并最终得到白色沉淀
8、同温同压下,等物质的量的SO2和CO2相比较,下列叙述正确的是
① 体积比为 1︰1 ② 密度比为 16︰11
③ 氧原子数比为 1︰1 ④ 质量比为 16︰11
A. ①③④ B. ①②④ C. ②③④ D. 全部
9、关于11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应的说法正确的是
A.氧化剂是P
B.Cu3P是既是氧化产物又是还原产物
C.当反应中有3mol电子转移时,被还原的CuSO4有1.5 mol
D.被氧化的P原子与被还原的P原子个数比5:6
10、下列离子方程式正确的是
Ca2++2HCO+2OH-= CaCO3↓+CO+2H2O
B. 澄清的石灰水与稀盐酸反应:Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C. 向氢氧化钠溶液中滴入少量硫酸铝溶液:Al3++3OH- = Al(OH)3↓
D.钠与CuSO4溶液反应:2Na + Cu2+ = 2Na+ + Cu
11、下列除去杂质所用的方法正确的是
A. 除去Fe(OH)3胶体中的少量FeC13溶液:将混合物进行过滤
B. 除去Na2CO3溶液中少量NaHCO3:向溶液中通入过量的CO2
C. 除去NaHCO3固体中少量Na2CO3粉末:把固体置于坩埚中充分加热
D. 除去FeC12溶液中少量FeC13:加入足量铁屑,充分反应后过滤
12、某溶液加入铝可以产生H2,则在该溶液中一定能大量存在的离子组是
C. K+、Fe2+、Cl-、NO3- D. Na+、HCO3-、Al3+、Cl-
13、制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为:
2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现在烧杯中的是
A.有铁无铜B.有铜无铁
C.铁、铜都有D.铁、铜都无
14、下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 向某待测液中通入Cl2,再滴入2滴KSCN溶液后,溶液变为血红色 | 证明该待测液中一定含有Fe2+ |
| B | 向某待测液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 证明该待测液中一定含有CO32- |
| C | 把硫酸酸化的H2O2溶液滴入FeCl2溶液中,溶液变成黄色 | 证明H2O2氧化性大于Fe3+ |
| D | 向Al(0H)3沉淀中分别加入盐酸和氨水,沉淀都会溶解 | 证明Al(0H)3是两性氢氧化物 |
15、工业上常用加入K2Cr2O7氧化剂的办法氧化Na2SO3,现已知1mol K2Cr2O7能把3 mol Na2SO3恰好氧化为Na2SO4,K2Cr2O7被还原为Crn+,则n的值为
A.+2 B.+3 C.+4 D.+5
第二部分 非选择题
二.(共55分)
16、
Ⅰ、下图表示的反应关系中,部分产物被略去。已知白色固体X的分解产物中只有A是白色固体,X、A、E、G的焰色反应均为黄色。
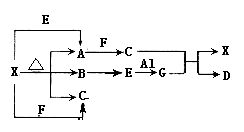
请回答下列问题:
(1)写出X→A+B+C的化学方程式:
(2)写出E→G的化学方程式:
(3)写出G与C反应的离子方程式:
(4)写出在溶液中X+E→A反应的离子方程式:
Ⅱ、根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

请回答下列问题:
(5) 写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(6)某同学取Y的溶液加热煮沸除去H2O2后,冷却,再加入淀粉KI溶液,变为蓝色。写出加入淀粉KI溶液的反应的离子方程式:
。
(7) 写出Cl2将Z氧化为K2EO4的化学方程式: 。
17、
Ⅰ、Na2O2与SO3(g)的反应类似于Na2O2与CO2(g)的反应,请写出Na2O2与SO3反应的化学方程式: 。
 Ⅱ、某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
Ⅱ、某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
请回答下列问题:
(1)图中各装置接口连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略,): → → → ⑥ → ⑦ → → →
(2)装置D中发生反应的化学方程式为: 。
(3)装置B的作用是(用离子方程式表示): 。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,还应注意 (填字母编号)。
a.视线与液体凹液面最低处相平才读数
b.等待气体恢复常温才读数
c.上下移动乙管,使甲乙两管液面相平才读数
(5)实验测得收集的氧气在标准状况下体积为V L,则参与反应的Na2O2 的物质的量为 mol。
18、FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
【查阅资料】1、无水FeCl3在空气中易潮解,加热易升华。
2、氯气(Cl2)是一种有毒的黄绿色气体,能与NaOH溶液
反应。
 【实验探究】 学习小组设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
【实验探究】 学习小组设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
请回答下列问题:
(1)装置A中反应的化学方程式为: 。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是: 。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填操作步骤序号) 。
(4)装置D中FeCl2溶液全部反应后,因失去吸收Cl2的作用而失效,写出证明FeCl2溶液已经失效的操作方法: 。
(5)该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到黄色固体。请写出该反应的离子方程式: 。
 19、硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3 MgO、CaO等,生产工艺流程示意如下:
19、硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3 MgO、CaO等,生产工艺流程示意如下:
请回答下列问题:
(1)将菱锌矿研磨成粉的目的是: 。
(2)漂白粉的有效成分是NaClO,请完成“氧化除铁”步骤中反应的离子方程式:$来&源:
□Fe(OH)2+ □ClO- + □_____= □Fe(OH)3+ □ Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,相对分子质量为89,化学式是 (不用考虑化学式中各元素的排列顺序)。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为 。
| Mg(OH)2 | Zn(OH)2 | |
| 开始沉淀的pH | 10.4 | 6.4 |
| 沉淀完全的pH | 12.4 | 8.0 |
| 开始溶解的pH | — | 10.5 |
资*源%库
(5)假设各步转化均完全,分析图中数据可知:菱锌矿粉中ZnCO3的质量是 。
2016-2017学年度第一学期
班级:_______________姓名:_______________学号:_______________ O•••••••••••••••••••••• 密•••••••••••••••••••••• O•••••••••••••••••••••• 封 •••••••••••••••••••••• O•••••••••••••••••••••• 线••••••••••••••••••••••O
成绩:资*源%库
注意事项:1、本答卷为第二部分非选择题答题区。考生必须用黑色字迹的钢笔或签字笔在各题目指定区域内的相应位置上答题,超出指定区域的答案无效。
2、如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液,不按以上要求作答的答案无效。
二.(共55分) 16、Ⅰ、 (1) (2) (3) (4) Ⅱ、 (5) (6) (7)
17、Ⅰ、
Ⅱ、(1) → → → ⑥ → ⑦ → → →
(2)
(3)
(4) (5)
18、(1)
(2)
(3)
(4)
(5)
19、(1)
(2)□Fe(OH)2+ □ClO- + □_____= □Fe(OH)3+ □ Cl-
(3) (4) (5)
2016-2017学年度第一学期高一级化学科期末试题答案
一、单选题(本题包括15小题,每小题只有一个选项符合题意,各3分,共45分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | A | B | C | D | A | B | B | D |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | |
| 答案 | C | A | D | B | A | C | B |
二、(共55分)
16、(共17分)
Ⅰ、(每小题2分,共8分)
(1)2NaHCO3△Na2CO3 + CO2↑ + H2O (2)2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
(3)AlO2-+ C02+ 2H20 = HCO3-+Al(OH)3↓(4)HCO3-+ 0H一= CO32-+ H20
Ⅱ、(每小题3分,共9分)
(5)Cu + H2O2 + H2SO4 = CuSO4+ 2H2O (6)2Fe3+ + 2I— = 2Fe2+ + I2
(7)10KOH + 3Cl2 + 2Fe(OH)3 = 2K2FeO4 + 6KCl + 8H2O
17、(共15分)
Ⅰ、2SO3+2Na2O2=2Na2SO4+O2(2分)
Ⅱ、(1)⑤③④,②①⑧(2分)
(2) 2Na2O2 + 2CO2 = 2Na2CO3 + O2(2分);2Na2O2 + 2H2O = 4NaOH + O2↑(2分)
(3) HCO3- + H+ = H2O+ CO2↑ (2分)
(4) abc (3分)
(5) V/11.2 (2分)
18、(共11分)
(1)2Fe+3Cl2![]() 2FeCl3(2分)
2FeCl3(2分)
(2)在沉积的FeCl3固体下方加热(2分)
(3)②⑤(2分)
(4)取待证明的溶液2mL,滴入1~2滴酸性KMnO4溶液,如果溶液变为红色,证明FeCl2溶液已经失效。(3分)
(5)2Fe3++H2S=2Fe2++S↓+2H+(2分)
19、(共12分)
(1)增大反应物接触面积(或增大反应速率或使反应更充分)(2分)
(2)2Fe(OH)2+ ClO-+ H2O = 2Fe(OH)3+ Cl-(2分)
(3)FeO(OH)(3分)
(4)8.0≤pH<10.4(2分)
(5)125m2/81m1(3分)