
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2014—2015学年度第二学期
高一年级化学(理科)期考试题
(考试时间:90分钟 满分:100分)
可能用到的相对原子质量:H-1 C-12 O-16 N-14 S-32 Cl-35.5
第Ⅰ卷(选择题,共44分)
一、单项选择题(本题包括6小题,每小题2分,共12分。每小题只有一个选项符合题意)
1.下列说法中,错误的是
A.能量变化是化学反应的基本特征之一
B.化学反应中能量变化的大小与反应物的质量多少无关
C.化学反应中必然伴随发生能量变化
D.化学变化中的能量变化主要是由化学键变化引起的
2.利用下列反应不能制得括号中纯净物质的是
A.乙烯与氯气加成(1,2-二氯乙烷)
B.等物质的量的氯气与乙烷在光照下反应(氯乙烷)
C.乙烯与水加成(乙醇)
D.乙烯与氯化氢在一定条件下反应(氯乙烷)
3.下列有关化学键的叙述,正确的是
A.离子化合物中一定含有离子键
B.单质分子中均存在化学键
C.由不同种非金属元素的原子形成的共价化合物一定只含极性键
D.含有共价键的化合物一定是共价化合物
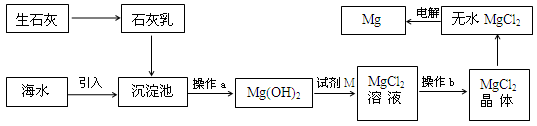 4.海水提镁的主要流程如下:下列说法正确的是
4.海水提镁的主要流程如下:下列说法正确的是
①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应
③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量
A.①②③④⑤B.②③C.④⑤D.①④⑤
5.已知1 mol X2完全燃烧生成X2O(g)放出热量a kJ,且氧气中1 mol O===O键完全断裂时吸收能量b kJ,X2O中1 mol X—O键形成时放出能量c kJ,X2中1 mol X—X键断裂时吸收能量为( )
A.(4c-b+2c)kJB. kJC.4c+b-2a kJD. kJ
6.下列有关有机化学实验的说法中,错误的是
A.除去乙醇中少量乙酸:加入足量生石灰蒸馏
B.乙烯和乙醇都能使酸性KMnO4溶液褪色
C.实验室里制备少量乙酸乙酯可用饱和Na2CO3溶液接收生成物
D.分离甘油和氯化钠溶液用分液的方法
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有1-2个正确答案。)
7.下列有关化学用语使用正确的是
A.钙离子的结构示意图:![]() B.乙烯的结构简式:CH2=CH2
B.乙烯的结构简式:CH2=CH2
C.CH4分子的球棍模型:D.丙烯的电子式:![]()
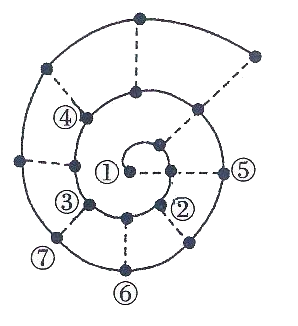 8.如果将前18号元素按原子序数递增的顺序排列,可形成右图所示的“蜗牛”形状,图中每个“· ”代表一种元素,其中①点代表氢元素。
8.如果将前18号元素按原子序数递增的顺序排列,可形成右图所示的“蜗牛”形状,图中每个“· ”代表一种元素,其中①点代表氢元素。
下列说法不正确的是( )
A.最简单气态氢化物的稳定性③比⑦小
B.最高价氧化物对应小化物的酸性⑥比⑦弱
C.金属性②比⑤弱
D.原子半径③比④大
9.今年3月11日, 在日本大地震灾难中,福岛核电站泄漏的放射性物质中含有I,下列有关说法正确的是
A.I元素中含中子数为53B.它是碘元素的一种同位素
C.I2的摩尔质量为262 g D.由此可确定碘元素相对原子质量为131
10.下列过程中需要吸收热量的是
A.H2→2HB.2H2+O2===2H2O
C.CaO+H2O ===Ca(OH)2D.2Cl→C12
11.已知化学反应:C(s)+1/2O2(g) == CO(g) △H1<0
CO(g) +1/2O2(g) == CO2(g)△H2<0
C(s)+O2(g) == CO2(g)△H3<0;
下列说法不正确的是(相同条件下)( )
A.56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量
B.12gC所具有的能量一定大于28gCO所具有的能量
C.△H1+△H2>△H3
D.将两份质量相等的碳燃烧,生成CO2的反应比生成CO的反应放出的热量多
12.下列说法正确的是
A.NH4Cl固体为离子化合物
B.CO2分子中含有离子健
C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行
D.X2+的核外有18个电子,则X在第四周期第ⅡA族
13.在绿色化学工艺中,理想状态是反应物中原子全部转化为欲制得的产物,即原子的利用率为100%,在用CH3C≡CH合成CH2=C(CH3)COOCH3的过程中,欲使原子利用率达到最高,还需要的反应物有
A.CO2和H2OB.CO和CH3OH
C.CH3OH和H2D.CO和H2
14.下列各种方法中,适用于炼制相应金属的是
A.加热氧化铜炼铜B.氧化镁跟铝粉共热炼镁
C.用焦炭还原氧化铜炼铜D.电解熔融氯化钠冶炼钠
第Ⅱ卷(非选择题,共56分)
 15.(8分)下列各组物质中属于同系物的是________,互为同分异构体的是________,互为同位素的是________,属于同一物质的是 。
15.(8分)下列各组物质中属于同系物的是________,互为同分异构体的是________,互为同位素的是________,属于同一物质的是 。
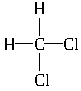
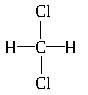
① C(CH3)4和C4H10② 和
③35Cl和37Cl ④ CH3—CH—COOH 和 CH3—CH2—CH2—NO2
⑤ (CH3)2CHCH(CH3)2和 (CH3)2CH(CH2)2CH3
⑥ CH3—CH—CH2—CH3 和 CH3—CH2—CH—CH2—CH3
⑦CH2=CH—CH=CH2 和 CH3—CH=CH—CH3⑧CH3CH2CH2Cl和CH3CH2Cl
16.(共12分)有A、B、C、D、E五种种短周期元素原子序数依次增大,A是原子半径最小的元素:B原子最外层电子数是次外层电子数的2倍;D是地壳中含量最多的元素:E元素最高正价是+7价。回答下列问题:
(1)元素E在元素周期表中的位置为____________________。
(2)B、C、D的原子半径由大到小的顺序为 (用元素符号表示,下同)。
(3)C的氢化物与它最高价氧化物对应的水化物相互反应生成的物质中所含的化学键类型有 。
(4)由原子个数比为1∶1∶1的A、B、C 三种元素组成共价化合物X,共形成4个共用电子对,X的结构式为 。
(5)A、D两种元素按原子个数之比为1∶1组成的常见液态化合物,在酸性溶液中能将海带中的I-氧化为碘单质,写出该反应的离子方程式 。
(6)CE3常温下呈液态,可与水反应生成一种酸和一种碱,反应的化学方程式为___________________________________________。
17.(10分)已知1 molCO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成气态水放出242 kJ热量;1 molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。1 mol液态水蒸发为气态水是要吸收44 kJ热量。
(1)写出能表示CO燃烧热的热化学方程式 。
(2)若1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量为 890 kJ
(填“>”、 “<”、“= ”)。
(3)燃烧10gH2生成液态水,放出的热量为 。
(4)氢气的燃烧热为 。
(5)写出CH4气体不完全燃烧生成只生成CO气体和液态水的热化学方程式
。
18.(14分)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,D、G是生活中常见的有机物,各物质发生如图所示的一系列化学反应。
根据如图回答下列问题:
(1)按要求填写:
A的结构式: ;B的结构简式: ;
C的电子式: ;D的官能团名称 ;
G官能团的结构简式 。
(2)写出④⑥⑧两步反应的化学方程式,并注明反应类型:
④ (反应类型 )。
⑥ (反应类型 )。
⑧ (反应类型 )。
19.(12分) 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是
(填序号)。
A.Cl2、Br2、I2的熔点 B. Cl2、Br2、I2的氧化性
C.HCl、HBr、HI的热稳定性 D. HCl、HBr、HI的酸性
(2)工业上,通过如下转化可制得KClO3晶体:
![]()
![]() NaCl溶液 NaClO3溶液 KClO3晶体
NaCl溶液 NaClO3溶液 KClO3晶体
①完成Ⅰ中反应的总化学方程式: 。
②Ⅱ中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(3)一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如下图所示。
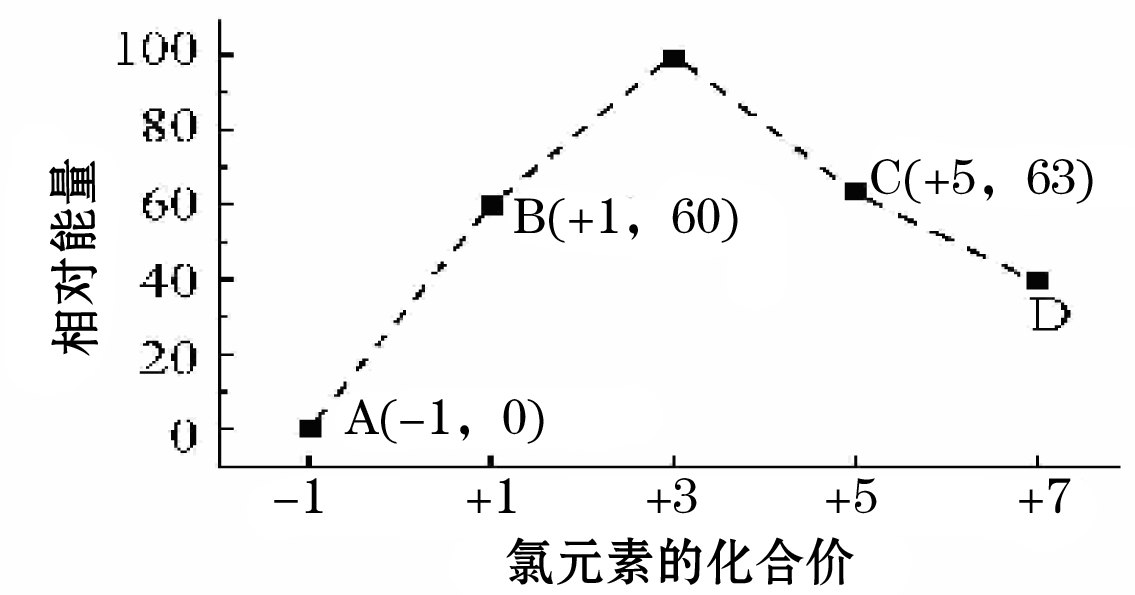
① D是 (填离子符号) 。
② B→A+C的反应中,生成1mol C ,同时会消耗 mol B,
并 KJ的热量(填吸收或放出以及具体数值)。
2014—2015学年度第二学期
高一年级化学(理科)期考试题参考答案
第Ⅰ卷(选择题,共44分)
一、单项选择题(本题包括6小题,每小题2分,共12分。每小题只有一个选项符合题意)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 答案 | B | B | A | D | B | D |
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有1-2个正确答案,全选且正确得4分;若题目有两个答案的,只选一个且正确得2分;多选、错选不得分。)
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 | BC | A | B | A | BC | AD | BD | CD |
第Ⅱ卷(非选择题,共56分)
15.(每空2分,共8分) ① ⑧ ④⑤ ③ ②⑥
16.(共12分)
(1)第三周期 ⅦA族(2分)
(2)C>N>O(2分)
(3)离子键、共价键(2分)
(4)H—C≡N(2分)
(5)H2O2+2I-+2H+=== I2+2H2O(2分)
(6)NCl3+4H2O===3HClO+NH3·H2O(2分)
17.(每空2分,共10分)
(1)CO(g ) + 1/2 O2(g ) = CO2(g) ;△H = -283 kJ/mol
(2)< (3) 1210 kJ (4)286 kJ/mol
(5)CH4(g ) +3/2 O2(g ) = CO(g)+2H2O(l) ;△H = -607 kJ/mol
18.(共14分)
(1)略 (每空1分)
(2)(方程式2分,类型1分,)
④![]() 加聚反应
加聚反应
⑥ 2CH3CH2OH + O22CH3CHO+2H2O 氧化反应
⑧ CH3COOH+HO-C2H5CH3COOC2H5+H2O ,取代反应;
19.(12分)
通电 △
(2)① NaCl+3H2O=====NaClO3+3H2↑ (2分)
② 复分解反应(1分)
室温下,氯酸钾在水中的溶解度明显小于其它晶体(1分)
(3)①ClO4- (2分) ② 3(2分) 放出117(2分)