
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
桥东中学2014~2015学年上学期期中考试
高一化学试卷
一、选择题(20小题,每小题3分,共60分。每小题只有一个选项符合题意)
1.下列广告语在科学上没有错误的是( )
A.这种饮料是纯天然的,不含任何化学物质
B.这种口服液含丰富的氮磷锌等微量元素
C.这种神奇液体加入水中可以“以水代油”做发动机燃料
D.没有水就没有生命
2.下列各物质的分类、名称(或俗名)、化学式都正确的是 ( )
A.碱性氧化物 氧化铁 FeO B.酸性氧化物 碳酸气 CO
C.酸 硫酸 H2S D.盐 纯碱 Na2CO3
3.胶体最本质的特征是( )
A.分散质微粒的粒度在1~100nm之间 B.具有丁达尔效应
C.可以透过滤纸 D.均一、稳定、透明
4.同物质的量浓度的下列物质中导电能力最强的是( )
A.氯化钠 B.硫酸 C.盐酸 D.酒精
5.下列说法正确的是( )。
A.CO2的水溶液能导电,所以CO2是电解质
B.BaSO4不溶于水,其水溶液很难导电,所以BaSO4是非电解质
C.液氯不导电,所以液氯是非电解质
D.氯化氢的水溶液能导电,所以氯化氢是电解质
6.在Zn、ZnO、ZnCO3、盐酸、CuCl2和CaCl2溶液六种物质中,每两种物质反应能生成ZnCl2的方法有( )
A.2种 B.3种 C.4种 D.5种
7.新制氯水与久置的氯水相比较,下列结论不正确的是( )
A.颜色相同B.前者能使有色布条褪色
C.都含有H+D.加AgNO3溶液都能生成白色沉淀
8.下列溶液中Cl-浓度最小的是( )
A.200mL 2mol/L MgCl2溶液 B.1000mL 2.5mol/L NaCl溶液
C.300mL 5mol/L KClO3溶液 D.250mL 1mol/L AlCl3溶液
9.将等物质的量浓度、等体积的硫酸溶液与烧碱溶液充分混合后,滴入紫色石蕊试液,溶液呈( )
A.紫色 B.红色 C.蓝色 D.无色
10.设NA代表阿佛加德罗常数,下列说法正确的是( )
A.22.4LCO和CO2的混合气体中所含的碳原子数一定是NA
B.含1molHCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为2NA
C.常温常压下,32gO2或32gO3所含氧原子数都是2NA
D.标准状况下,11.2LH2O含有0.5NA分子
11.用自来水(用Cl2消毒)养金鱼时,将水注入鱼缸的前需在阳光下暴晒一段时间,
目的是 ( )
A.使水的温度升高B.增加水中O2的含量
C.起到杀菌作用 D.使水中HClO分解
12.除去粗盐中的Ca2+、Mg2+、SO42-,可将粗盐溶于水后进行如下操作:①过滤,②加过量的NaOH溶液,③加适量的盐酸,④加过量的Na2CO3溶液,⑤加过量的BaCl2溶液,⑥蒸发结晶,其中操作顺序正确的是( )
13.实验室用下列两种方法制取氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量的浓盐酸反应,则所得Cl2( )
14.下列氯化物中,不能用单质跟氯气直接反应制得的是( )
A.NaCl B.FeCl2C.CuCl2D.HCI
15.下列选项中,与氯气用途无关的是 ( )
A、消毒杀菌 B、制漂白粉 C、制盐酸 D、从海水中提取食盐
16.氯气可以用来消灭田鼠,使用方法是将氯气通过软管灌入田鼠洞中,这是利用了氯气以下性质中的 ( )
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤能溶解于水
A、①②③ B、②③ C、③④ D、③④⑤
17.下列有关实验用品的使用或操作的叙述中,正确的是( )
A.用红色石蕊试纸检验溶液的酸性
B.容量瓶可以配制准确浓度的溶液,但不能作为反应容器使用
C.配制稀硫酸时,先向烧杯中注入浓硫酸,再加水稀释
D.称量NaOH固体时,将NaOH直接入在托盘上的纸上
18.在相同物质的量的下列分子中,电子总数最少的是( )
A.CO B.O2C.H2S D.NO
19.已知元素R有某种核素的离子Rx+,该离子核内中子数为Y,核外电子数为Z,该核素的符号为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
20.现有A.B.C三种化合物,各取20g相混合,完全反应后,得9g B,24.5g C,还有D生成。已知D的相对分子质量为106。现将11gA和5.5gB反应,能生成D ( )
二、非选择题(共40分)
21.(6分)已知过氧化钠(Na2O2)能与水发生如下反应:
2Na2O2+2H2O====4NaOH+ O2↑,7.8g过氧化钠与足量水反应后,将会产生
molNaOH,生成的O2在标准状况下所占的体积是 L
22.(18分)实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
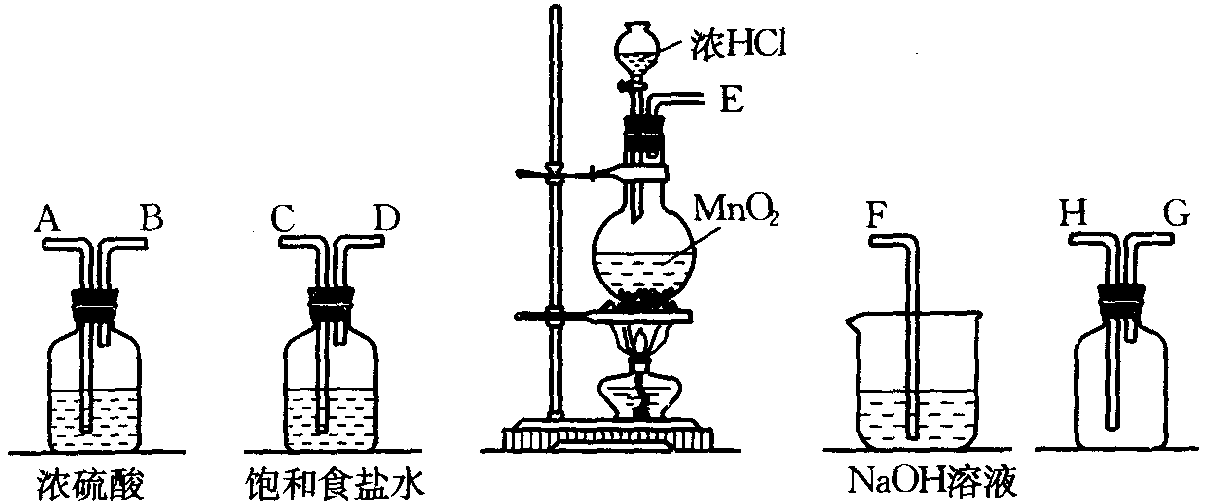
(1)盛放浓盐酸的玻璃仪器的名称是 。
(2)连接上述仪器的正确顺序是(填各接口处的字母): 接 , 接 ,
接 , 接 。
(3)① 饱和食盐水的作用 ,
② 浓硫酸起的作用是 。
(4)化学实验中如果将Cl2通入蒸馏水中,得到 色的溶液,写出反应方程式 。该溶液中含有多种微粒,其中,显示颜色的微粒是(填微粒符号,下同) ,具有漂白性的微粒是 ,与硝酸银溶液反应产生白色沉淀的微粒是 ,显酸性的微粒是 。
(5)① 气体发生装置中进行的反应化学反应方程式是:
;
② NaOH溶液的作用是: ,
反应的化学方程式是: 。
23.(共9分) 完成以下实验题
(1)用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液500 mL。
a.实验中用到的玻璃仪器有量筒、玻璃棒、烧杯、胶头滴管,还缺少____________;实验中两次用到玻璃棒,其作用分别是______________、________________。
b.应称取Na2CO3·10H2O的晶体的质量(用托盘天平称取):_____________。
c.配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容
正确的操作顺序是__________________(填序号)。
(2)某学生取5mL 某浓度的Na2SO4溶液,加入一定量的BaCl2溶液,产生白色沉淀,确定加入的BaCl2溶液已过量的实验方法是:
。
24.(7分)实验室欲用KMnO4固体和浓盐酸反应制取标准状况下的氯气4.48L,反应的化学方程式如下:
2KMnO4+16HCl(浓) === 2KCl+2MnCl2+5Cl2↑+8H2O。
(1) 该反应是否氧化还原反应?答: 。
(2) 理论上需要高锰酸钾的质量是多少?(按规范要求写出计算过程,下同)
(3) 若反应前后溶液的体积均为200mL,且反应后残留盐酸的浓度为7.8 mol·L-1,求反应前所用浓盐酸的物质的量浓度时多少?
班级 姓名 原班级座号 准考号 密 封 线 内 不 得 作 答
高一化学试卷答题卷2014.11
| 题号 | 选择题 | 填空题 | 总分 | |||
| 得分 | ||||||
一、选择题:(单选。每小题3分,共60分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | ||||||||||
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 |
二、非选择题:(第21至24题,共40分)
21.(6分) ; 。
22.(18分) (1) 。
(2) 接 ,_____接 ,_____接 , 接 。
(3)① ;② 。
(4) 色; ;
; ; ; 。
(5)① ;②
; __ 。
23.(9分)
(1)a ; ; ;
b ;c 。
(2)
。
24.(7分) (1) 。 (2)、(3)解题过程答在下列空白处:
| 座位号 | |

