
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
鹤岗一中2016—2017度上学期期末考试
高一化学试题
可能用到的原子量:H1O16Na23Mg24Al27Fe56Cl35.5
1.化学与生产、生活密切相关,下列说法正确的是
A.PM2.5是指大气中直径接近2.5×l0-6m的颗粒物,分散在空气中形成胶体
B.石英用于生产光导纤维和计算机芯片
C.焰火的五彩缤纷是某些金属元素物理性质的展现
D.食盐、次氯酸钠溶液均可以将某些病毒氧化而达到消毒的目的
2.下列有关物质分类或归类正确的一组是( )
A.液氯是混合物 B.水玻璃是纯净物 C.酒精是电解质 D.纯碱不属于碱
3.下列离子方程式书写正确的是( )
A.酸性条件下KIO3溶液与KI溶液发生反应生成I2:
IO3﹣+5I﹣+6H+═3I2+3H2O
B.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
C.石灰乳与Na2CO3溶液混合:Ca2++CO32﹣═CaCO3↓
D.用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑
4.下列有关实验的说法正确的是( )
A.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该溶液一定有CO32﹣
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
D.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
5.某无色溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是
A.NH4+、Fe2+、Cl-、SO42-B.Na+、K+、Cl-、SO42-
C.Mg2+、AlO2-、Cl-、SO42-D.K+、Ca2+、HCO3-、Cl-
6.下列有关物质的性质或应用正确的是
A.钠与硫酸铜溶液反应会置换出红色的铜
B.常温下干燥氯气与铁不反应,可以用钢瓶储存液氯
C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D.普通玻璃的组成可用Na2O·CaO·6SiO2表示,是纯净物
7.Na2CO3和NaHCO3是金属钠常见的两种碳酸盐,它们广泛地应用于生产和生活中。下列有关碳酸钠和碳酸氢钠的说法中,不正确的是( )
A.NaHCO3能中和胃酸,对胃壁不产生强烈的刺激或腐蚀作用,可用于治疗胃酸过多症,但不适合胃溃疡病人
B.NaHCO3能中和面粉发酵后产生的酸,并且产生二氧化碳气体,可用于做馒头
C.可以用澄清石灰水来鉴别Na2CO3溶液中和NaHCO3溶液
D.往Na2CO3饱和溶液中通入CO2气体,可获得NaHCO3沉淀
8.一定量的MnO2与xmL10mol/L的盐酸共热制取氯气,在标准状况下产生2.24L气体.则x的值应为( )
A.x=20B.x=40C.20<x<40D.x>40
9.下列各组溶液,只用胶头滴管和试管,不用其它任何试剂就可以鉴别的是( )
①Al2(SO4)3和KOH ②稀盐酸和稀Na2CO3
③NaAlO2和H2SO4④Ba(OH)2和NaHCO3.
A.①B.①③C.①②③D.①②③④
10.已知反应:①Cl2+2HBr=2KCl+Br2;②KClO3+6HCl=KCl+3Cl2↑+3H2O;③2KBrO3+Cl2=Br2+2KClO3,下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2
C.反应②中氧化剂与还原剂的物质的量之比为1:6
D.反应③中1mol还原剂反应,则氧化剂得到电子的物质的量为2mol
11.如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条上看不到明显现象;当关闭B阀后,C处红布逐渐褪色,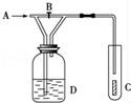 则D瓶中装的是( )
则D瓶中装的是( )
A.浓H2SO4B.NaOH溶液
C.Na2SO3溶液 D.饱和NaCl溶液
12.下列推断不正确的是( )
资*源%库A.工业上可以用碳还原二氧化硅得到硅和二氧化碳
B.制普通玻璃的主要原料是纯碱、石灰石、石英
C.Mg失火不能用CO2灭火;Na失火也不能用CO2灭火
D.Fe与S直接化合生成FeS;Al与S也可以直接化合得到Al2S3
13.以下物质间的每步转化通过一步反应就能实现的是( )
A.Al--Al2O3--Al(OH)3--NaAlO2
B .S--SO3-- H2SO4-- MgSO4
C.Mg--MgCl2--Mg(OH)2—MgO
D.Si--SiO2--H2SiO3--Na2SiO3
14.将0.03 mol Cl2缓缓通入含0.02mol H2SO3和0.02 mol HBr的混合溶液中,在此过程溶液的c(H+)与Cl2用量的关系示意图是(已知Br2+SO2+2H2O= H2SO4+2HBr,溶液的体积视为不变)( )

15.有一块铁的“氧化物”样品,用140mL 5.0mol/L盐酸恰好将之完全溶解,所得溶液还能吸收0.025mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe4O5B.Fe5O7C.Fe2O3D.Fe3O4
16.工业上用固体硫酸亚铁制取颜料铁红,反应原理是:2FeSO4![]() Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
A.(I)中会生成 BaSO3、BaSO4两种沉淀
B.可将(I)中的 BaCl2溶液改为 Ba(NO3)2溶液
C.(II)所盛 x 应为品红溶液
D.(III)的作用是检验生成的SO2气体
17.下列实验操作能够达到实验目的的是( )

A.实验室采用图①所示装置收集SO2
B.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤
C.称取0.40 g NaOH,置于100 mL容量瓶中,加水溶解,配制0.10 mol/L NaOH溶液
D.可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱
18.盛有O2和NO2的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半.则原混合气体中O2和NO2的体积比是( )
A.3:1B.3:2C.2:1D.1:2
 B
B C
C

20.(10分)(1)质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是.
(2)下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是.(填序号)
①NaAlO2②Ca(OH)2③Na2CO3④Al(OH)3⑤NaHCO3
(3)Na、Mg、Al分别与足量的硫酸溶液反应,当生成气体的质量相同时,消耗掉的Na、Mg、Al的物质的量之比为.
(4)将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量是溶液中所含铝元素的质量的2倍,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是
(5)1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
21.(8分)有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+ | Na+ | Cu2+ | Al3+ |
| 阴离子 | SO42- | HCO3- | NO3- | OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是:①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成。根据上述实验填空:
(1)写出C、D的化学式:C ,D 。
(2)向C溶液中加入过量E溶液,反应的离子方程式为 。
(3)检验C中阴离子的方法: 。
22.(14分)如图是一些中学常见的物质之间的转化关系(其中部
分反应产物省略),其中A和B常温下都是气体,且水溶液都有漂白性; F、M、N均为难溶于水的白色沉淀,其中M和N不溶于稀硝酸;C和D是两种常见的强酸.请回答下列问题:

(1)写①的化学方程式
(2)写反应②的离子方程式
(3)写出将A通入石灰乳的化学方程式
(4)在①②③④⑤⑥中,属于氧化还原反应的有:(填编号)
(5)F很不稳定,露置在空气中容易被氧化为H,该反应的化学方程式为
,保存 E溶液时应加入少量的
(6)检验G溶液中阳离子的方法:(写出加入试剂的名称和现象)
23.(14分)如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉).请回答:
(1)仪器A的名称是,烧瓶中反应的化学方程式是.
(2)装置B中盛放液体是,气体通过装置B的目的是.
装置C中盛放的液体是,气体通过装置C的目的是.
(3)D中反应的化学方程式是
(4)烧杯E中盛放的液体是,反应的离子方程式是.
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应.为收集D中产物,在D与E之间,除增加收集装置外,还需要增加装置.
24(6分)准确称取22.7g某矿石样品(含Al2O3、Fe2O3和不溶于水和酸的杂质),放入盛有100mL某浓度的硫酸的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如图所示.请回答:

(1)硫酸的物质的量浓度是多少?
(2)若a=10,矿石样品中Fe2O3的质量是多少?
(3)试计算a的取值范围.
资*源%库

资*源%库
高一化学试题答案
(1-9,2分,10-19,3分,共48分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C | D | A | C | B | B | C | D | C | B |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | |
| D | A | C | A | B | C | D | B | B |
20. (8分,每空2分)
21. (14分)(1)SO2+Cl2+2H2O=H2SO4+2HCl;
(2)2Fe2++Cl2=2Fe3++2Cl﹣;
(3)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(4)①②⑥;(2分) (5)4Fe(OH)2+O2+2H2O=4Fe(OH)3;铁粉(1分);(6)硫氰化钾溶液(2分),变红(1分).
23.(14分)
(4)NaOH溶液(1分),2OH﹣+Cl2=Cl﹣+ClO﹣+H2O(2分);
(5) 干燥(2分).
24.(6分)(1)5mol/L(2)16g(3)4ml<a<70ml