
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
金山中学2015学年度第一学期高二年级化学学科期末等级考试卷
(考试时间:60分钟 满分:100分 命题人:陈英 审核人:沈龙根)
可能用到的相对原子质量:H-1 O-16 C-12 S-16 Fe-56 Cu-64 Ba-137
一、选择题(每小题只有一个正确选项,每题2分,共40分)
1、下列物质中,属于烃类的是
A.C2H5OH B.CH3Cl C.C9H8D.C6H5NO2
2、下列表示甲基的电子式中,正确的是
![]()
3、大量获得乙烯的工业方法是:
A.乙醇脱水B.石油分离C.石油裂化D.石油裂解
4、下列关于测定1mol氢气体积的操作中,错误的是
17.两种气态烃的混和气体共1升,在空气中完全燃烧生成1.5升CO2气体和2升水蒸气(气体体积均在相同状况下测定),关于该混和气体的说法正确的是
A. 一定不含乙烷 B. 一定含甲烷,不一定含乙烷
C. 一定含乙烷,不一定含甲烷 D. 一定含甲烷
18、现有乙酸(分子式:C2H4O2)和两种链状单烯烃混合物,其中氧的质量分数为a,则碳的质量分数是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
19、“塑料王”的耐热性和化学稳定性均超过其他塑料,合成路线如下:

下列说法中,错误的是
A.“塑料王”是高分子材料
B.二氟一氯甲烷的分子中只含共价键
C.聚四氟乙烯中碳原子均在同一直线上,形成链状高分子
D.四氟乙烯(CF2=CF2)中所有的原子都在同一个平面上
![]() 20、β—月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有
20、β—月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有
A. 4种 B.3种 C. 2种 D.6种
二、选择题(本题包括5个小题,每小题有一或二个选项符合题意,错选或多选不得分;每小题4分,共20分)
21、已知Mg2C3的结构与CaC2相似,由此可断定Mg2C3与水反应的产物是
A.Mg(OH)2和CH≡CH B.MgO和CH≡CH
C.Mg(OH)2和CH3CH==CH2D.Mg(OH)2和CH3C≡CH
22、不考虑现代物理手段,溶液中离子的定性检验有三种基本方法,①沉淀法(观察反应中沉淀的发生或消失)、②气体法(观察反应中气体的产生及其验证)、③显色法(观察颜色变化)。溶液中下列离子的检验或鉴别有以上两种基本方法可供选择的是
A. Al3+B.Na+ C. I- D. CO32-
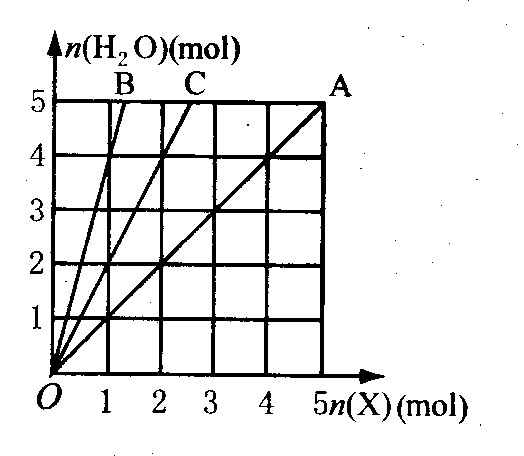 23、如右图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是
23、如右图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是
A. C2H4与C3H4,体积比为任意比
B. H2与C4H8,体积比2:1
C. C2H2与C3H8,体积比1:2
D. H2与C2H6,体积比3:1
24、硫酸铜结晶水含量测定的实验中,若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有
A.被测样品中含有加热不挥发的杂质B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水D.加热前所用的坩埚未完全干燥
25、下列各组烃的混和物,只要总质量一定,无论它们按什么比例混和,完全燃烧后生成的CO2和H2O都是恒量的是
A.C2H2C2H4B.C2H4C3H6C.C3H8C3H6D.C6H6C2H2
三、填空题(共30分)
26、(1)把1体积甲烷和4体积Cl2组成的混合气体充入大试管中后倒立在盛有饱和食盐水的水槽里,放在光亮处。片刻后发现试管中的气体颜色 ,试管中的液面 ,试管壁上有 出现,水槽中的现象是 。
27、Ⅰ.①![]() H与
H与![]() H;②O2与O3;③正丁烷(CH3CH2CH2CH3)与异丁烷
H;②O2与O3;③正丁烷(CH3CH2CH2CH3)与异丁烷![]() ;④甲烷(CH4)与丙烷(C3H8):
;④甲烷(CH4)与丙烷(C3H8):
(1)互为同位素的是______ (填序号,下同)。
(2)互为同系物的是______。
(3)互为同分异构体的是______。
(4)互为同素异形体的是______。
II.A~E等几种烃分子的球棍模型如下图所示,据此回答下列问题。
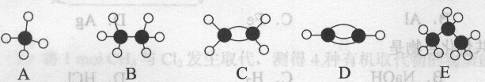
(1)D的电子式为___________,A的二氯取代物有 种。
(2)可作为植物生长调节剂的是 (填结构简式);
(3)C与水在一定条件下反应的化学方程式为: 。
28、乙烷和丙烷的混合气体与足量的氧气混合点燃后,将燃烧产物通过浓硫酸,浓硫酸增重3.06g,使剩余气体再通过足量的Na2O2(反应方程式:2CO2+ 2Na2O2→Na2CO3+ O2),固体质量增加3.36g,求原混合气中乙烷和丙烷的体积比
29、实验室制取乙烯并检验乙烯性质的装置如下图。请回答有关问题: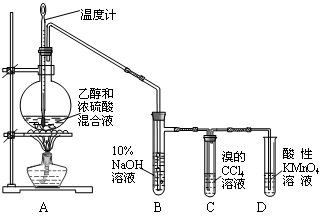
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是 。
(2)烧瓶中产生乙烯的反应方程式为 。
(3)反应开始后,可观察到C和D中共同的现象是 ; C中的反应类型为 反应、D中的反应类型为 反应。
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是 。
30、某同学欲配制0.1 mol/L Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂,配制溶液时发现所取试剂在水中部分溶解,烧杯中存在大量未溶物。
(1)他猜测烧杯中未溶物为 ,因为____________ ;
(2)为准确测定样品中Ba(OH)2的含量,进行如下实验:
①配制250 mL约0.1 mol/L Ba(OH)2溶液:称取5.000 g试样,置于烧杯中,加适量蒸馏水,充分搅拌溶解,静置过滤,得滤液和沉淀,将滤液转入______中,洗涤烧杯和玻璃棒,定容,摇匀。
②滴定:准确量取25.00 mL所配制Ba(OH)2溶液于锥形瓶中,滴加2滴甲基橙,将0.200 mol/L标准盐酸装入滴定管,滴定至终点,记录数据,重复滴定3次,平均消耗盐24.20 mL。计算样品中Ba(OH)2的质量分数为____________(保留小数点后面2位)。
(3)上述滴定中,滴定管在注入标准盐酸之前,先用蒸馏水洗净,再用_______________;在滴定中,准确读数应该是滴定管上蓝线的________________处所对应的刻度,滴定终点的现象是_______________。
四、计算题(共10分)
31、硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
| 实验次序 | 温度(℃) | 冷却后剩余固体的质量(g) |
| 1 | 102 | 6.848 |
| 2 | 113 | 5.696 |
| 3 | 258 | 5.120 |
| 4 | 570 | 2.560 |
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
金山中学2015学年度第一学期高二年级化学学科期末等级考试
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | C | C | D | B | B | D | B | C | B | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | A | D | C | B | A | A | C | C | A |
二、选择题(本题包括5个小题,每小题有一或二个选项符合题意,错选或多选不得分;每小题4分,共20分)
| 题号 | 21 | 22 | 23 | 24 | 25 |
| 答案 | D | CD | B | AC | BD |
三、填空题(共30分)
26、黄绿色逐渐变浅 上升 油状液滴 有少量晶体出现 (4分)
27、Ⅰ(1)①(2)④(3)③(4)② (4分)
II. (1)![]() 1 (2分)
1 (2分)
(2)CH2=CH2(1分)
(3)CH2=CH2+H2O![]() CH3CH2OH (1分)
CH3CH2OH (1分)
28、3:2 (2分)
29、(1)防止暴沸(1分)
(2)![]() (2分)
(2分)
(3)褪色 加成 氧化 (3分)
(4)浓硫酸将乙醇和乙酸炭化,浓硫酸被碳还原产生了SO2;(2分)
30、(1)BaCO3Ba(OH)2能与空气中的CO2反应,生成难溶于水的BaCO3;(2分)。
(2)①250 mL容量瓶中;②0.83(3分)。
(3)标准盐酸溶液润洗2~3次;粗细交界点;
溶液由黄色变为橙色,且半分钟内保持不变(3分)
四、计算题(共10分)
31、(1)1.152g(3分)(2)CuSO4·H2O(3分)(3)64 mL(4分)