
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
宁夏育才中学孔德学区2015-2016-2高二年级月考1
化学试卷
(试卷满分100分,考试时间为100分钟) 命题人:
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 P-31 S-32 Cl-35.5
Cr-52 Br-80
第一部分:选择题(共25小题,每小题2分,共50分)
一.选择题(每题2分,共25题)
1.用高能Mg核轰击Cm核,发生核合成反应,得到新原子Hs,该原子中中子数与核外电子数之差为( )
A.161 B.108 C.84 D.53
2.按能量由低到高的顺序排列,正确的一组是( )
A.1s、2p、3d、4sB.1s、2s、3s、2p
C.2s、2p、3s、3pD.4p、3d、4s、3p
3.表示一个原子在第三个电子层上有10个电子可以写成( )
A.3s10B.3d10C.3s23p63d2D.3s23p53d3
4.隐形战机的核心材料是金属钛,我国探明储量世界第一。下列有关推断不正确的是( )
A.钛的原子序数为22
B.钛位于元素周期表第四周期
C.钛原子核外电子排布式为1s22s22p63s23p63d4
D.钛属于过渡元素
5.价电子排布为5s25p1的元素,在周期表中的位置是( )
A.第四周期第ⅤA族 B.第五周期第ⅢA族
C.第五周期第ⅠA族 D.第四周期第ⅢA族
6.某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是( )
A.电子排布式为:1s22s22p63s23p63d34s2
B.该元素为V
C.该元素为ⅡA族元素
D.该元素位于d区
7.具有下列电子层结构的原子,其对应元素一定属于同一周期的是( )
A.两种原子的电子层上全部都是s电子
B.3p能级上只有一个空轨道的原子和3p能级上有一个未成对电子的原子
C.最外层电子排布式为2s22p6的原子和最外层电子排布式为2s22p6的离子
D.原子核外的M层上的s能级和p能级都填满了电子,而d轨道上尚未排有电子的两种原子
8.X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下列说法中正确的是( )
A.X的原子半径比Y的小
B.X和Y的核电荷数之差为m-n
C.电负性X>Y
D.第一电离能X<Y
9.已知短周期元素R原子最外层p能级上有2个未成对电子。下列关于R原子的叙述正确的是( )
A.R的氧化物都能溶于水
B.R的最高价氧化物对应水化物的化学式都是H2RO3
C.R都是非金属元素
D.R的氧化物都能与NaOH溶液反应
10.下列物质的分子中既有σ键,又有π键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
A.①②③ B.③④⑤⑥ C.①③⑥ D.③⑤⑥
11.下列关于化学键的说法正确的是( )
A.构成单质分子的粒子中一定含有共价键
B.由非金属元素组成的化合物不一定是共价化合物
C.非极性键只存在于双原子单质分子里
D.不同元素组成的多原子分子里的化学键一定是极性键
12.在白磷(P4)分子中,4个P原子分别处在正四面体的四个顶点,结合有关P原子的成键特点,下列有关白磷的说法正确的是( )
A.白磷分子的键角为109°28′ B.分子中共有4对共用电子对
C.白磷分子的键角为60° D.分子中有6对孤电子对
13.下列事实不能用键能的大小来解释的是( )
A.N元素的电负性较大,但N2的化学性质很稳定
B.稀有气体一般难发生反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.F2比O2更容易与H2反应
14.用价层电子对互斥理论判断SO3的分子构型为( )
A.正四面体形 B.V形 C.三角锥形 D.平面三角形
15.下列分子中,各原子均处于同一平面上的是( )
A.NH3B.CCl4C.PCl3D.CH2O
16.下列分子的结构中,原子的最外层电子不都满足8电子稳定结构的是( )
A.CO2B.PCl3C.CCl4D.BF3
17.下列分子中的中心原子杂化轨道的类型相同的是( )
A.CO2与SO2B.CH4与NH3
C.BeCl2与BF3D.C2H2与C2H4
18.用过量的硝酸银溶液处理含有0.01 mol氯化铬(CrCl3·6H2O)的水溶液,生成0.02 mol AgCl沉淀,此氯化铬最可能是( )
A.[Cr(H2O)6]Cl3B.[Cr(H2O)5Cl]Cl2·H2O
C.[Cr(H2O)4Cl2]Cl·2H2O D.[Cr(H2O)3Cl3]·3H2O
19.下列各组物质中,都是由极性键构成的极性分子的是( )
A.CH4和Br2B.NH3和H2O
C.H2S和CCl4D.CO2和HCl
20.下列关于氢键的说法正确的是( )
A.由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3
B.氢键只能存在于分子间,不能存在于分子内
C.没有氢键,就没有生命
D.相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
21.下列现象不能用“相似相溶原理”解释的是( )
A.氯化氢易溶于水 B.氯气易溶于氢氧化钠溶液中
C.碘易溶于四氯化碳 D.碘难溶于水
22.判断物质在不同溶剂中的溶解性时,一般都遵循“相似相溶”规律。下列装置中,不宜用做HCl尾气吸收的是( )
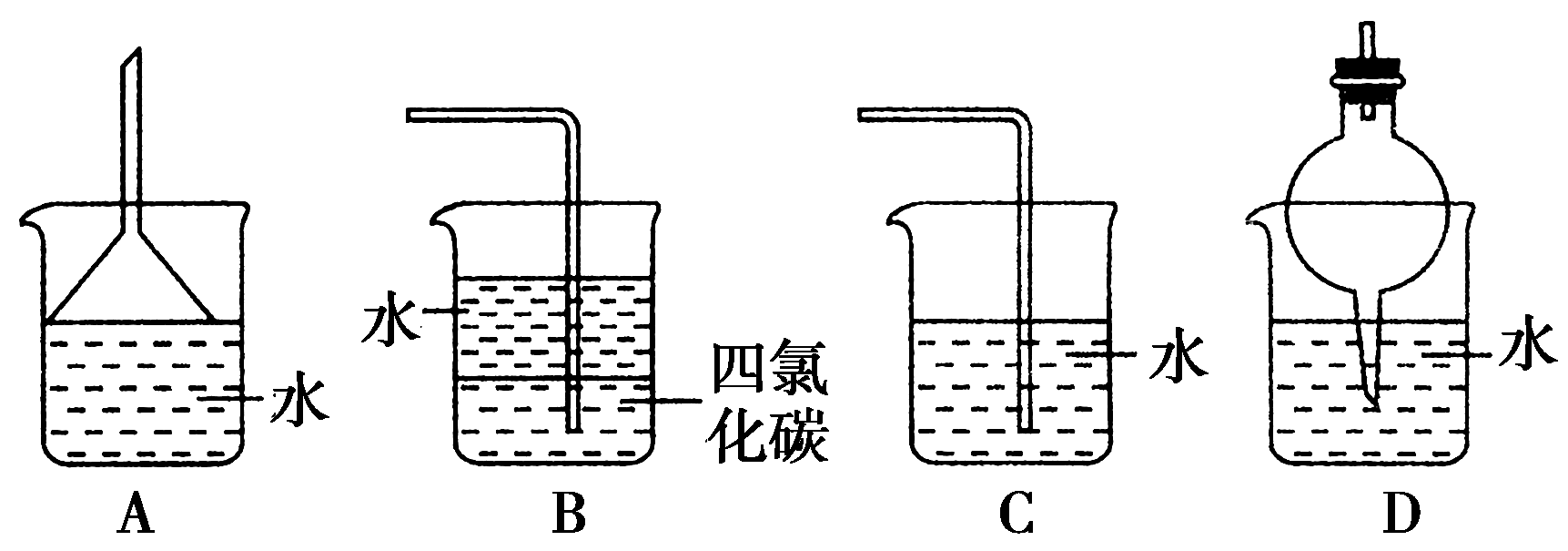
23.下列途径不能得到晶体的是( )
A.熔融态物质快速冷却 B.熔融态物质凝固
C.气态物质凝华 D.溶质从溶液中析出
24.下列物质有固定熔沸点的是( )
A.CuSO4溶液 B.石蜡
C.玻璃 D.白磷
25.如下图,在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )

A.十二面体 B.正八面体 C.正六面体 D.正四面体
第二部分:综合题(共3小题,共50分)
26.(每空2分,共16分)
I.有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:
II.元素周期表揭示了许多元素的相似性和递变规律,根据元素周期表元素的性质和递变规律,回答下列问题。
27.(每空2分,共18分)
A、B、C、D、E五种元素中,A原子3p轨道上成对电子数等于未成对电子数,B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同,C的价电子排布式为nsnnpn+2,D的核电荷数是A与C的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)A的最高价氧化物的化学式为_________,中心原子的VSEPR构型为_________。
(2)AC2与BC2分子的立体结构分别是__________和__________,相同条件下两者在水中的溶解度较大的是__________(写分子式),理由是____________________________
_______________________________________________________________________。
(3)D的元素符号是_________,它的核外电子排布式的简化式为____________。
(4)用氢键表示写出E的氢化物的水溶液中存在的所有氢键_____________________。
28.(每空2分,共16分)
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_____________。
(2)B的氢化物的分子空间构型是_____________。其中心原子采取_____________杂化。
(3)写出化合物AC2的电子式_____________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为_____________。
(4)E的核外电子排布式是_____________, ECl3形成的配合物的化学式为_____________,
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是__________________________。
2012-2016-2孔德学区高二第一次月考化学选修3答案
选择题答案(2*25=25)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 选项 | D | C | C | C | B | C | D | D | C | D | B | C | B |
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 选项 | D | D | D | B | B | B | C | B | C | A | D | B |
26.(2*8=16)
I.(1) S2-(2) K+(3)Cl-
II.(1) KOH(2) Ar K+HCl(答案合理即可) (3)S2-
27.(2*9=18)
(1)SO3平面三角形
(2)V形直线形SO2CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶原理”SO2在H2O中溶解度较大。
(3)Cr [Ar]3d54s1
(4)F-H...F F-H...O O-H...O O-H...F
28.(2*8=16)
(1)C<O<N(2)三角锥形 sp3
(3)![]() N2O
N2O
(4)1s22s22p63s23p63d54s1[Cr(NH3)4(H2O)2]Cl3
(5)4Mg + 10HNO3 = 4Mg(NO3)2+ NH4NO3+3H2O