
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
丰台区2015 ~2016学年度第一学期期末练习
高三化学
2016.1
满分:100分 考试时间:120分钟
可能用到的相对原子质量:
H-1 C-12 O-16 N-14
第一部分(选择题 共42分)
选择题(每题只有一个符合题意的选项,每题3分,共42分)
1.在下列自然资源的开发利用中,不涉及化学变化的是
A.用蒸馏法淡化海水 B.用铁矿石冶炼铁
C.用石油裂解生产乙烯 D.用煤生产水煤气
2. 下列化学用语正确的是
A.乙酸的结构简式 C2H4O2
![]() B. 氯化氢的电子式
B. 氯化氢的电子式
![]() C.镁的原子结构示意图
C.镁的原子结构示意图
D.水的电离方程式 H2O== H++OH-
3. 设NA为阿伏加德罗常数的值。下列说法正确的是
A.1 mol 18O含有的中子数为10NA
B.22.4L甲烷气体中所含分子数目为NA
C.1L 0.1 mol·L-1NH4Cl 溶液中NH4+数目为 0.1NA
D.1L pH=1的醋酸溶液中,CH3COOH分子的数目为0.1NA
4.下列表示物质用途的化学方程式不正确的是
A.用硅酸钠与盐酸反应制备硅胶:SiO32-+2H+==== H2SiO3(胶体)
高温
B.用二氧化硅与烧碱反应制备硅酸钠:SiO2+ OH-==== SiO32-+ H2OC.用铝热法炼铁:2Al+Fe2O3==== 2Fe+Al2O3
D.用氯气制备漂白粉:2Cl2+2Ca(OH)2==== CaCl2+Ca(ClO)2+2H2O
5.依据元素周期表及元素周期律,下列推断正确的是
A.碱性:Ca(OH)2>Mg(OH)2B.酸性:H3BO3>H2CO3
C.热稳定性:NH3< PH3D.还原性:S2-< F-
6. 下列物质的分类依据、类别、性质三者之间对应关系完全正确的是
| 物质 | 分类依据 | 类别 | 性质 | |
| A | FeCl2 | 铁元素化合价 | 还原剂 | 可与O2、Zn等发生反应 |
| B | FeCl2 | 电离产生的微粒 | 盐 | 可发生水解反应,溶液显碱性 |
| C | HNO3 | 在水中能电离出H+ | 酸 | 可与CuO反应生成NO |
| D | HNO3 | 氮元素的化合价 | 氧化剂 | 可与Al、I-等发生反应 |
7. 某同学在实验室利用氢氧化钠、盐酸分离铁粉和铝粉混合物,物质转化关系如下图所示:
下列说法不正确的是
8.将氯气分别通入下列溶液中,由实验现象得出的结论正确的是
| 选项 | 氯气通入下列溶液中 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液 | 变红 | 氯气具有还原性 |
| B | 滴有酚酞的NaOH溶液 | 褪色 | 氯气具有漂白性 |
| C | 紫色石蕊溶液 | 先变红后褪色 | 氯气具有酸性、漂白性 |
| D | 少量氯气通入大量水中 | 溶液pH<7 呈浅黄绿色 | 氯气与水反应生成酸性物质, 且该反应为可逆反应 |
9. 某同学研究浓度对化学平衡的影响,下列说法正确的是
| (橙色)(黄色)已知:Cr2O72-(aq) +H2O(l) | |
| 步骤: | 现象: 待试管b中颜色不变后与试管a比较,溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深。 |
D.试管c中的现象说明影响平衡的主要因素是温度
10.下列有关2个电化学装置的叙述正确的是
11.下列实验事实不能用基团间相互作用来解释的是
A.与Na反应时,乙醇的反应速率比水慢
B.苯酚能与NaOH溶液反应而乙醇不能
C.乙醇能使重铬酸钾溶液褪色而乙酸不能
D.苯、甲苯发生硝化反应生成一硝基取代产物时,甲苯的反应温度更低
12. 下列说法正确的是
A.蔗糖与麦芽糖都具有还原性,水解产物都是葡萄糖
B.淀粉和纤维素互为同分异构体,水解产物都是葡萄糖
C.蛋白质在酶的作用下,水解为多肽,最终生成氨基酸
D.植物油和动物油都是高级脂肪酸甘油酯,前者的饱和程度更高
13. 下列说法不正确的是
B.用质谱法可确定有机物分子中的官能团
C.用核磁共振氢谱能够区分CH3CH2CHO和CH3COCH3
. D. 乙二酸、甲醛、苯乙烯均可发生聚合反应
14.在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:
 C(s)+2NO(g)
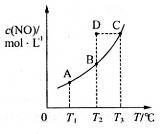
C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c(NO)与温度T的关系如下图所示,则下列说法正确的是
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如下图所示,则下列说法正确的是
![]() C.在T2时,若反应体系处于状态D,则此时
C.在T2时,若反应体系处于状态D,则此时
D.若状态B、C、D的压强分别为PB、PC、PD,则PC=PD>PB
第二部分 (非选择题 共58分)
15. (11分)某同学在实验室研究Na2CO3和NaHCO3的性质及相互转化。
(1)分别向浓度均为0.1mol/LNa2CO3及NaHCO3溶液中滴加几滴酚酞试剂:
① Na2CO3溶液由无色变为红色,其原因是 。
② NaHCO3溶液也由无色变为红色,其原因是 。
③ 比较两份溶液的颜色,红色较浅的是 (填化学式)。
(2)研究NaHCO3与CaCl2的反应。
| 实验序号 | 实验操作 | 实验现象 |
| 实验1 | 向2mL 0.001mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 无明显变化。用激光笔照射,没有出现光亮的通路。 |
| 实验2 | 向2mL 0.1mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 略显白色均匀的浑浊,用激光笔照射,出现光亮的通路。 |
① 实验1中没有出现白色浑浊的原因是 。
② 实验2中形成的分散系属于 。
③ 用离子方程式表示实验2中发生的反应 。
(3)在不引入其他杂质的前提下,实现Na2CO3与NaHCO3之间的转化,请在下图中标出所用的试剂、用量或物质的浓度(反应前后溶液体积的变化可忽略)。
催化剂
(10分)实验室利用下列装置模拟工业生产制备少量硝酸。B
A
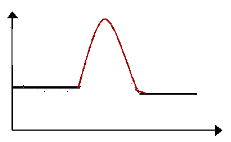
能
量
4NO(g)+6H2O(g)
4NH3(g)+5O2(g)
反应过程
D
C
① 当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。请用化学方程式表
示白烟产生的原因 。
② 欲使氨气尽可能完全转化为硝酸,理论上n(NH3):n(O2)的最佳比例为 。
17.(8分) 将氯碱工业与燃料电池联合能够有效降低能源消耗,下图是该工艺的图示(电源及电极未标出),请回答下列问题:
装置Ⅱ
| 实验操作 | 实验现象 |
| 向2mL mol/L 溶液(填化学式)中通入SO2 |
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | |
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线。 | 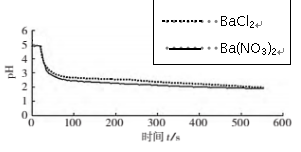 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2 |
已知:
ⅰ碳碳双键容易被氧化
![]()
1,2—加成
+Cl2
![]() ⅱ
ⅱ
![]()
1,4—加成
ⅲ
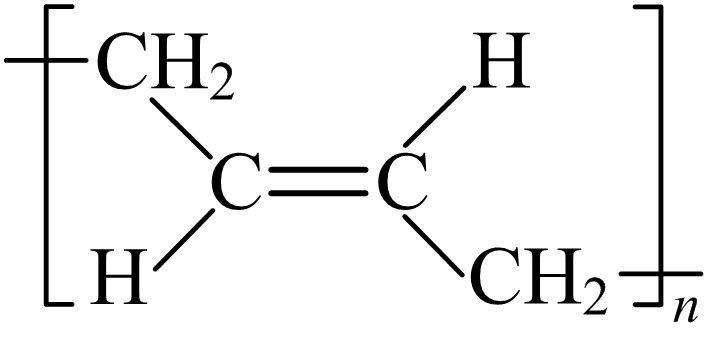
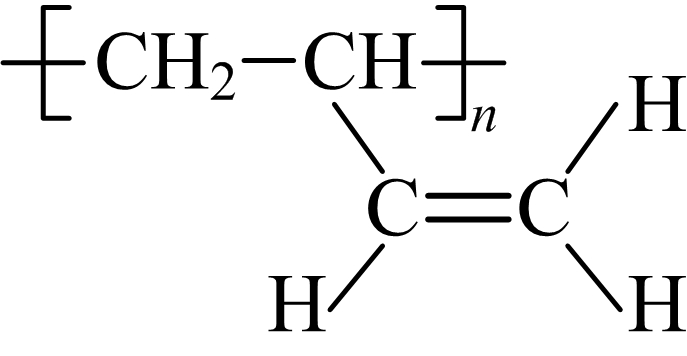
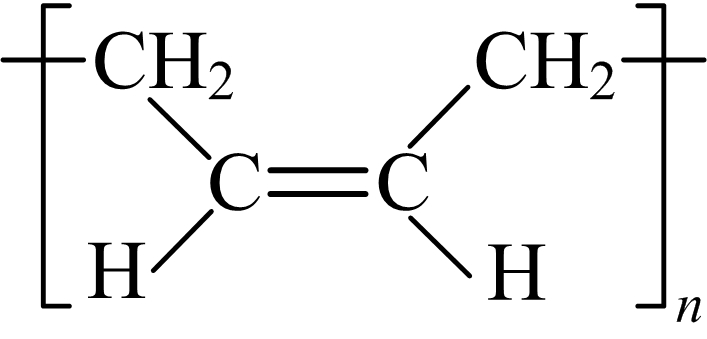
a. b. c.
(2)已知1molE发生银镜反应可生成4molAg。E中含氧官能团的名称为 。
(3)E由B经①、②、③合成。
a.①的反应试剂和条件是 。
b.②、③的反应类型依次是 、 。
(4)1molF转化成G所消耗的NaOH的物质的量为 mol。
(5)M的结构简式为 。
(6)完成下列化学方程式:
①EHPB不能与NaHCO3反应,有机物N →EHPB的化学方程式为 。
②有机物K与试剂x发生反应的化学方程式为 。
(7)有机物N有多种同分异构体,写出一种满足下列条件的同分异构体的结构简式 。
c. 苯环上的一氯代物只有一种 d.核磁共振氢谱有5组峰
丰台区2015 ~2016学年度第一学期期末练习
高三化学参考答案及评分标准
第Ⅰ卷(选择题 共42分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 答案 | A | C | A | B | A | D | D |
| 题号 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 | D | C | B | C | C | B | C |
第Ⅱ卷(非选择题 共58分)
说明:其他合理答案均可参照本标准给分,标记处每空2分,其余每空1分。
②胶体
③Ca2++2HCO3-=CaCO3↓+CO2+H2O
②2NO2(g)![]() 2NO(g)+ O2(g)ΔH>0,升高温度,平衡正向移动,有利于NO2的分解,因此难以生成NO2(2分)
2NO(g)+ O2(g)ΔH>0,升高温度,平衡正向移动,有利于NO2的分解,因此难以生成NO2(2分)
(5)①2NO+O2=2NO2,3NO2+H2O=2HNO3+NO,NH3+HNO3=NH4NO3(2分)(合理答案酌情给分)
②1:2
(4)A正极发生反应Cl2+2e-=2Cl-,负极发生反应H2-2e-=2H+,H+从负极经阳离子膜移动到正极,盐酸浓度增大(2分)
②3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+(2分)
③0.1 BaCl2试管内有白色沉淀产生
(3)SO2+H2O![]() H2SO3H2SO3
H2SO3H2SO3![]() HSO3-+H+(2分)
HSO3-+H+(2分)
(4)2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+(2分)
在BaCl2溶液中起氧化作用的是O2,在Ba(NO3)2溶液中起氧化作用的是O2和NO3-,而图2中,分别向BaCl2、Ba(NO3)2溶液中通入SO2,pH变化趋势、幅度接近,因此起氧化作用的主要是O2。(2分)
b. 加成反应 氧化反应
![]() (4)3
(4)3
(5) (2分)
(6)
① (2分)
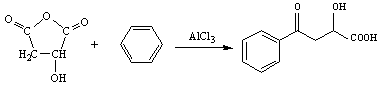
② (2分)
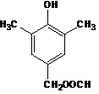
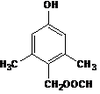
(7) 或者 (2分)