
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
淮南二中2017届高三年级第四次月考化学试卷
分值 100分 ; 时间90分钟
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Al-27 Fe-56 Cu-64 Zn-65
Sn-119 Cl-35.5 Ca-40
第Ⅰ卷 选择题(共51分)
一.选择题(本题包括17小题,每小题3分,共51分。每小题只有一个选项符合题意)
1.《汉书》中“高奴县有洧水可燃”,沈括在《梦溪笔谈》对“洧水”的使用有“予知其烟可用,试扫其烟为墨,黑光如漆,松墨不及也,此物必大行于世”的描述,对上文进行的某些分析中正确的是
A.“洧水”的主要成分是油脂 B.“洧水”的主要成分是煤油
C. 烟的主要成分是炭黑 D. 烟的主要成分是石油
2.设NA为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4L三氯甲烷中共价键数目为4NA
B.1mol碳烯(:CH2)所含电子总数为10NA
C.6.4gCaC2晶体中含有阴阳离子总数为0.2NA
D.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
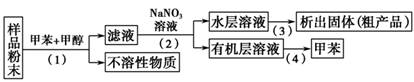 3.按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
3.按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
下列说法错误的是
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
4.铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法错误的是
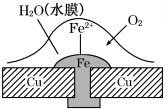 A.正极电极反应式为:2H++2e-===H2↑
A.正极电极反应式为:2H++2e-===H2↑
B.此过程中还涉及到反应:4Fe(OH)2+2H2O+O2===4Fe(OH)3
C.此过程中Cu并不被腐蚀
D.此过程中电子从Fe移向Cu
5.已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。下列说法不正确的是
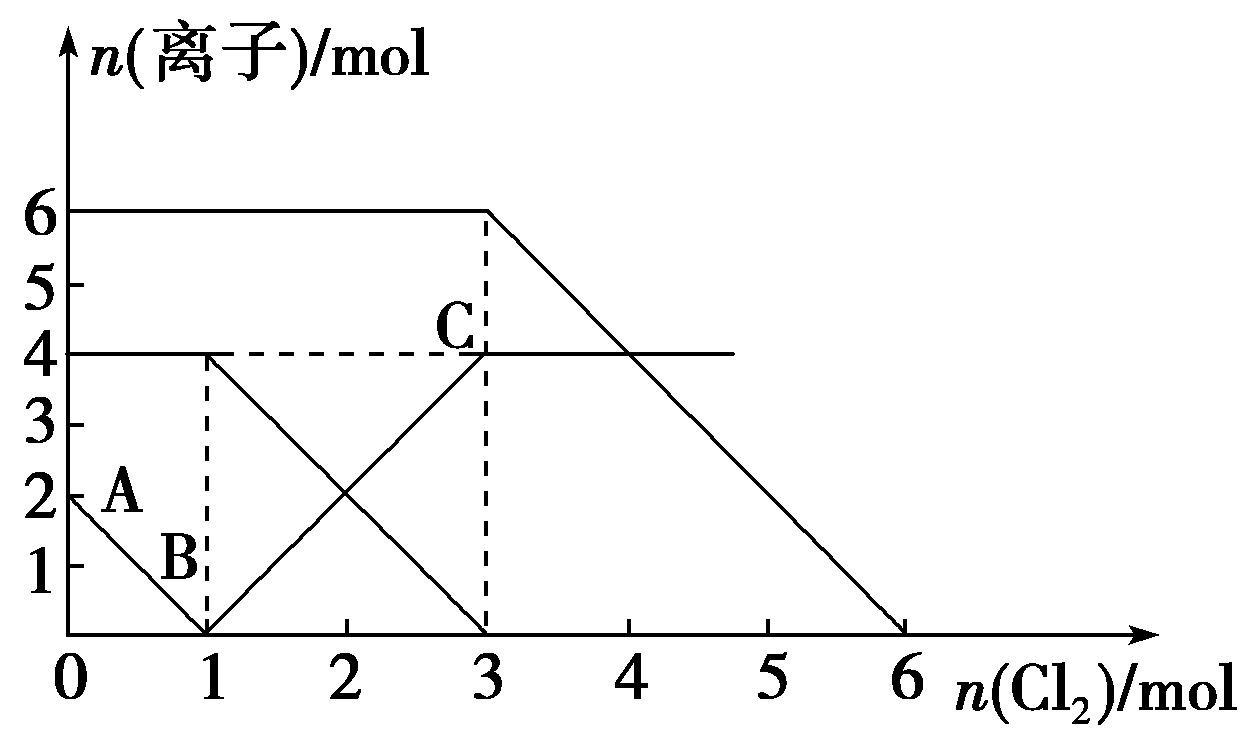 A.还原性:I->Fe2+>Br-
A.还原性:I->Fe2+>Br-
B.原混合溶液中FeBr2的物质的量为6 mol
C.当通入2 mol Cl2时,溶液中已发生的离子反应可表
示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
6.下列评价及离子方程式书写正确的是
| 选项 | 离子组 | 评价 |
| A | H+、Fe2+、NO3—、Cl— | 不能大量共存于同一溶液中,因为发生了氧化还原反应4Fe2++NO3—+6H+=4Fe3++2NO↑+3H2O |
| B | Na+、CO32—、Cl—、Al3+ | 不能大量共存于同一溶液中,因为发生了互促水解反应2Al3++3CO32—+3H2O=2Al(OH)3↓+3CO2↑ |
| C | Fe3+、K+、SCN—、Br— | 不能大量共存于同一溶液中,因为有红色沉淀生成 Fe3++3SCN—===Fe(SCN)3↓ |
| 资*源%库D | HCO3—、OH—、Na+、Ca2+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3—+OH—===CO2↑+H2O |
7.下列装置能达到实验目的的是
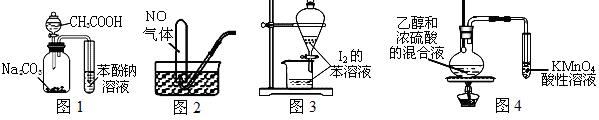
A.图1证明酸性:CH3COOH>H2CO3>苯酚 B.图2用排水法收集NO
C.图3萃取碘水中I2,分出水层后的操作 D.图4验证乙烯的生成
8.下列物质的转化在给定条件下能实现的是
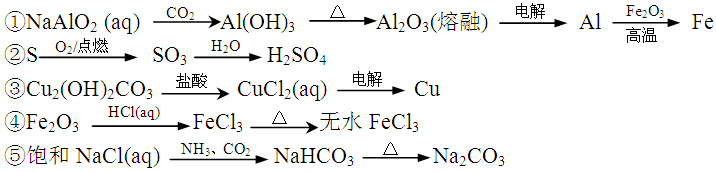
A.①③⑤ B.②③④ C.②④⑤ D.①④⑤
9.水热法制备Fe(FeO2)2纳米颗粒反应3Fe2++2S2O32﹣+O2+xOH﹣= Fe(FeO2)2+S4O62-+ 2H2O.
下列说法中,不正确的是
A.该反应中Fe2+和S2O32﹣都是还原剂
B.3molFe2+被氧化时有1molO2被还原
C.每生成1mol Fe(FeO2)2转移4mol电子
D.反应方程式中化学计量数x=4
10.短周期元素W、X、Y、Z在元素周期表中的位置如表所示下列说法中正确的是
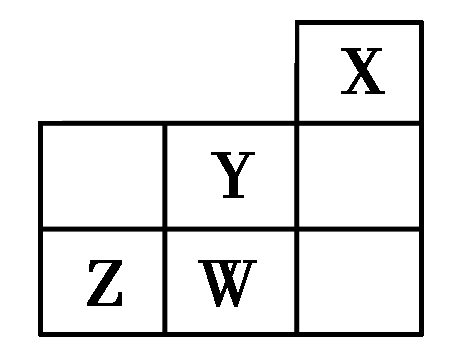 A.W的最高价氧化物对应的水化物是强酸
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
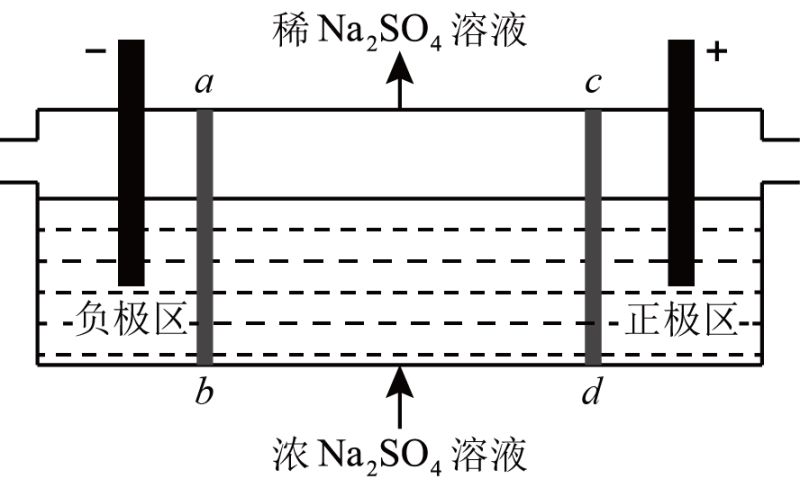 11、三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
11、三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
A.通电后中间隔室的SO42-向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
12.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A.在含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+
B.在含等物质的量的Al3+、NH4+、H+的溶液中滴加KOH溶液:H+、NH4+、 Al3+
C.在含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D.在含等物质的量的AlO2﹣、OH﹣、CO32﹣的溶液中,逐滴加入盐酸:AlO2﹣、OH﹣、CO32-
13.下面是利用盐桥电池从某些含碘盐中提取碘的两个装置:
下列说法中正确的是 ( )
A.两个装置中石墨I和石墨II作负极
B.碘元素在装置①中被还原,在装置②中被氧化
C.①中MnO2的电极反应式为:MnO2+2H2O+2e-==Mn2++4OH-
D.反应①、②中生成等量的I2时导线上通过的电子数之比为1∶5
14.W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Z是非金属元素,W、X的最高价氧化物对应的水化物可以相互反应生成盐和水,向一定量的W的最高价氧化物对应的水化物溶液中逐滴加入XZ3溶液,生成的沉淀X(OH)3的质量随XZ3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是
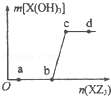 A.d点对应的溶液中:K+、NH4+、CO32﹣、I﹣
A.d点对应的溶液中:K+、NH4+、CO32﹣、I﹣
B.c点对应的溶液中:Ag+、Ca2+、NO3﹣、Na+
C.b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
D.a点对应的溶液中:Na+、K+、SO42﹣、HCO3﹣
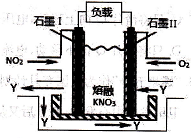 15. NO2、O2和熔融KNO3可制作燃料电池,其原理如下图所示。该电池在放电过程中石墨 I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
15. NO2、O2和熔融KNO3可制作燃料电池,其原理如下图所示。该电池在放电过程中石墨 I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
A.放电时,N03一向石墨Ⅱ电极迁移
B.石墨Ⅱ附近发生的反应为: NO+O2+e一=NO3一
C.电池总反应式为:4NO2+O2 = 2N2O5
D.当外电路通过4mol e一,负极上共产生2mol N2O5
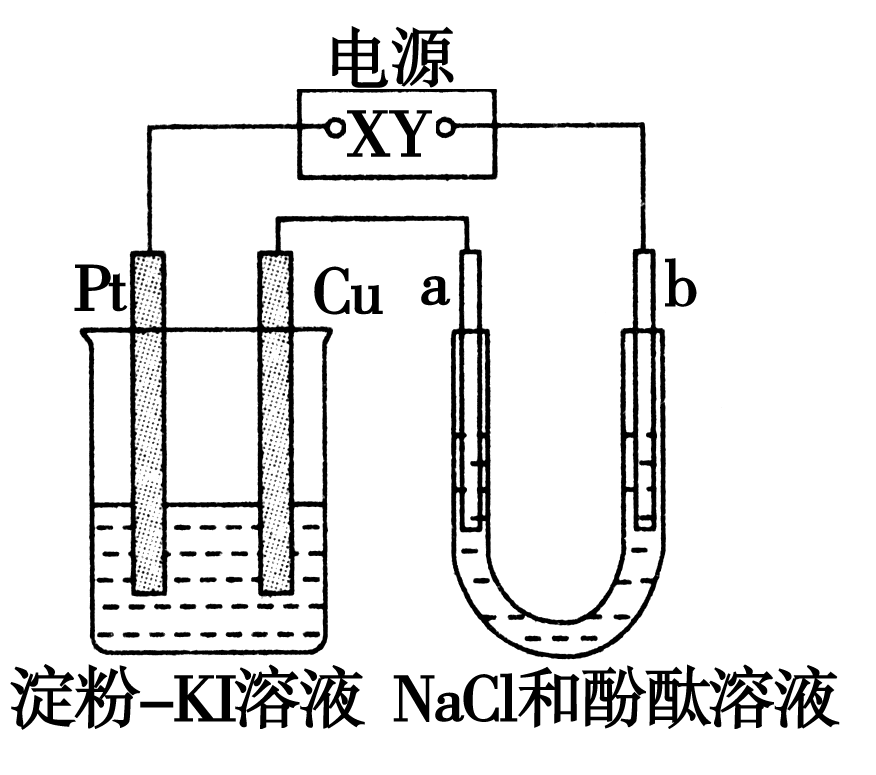 16.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到。如图所示装置中,a、b都是惰性电极,通电一段时间后,在淀粉-KI溶液中阳极周围变蓝色,则下列说法一定正确的是:
16.CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到。如图所示装置中,a、b都是惰性电极,通电一段时间后,在淀粉-KI溶液中阳极周围变蓝色,则下列说法一定正确的是:
A.淀粉-KI溶液中,Cu电极为阳极
B.淀粉-KI溶液中,Pt电极上有:2 H2O-4e-=4H++O2↑
C.NaCl和酚酞溶液中,Na+向b极迁移
D.NaCl和酚酞溶液中,ab两极均有气泡产生
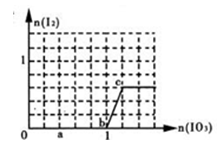
17.已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图(不考虑I2+I-![]() I3-)下列说法不正确的是
I3-)下列说法不正确的是
A.a点时消耗NaHSO3的物质的量为1.2mol,得到的氧化产物为SO42-
 B.b~c段的反应可用如下离子方程式表示:IO3-+5I-+6H+=3I2+3H2O
B.b~c段的反应可用如下离子方程式表示:IO3-+5I-+6H+=3I2+3H2O
C.滴加过程中水的电离平衡一直逆向移动。
D.从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏
第Ⅱ卷非选择题(共49分)
二.非选择题(本题包括3小题,共38分。)
18.(14分)铁及其化合物是常见的化学物质。
(1)已知:铝的燃烧热为1675kJ•mol-1;
2Fe(s)+3/2 O2(g)═Fe2O3(s);△H=-822kJ•mol-1;
则 2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s); △H=______;
(2)钢铁的“烤蓝”是钢铁防腐的一种方法。“烤蓝”通常是在加热条件下用NaNO2碱性溶液处理钢铁部件,使其表面形成致密的Fe3O4保护膜,且有能使湿润的红色石蕊试纸变蓝的气体生成,反应的离子方程式为_________________________;
(3)K2FeO4是一种重要的试剂,可用下列电解方法制备:
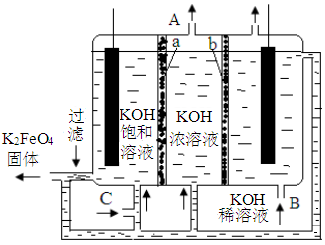
①以铁丝网和石墨为电极,石墨接电源的_____极;铁丝网的电极反应为___________。
②A口出来的溶液补充适量的_____从B口进入电解槽,C口补充适量的_____(填化学式)。
③上述电解的副产物为_______________________。
19.(12分)硫酸的工业制备是一个重要的化工生产过程,但在生产过程中会产生大量污染,需要在生产工艺中考虑到绿色工艺。以硫酸工业产生的二氧化硫尾气、氨水、石灰石、焦炭、碳酸氢铵为原料可以合成硫化钙、硫酸铵、亚硫酸铵等物质。合成路线如下:
(1)写出反应Ⅰ的化学方程式 。
(2)反应Ⅲ中每生成1mol硫化钙理论上转移电子数 ;为充分利用副产品CO,有人提出以熔融的K2CO3为电解质,设计燃料电池,请写出此电池的负极反应 。
(3)为检验反应Ⅱ得到的产品是否因部分被氧化而变质,需选择的化学试剂有 。
(4)根据合成流程,可以循环利用的是 。
(5)(NH4)2SO3溶液可用于电厂产生的烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的离子方程式 。
20.(12分)某实验研究小组欲检验草酸晶体分解的产物并测定其纯度(杂质不发生反应)。查阅资料:草酸晶体( H2C2O4·2H2O) l00℃开始失水,101. 5C熔化,150℃左右分解产生H2O、CO和 CO2。下面是可供选择的实验仪器(图中某些加热装置已略去),实验所需药品不限。
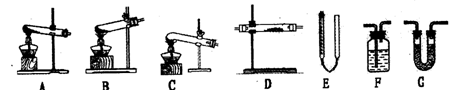
(l)最适宜加热分解草酸晶体的装置是C。若选装置A可能会造成的后果是____ ;
若选装置B可能会造成的后果是____ 。
(2)三种气体检验的先后次序是____ (填编号)。
(3)实验利用装置“G(碱石灰)-F-D(CuO固体)-F”检验CO,则F中盛装的试剂是
___ _,证明含有CO的现象是____ ____ ____ 。
(4)把分解装置与装有NaOH溶液的E装置直接组合,测量完全分解后所得气体的体积,
测定ag草酸晶体的纯度。经实验得到气体的体积为V mL(已换算成标准状况),则草酸
资*源%库 纯度的表达式为____。
三.选做题。(本题包括2小题,任选一题作答,并填涂选作标记。)
资*源%库21 [化学—选修3:物质结构与性质] (11分)
安徽省具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题,
(1)请写出基态Cu原子的外围电子排布式 。
焰火中的绿色是铜的焰色,基态铜原子在灼烧时外围电子发生了 而变为激发态。
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式
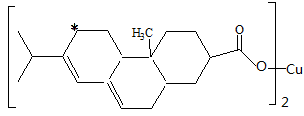
请分析1个松脂酸铜中π键的个数 ;加 “*”碳原子的杂化方式为 。
(3)下图是某铜矿的晶胞图,请推算出此离子晶体的化学式(以X表示某元素符号) ;与X等距离且最近的X原子个数为
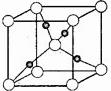
X原子 Cu原子
(4)黄铜矿在冶炼的时候会产生副产品SO2,SO2分子的几何构型 ,比较第一电离能:S O(填“>”或“<”)
(5)黄铜合金可以表示为Cu3Zn,为面心立方晶胞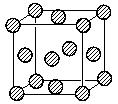 ,晶体密度为8.5g/cm3,求晶胞的边长(只写计算式,不求结果)。 。
,晶体密度为8.5g/cm3,求晶胞的边长(只写计算式,不求结果)。 。
22.[化学——选修5:有机化学基础](11分)
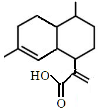
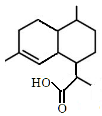
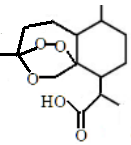
上海交通大学科研团队历时7年,研发出一种合成路线短、收率高、适合于大规模工业化生产的青蒿素化学合成方法。其主要合成路线如下:
![]()
![]()
![]()
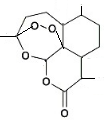
A B C 青蒿素
回答下列问题:
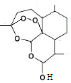 ,则C与双氢青蒿素的关系是__________。
,则C与双氢青蒿素的关系是__________。A、分子中含有酯基、醚键和过氧键
B、化学性质不稳定
C、能发生还原反应
D、利用红外光谱谱图可鉴别出C和青蒿素
(5)应用学过的知识,以![]() 为原料合成B,写出其合成路线(指明所用试剂和反应条件):__________________________________。
为原料合成B,写出其合成路线(指明所用试剂和反应条件):__________________________________。
淮南二中2017届高三第四次月考化学参考答案
选择题(每题3分,共17题。) CCCAB BBABA BADCC DC
18.(14分)
(1)△H=—-2528kJ·mol—1(2分)
(2)9Fe+4NO2—+8H2O==3Fe3O4+4NH3+4OH—(2分)
Fe—6e—+8OH—+2K+= K2FeO4↓+4H2O (2分)
② H2O (2分)
KOH (2分)
③ H2(2分)
19(12分)
(1)2CaCO3+O2+2SO2=2CaSO4+2CO2(2分)
(2)8NA(2分)
CO+CO32--2e-=2CO2(2分)
(3)稀盐酸 BaCl2溶液 (2分)
(4)CaCO3(2分)
(5)2NO2+4SO32-=N2+4SO42-(2分)
20.(12分)
(1)固体药品熔化后会流到试管口; (2分)
冷凝水会倒流到试管底,造成试管破裂; (2分)
(2)C (2分)
(3)澄清石灰水 (2分)
前一个F中未变浑浊,后一个F中有白色浑浊;且D中固体由黑变红。 (2分)
(4) (2分)
(2分)
21. (11分)
(1)3d104s1(1分) 跃迁(1分)
(2)6(1分) sp3(1分)
(3)Cu2X(1分) 8(1分)
(4)折线形(V形或角形)(1分)< (1分)
(5)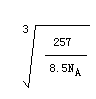 cm或者
cm或者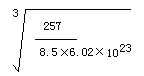 (3分)
(3分)
22.(11分)
(1)碳碳双键、羧基 (2分) 相同 (1分)
(2)还原反应 氧化反应 (2分)
(3)同分异构体 (1分)
(4)ABCD (2分)
(5)![]()
![]()
![]()
![]()
![]()
![]()
![]() (3分)
(3分)