
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 河北定州中学2017—2018学年度第一学期期末考试
河北定州中学2017—2018学年度第一学期期末考试
高四年级 化学试卷
一、单选题
1.下列说法不正确的是
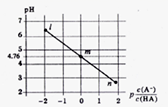
2.常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示【已知:P[c(A-)/c(HA)]=-1g[c(A-)/c(HA)]】。下列叙述不正确的是
3.25℃时,下列有关电解质溶液的说法正确的是( )
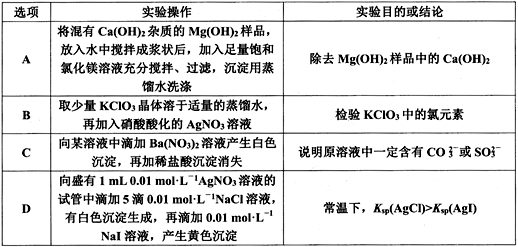
4.下表中的实验操作能达到实验目的或能得出相应结论的是( )
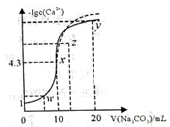
5.某温度下,向10mL0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液(此时不考虑CO32-的水解),滴加过程中溶液中-lgc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是
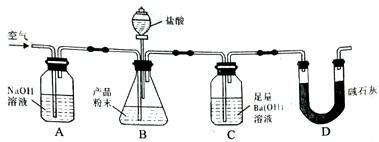
6.某实验小组设计如下实验装置(图中夹持装置省略)测定制备的CaCO3粉末的纯度(样品中杂质不与酸反应,反应前装置中的CO2已全部排出)。下列说法错误的是
7.设NA为阿伏加德罗常数的值,下列说法正确的是
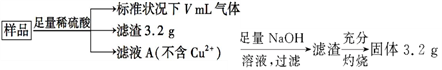
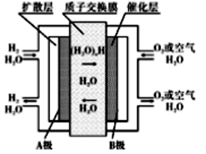
9.质子交换膜燃料电池(简称:PEMFC),又称固体高分子电解质燃料电池,是一种以含氢燃料与空气作用产生电力与热力的燃料电池,膜极组和集电板串联组合成一个燃料电池堆。目前,尤以氢燃料电池倍受电源研究开发人员的注目。它的结构紧凑,工作温度低(只有80℃),启动迅速,功率密度高,工作寿命长。工作原理如图,下列说法正确的是
10.实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 | 实验目的 | 主要仪器 | 所用试剂 |
| A | 检验石蜡油的分解产物 | 硬质试管、酒精灯 | 石蜡油、石棉 |
| B | 鉴别葡萄糖和蔗糖 | 试管、酒精灯 | 葡萄糖溶液、蔗糖溶液、新制氢氧化铜悬浊液 |
| C | 测盐酸的浓度 | 滴定管、锥形瓶、烧杯 | 标准氢氧化钠溶液、待测盐酸溶液、石蕊溶液 |
| D | 铝热反应 | 试管、酒精灯 | 铝粉、氧化铁 |
11.己知烯烃X与氢气反应的热化学方程式为X(g)十H2 (g)=Y(g) △H<0,其中烃Y的键线式为“王”字,下列有关说法不正确的是
12.标准状况下,下列说法正确的是
13.根据下表信息,将乙二醇和丙三醇分离的最佳方法是
| 物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度/g·cm–3 | 溶解性 |
| 乙二醇 | C2H4O2 | –11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
14.草莓酸的结构简式为CH3CH2CH=C(CH3)COOH,以下说法错误的是
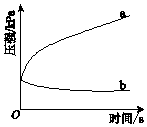
15.生铁在pH=2和pH=4的盐酸中发生腐蚀.在密闭容器中,用压强传感器记录该过程的压强变化,如图所示.下列说法中,不正确的是( )
16.已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO。利用如图装置用正丁醇合成正丁醛。相关数据如表:
CH3CH2CH2CHO。利用如图装置用正丁醇合成正丁醛。相关数据如表:
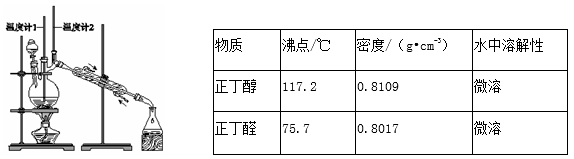
下列说法中,不正确的是
17.298K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) △H=-akJ/mol(a>0).N2O4的物质的量浓度随时间变化如图.达平衡时,N2O4的浓度为NO2的2倍,
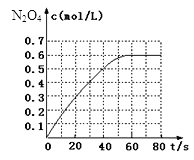
若反应在398K进行,某时刻测得n(NO2)=0.6mol、n(N2O4)=1.2mol,则此时,下列大小关系正确的是
C. v(正)=v(逆) D. v(正)、v(逆)大小关系不确定
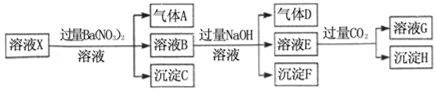
18.pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )
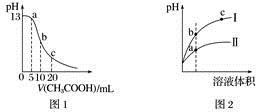
19.根据下列各图曲线表征的信息,得出的结论不正确的是

20.在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应:2CO(g)+SO2(g) S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
| 容器 | 起始时物质的量/mol | 平衡时CO2(g)的物质的量/mol | |||
| CO(g) | SO2(g) | S(g) | CO2(g) | ||
| 甲 | 1 | 0.5 | 0.5 | 0 | a |
| 乙 | 1 | 0.5 | 0 | 0 | 0.8 |
| 丙 | 2 | 1 | 0 | 0 | b |
下列说法正确的是
二、推断题
21.某化学兴趣小组利用以下线路合成有机化合物F:
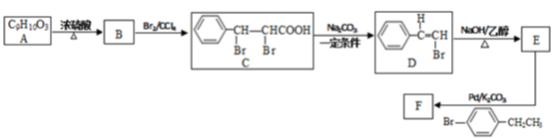
已知:R-C≡CH+R´-Br![]() R-C≡C-R´+HBr
R-C≡C-R´+HBr
(1)B中官能团的名称是______,E的化学名称是_______;
(2)F的结构简式为____,由D生成E的反应类型是_______;
(3)试推断在核磁共振氢谱中A有多少组峰__;
A.8 组 B.9 组 C.7 组
(4)写出C与足量NaOH 溶液在加热条件下反应的化学方程式:____________;
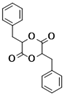
(5)2 分子A在一定条件下反应生成一种含有3个六元环的化合物,该生成物的结构简式为_______ ;
(6) 同时满足下列条件的A 的同分异构体有___种( 不考虑立体异构)。
①属于芳香族化合物;
②能与碳酸氢钠溶液反应生成CO2;
③在一定条件下能发生催化氧化,且其产物能发生银镜反应。
三、综合题
22.高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64% (均为体积分数)。某科研小组对尾气的应用展开研究:
I.直接作燃料
己知:C(s)+O2(g)=CO2 (g) △H=-393.5kJ/mol
2C(s)+O2(g)=2CO (g) △H=-221kJ/mol
(1)CO燃烧热的热化学方程式为____________________________________________________________________________ 。
II.生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:
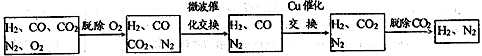
在脱氧过程中仅吸收了O2;交换过程中发生的反应如下,这两个反应均为吸热反应:CO2+CH4![]() CO+H2CO+H2O
CO+H2CO+H2O![]() CO2+ H2
CO2+ H2
(2)气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原因:____________________________________________________________________________ 。
(3)通过铜催化交换炉后,所得气体中V(H2):V(N2)= ______________。
III.合成氨后的气体应用研究
(4)氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该科研小组在恒温条件下,向2L恒容密闭容器中加入0.2molNO 和0.1molCl2,发生如下反应:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0。10min时反应达平衡,测得10min 内v (ClNO)=7.5
2ClNO(g) △H<0。10min时反应达平衡,测得10min 内v (ClNO)=7.5![]() 10-3mol/(L·min),则平衡后n(Cl2)=_________mol。
10-3mol/(L·min),则平衡后n(Cl2)=_________mol。
设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO 的转化率为α2,则α1____α2(填“>”、“<”或“=”);平衡常数K____ (填增大”“减小 ”或“不变”)
(5)氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为_____________________________。
参考答案
CDBAD CDCBB DCBCC DBCBC
21. 碳碳双键、羧基 苯乙炔 ![]() 消去反应 C
消去反应 C ![]()
 17
17
22. CO(g)+1/2O2(g)=CO2(g) ΔH=-283kJ/mol 该反应是吸热且熵增的反应,只有在较高温度下ΔG=ΔH-TΔS 才有可能小于0,反应才有利于自发进行 88.36∶55(或1.61∶1或8∶5) 0.025 < 不变 HC1O+2C1O2-+H+=2ClO2↑+Cl-+H2O