2015-2016学年高三化学期中测试题
可能用到的相对原子质量:Cu:64 Fe:56 S:32 O:16 Ca:40 Si:28 Na:23 Cl:35.5
Al:27 N:14 C:12
一、选择题(每题有且只有一个选项符合题意,每题3分共48分)
1、下列叙述错误的是 ( )
A.葡萄糖注射液不能产生丁达尔效应,不属于胶体
B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
C.明矾和漂白粉常用于自来水的净化和杀菌流消毒,两者原理相同
D.化学变化中一定有能量变化,而有能量变化过程不一定发生化学反应
2.下列装置、试剂选用或操作正确的是( )
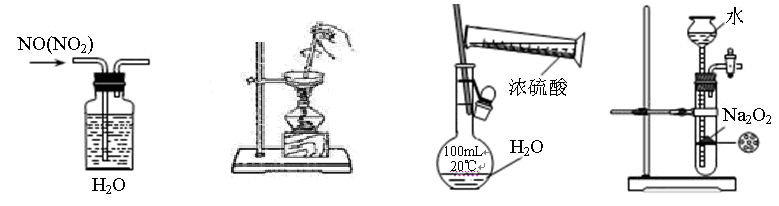
A.除去NO中的NO2B.用于AlCl3蒸发结晶C.稀释浓硫酸D.制备少量O2
3、以下除杂方案不正确的是( )
A. Cl2中混有HCl,可依次通入盛有饱和食盐水、浓H2SO4的洗气瓶
B. NH4Cl 溶液中混有Fe3+,可加入NaOH溶液后过滤
C. CO中混有CO2,可依次通入盛NaOH 溶液、浓 H2SO4的洗气瓶
D. Na2CO3固体中混有NaHCO3,可用加热的方法除尽
4.下列选项中有关离子方程式的书写正确的是( )
A.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑
B.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C.过量的CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O=HCO3-+HClO
D.硫化钠水溶液呈碱性的原因:S2-+2H2O=H2S+2OH-
5.设NA为阿伏加德罗常数的值,下列各项叙述正确的是 ( )
①1 molCl2参加反应转移电子数一定为2NA
②1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
③1L 2mol·L-1的Al(NO3)3溶液中含Al3+个数为2NA
④1 L 2 mol/L的氯化铁溶液完全制成胶体,氢氧化铁胶体的粒子数小于2 NA
⑤6.0 g SiO2晶体中含有的硅氧键数目为0.4 NA
⑥标准状况下,2.24 L乙醇分子所含的C-H键数为 0.5NA
- ①③④ B.①③⑤ C.②④⑤ D.②④⑥
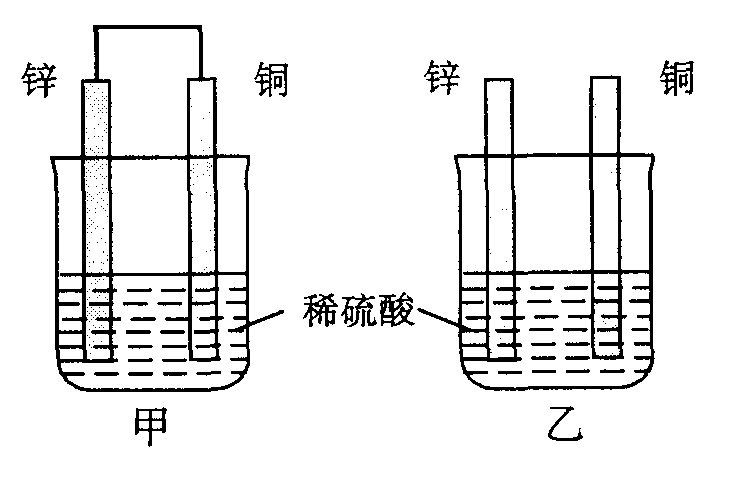 6. 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
6. 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
A. 两烧杯中铜片表面均无气泡产生 B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均增大 D. 产生气泡的速度甲比乙慢
7.常温下,下列各组离子在指定溶液中能大量共存的是 ( )
A.Kw/c(H+)=1 mol·L-1的溶液中:Na+、SiO32-、I-、CO32-
B.氨水中:Al3+、K+、F-、NO3-
C.pH=1的溶液中:NH4+、Na+、SO42-、CH3COO-
D.0.1 mol·L-1的NaHSO4溶液中:K+、Fe2+、Cl-、NO3-
8.己知在碱性溶液中可发生如下反应:
2R(OH)3 + 3C1O-+ 4OH- = 2RO4n-+3Cl-+5H2O。则RO4n-中r的化合价是( )
A.+3B.+4C.+5D.+6
9.A~D是含同一元素的四种物质,相互之间有如图所示的转化关系,其中D是最高价氧化物对应的水化物。那么A可能是( )
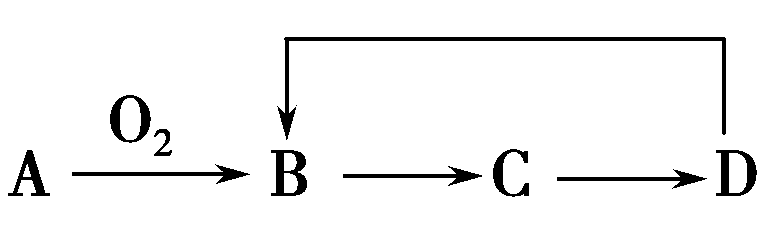 ①N2 ②Si ③Cu ④CH4 ⑤H2S
①N2 ②Si ③Cu ④CH4 ⑤H2S
A.只有①④⑤B.只有①②③C.只有①⑤D.全部
10.可逆反应2SO2(g)+O2(g) 2SO3(g) ;△H<0, 在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间的关系如右图所示。
2SO3(g) ;△H<0, 在一定条件下达到平衡状态,时间为t1时改变条件。化学反应速率与反应时间的关系如右图所示。
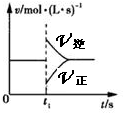 下列说法正确的是( )
下列说法正确的是( )
A. 维持温度、反应体系容积不变,t1时充入SO3(g)
B. 维持压强不变,t1时升高反应体系温度
C. 维持温度、容积不变,t1时充入一定量Ar
D. 维持温度、压强不变,t1时充入SO3(g)
11.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO2所表现的化学性质或作用进行判断,a~e的叙述中有几个正确的选项( )
①SiO2+2NaOH===Na2SiO3+H2O②SiO2+2CSi+2CO↑
③SiO2+4HF===SiF4↑+2H2O④Na2CO3+SiO2Na2SiO3+CO2↑
⑤SiO2+3CSiC+2CO↑
a.反应①中SiO2作为玻璃的成分被消耗,用于刻蚀玻璃
b.反应②中SiO2表现出氧化性
c.反应③中SiO2表现了酸性氧化物的通性
d.反应④符合用较强酸制取较弱酸的道理
e.反应⑤中SiO2未参加氧化还原反应
A.二个B.三个C.四个D.五个
12.下列说法正确的是( )
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,0.5mol N2和1.5molH2置于密闭容器中充分反应生成氨气,放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)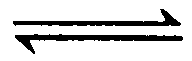 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g)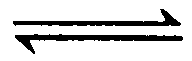 H2O(l)的ΔH=+40.69 kJ·mol-1
H2O(l)的ΔH=+40.69 kJ·mol-1
D.酸碱发生中和反应生成1mol液态H2O时,所放出的热量称为中和热,可表示为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ·mol-1
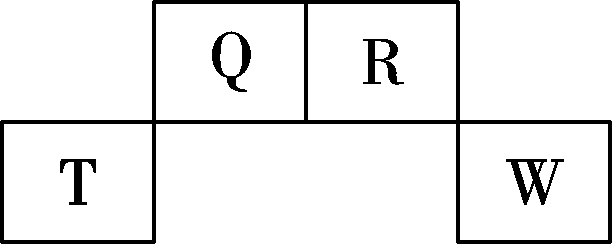 13.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8∶3,下列说法正确的是( )
13.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8∶3,下列说法正确的是( )
A.Q的最高价氧化物对应水化物的酸性大于R的最高价氧化物对应水化物的酸性
B.T的离子半径大于W的离子半径
C.元素T形成单质的还原性大于元素W形成单质的还原性
D.在R的最高价氧化物对应水化物的浓溶液中单质T不溶解,说明未发生化学反应
14. 下列实验可达到实验目的的是( )
A.将2-氯丙烷与NaOH的醇溶液共热制备CH3—CH═CH2
B.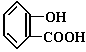 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备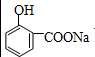
C.用分液法分离苯和液溴的混合物
D.向卤代烃水解后的溶液中直接加入硝酸银溶液,可以确定卤代烃中的卤元素
15.已知0.1 mol·L-1的二元酸H2A溶液的pH=4.0,则下列说法正确的是( )
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-)
 16.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是 ( )
16.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是 ( )
A.该反应的化学方程式为3X+Y===2Z
B.2 min时,反应达最大限度,但化学反应仍在进行
C.反应开始至2 min,Z的反应速率为0.05 mol·L-1·min-1
D.反应达到平衡时,压强是开始时的0.9倍
二、非选择题(共52分)
17.(一)化学实验有助于理解化学知识,形成化学观念。在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
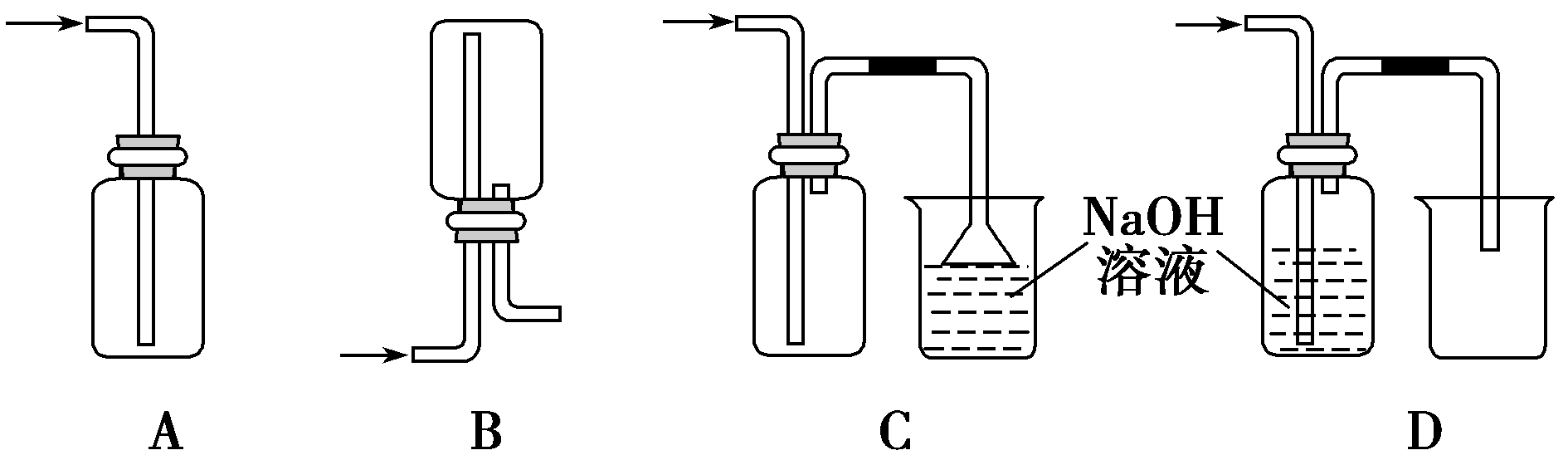 (1)下列收集Cl2的正确装置是________。
(1)下列收集Cl2的正确装置是________。
(2)将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是______________。
(3)设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,__________________________________________________________。
(二)某学生对SO2与漂粉精(漂白粉)的反应进行实验探究:| 操作 | 现象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |

A | ⅰ.液面上方出现白雾;
ⅱ.稍后,出现浑浊,溶液变为黄绿色;
ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
- Cl2和Ca(OH)2制取漂粉精的化学方程式是_________________________。
- 用离子方程式解释漂粉精溶液使pH试纸变蓝的原因________________。
- pH试纸颜色的变化说明漂粉精溶液具有的性质是________________。
- 将A瓶中混合物过滤、洗涤,得到沉淀X,向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
18.某无色废水中可能含有H+、NH、Fe3+、Al3+、Mg2+、Na+、NO、CO、SO中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关图像如下所示:
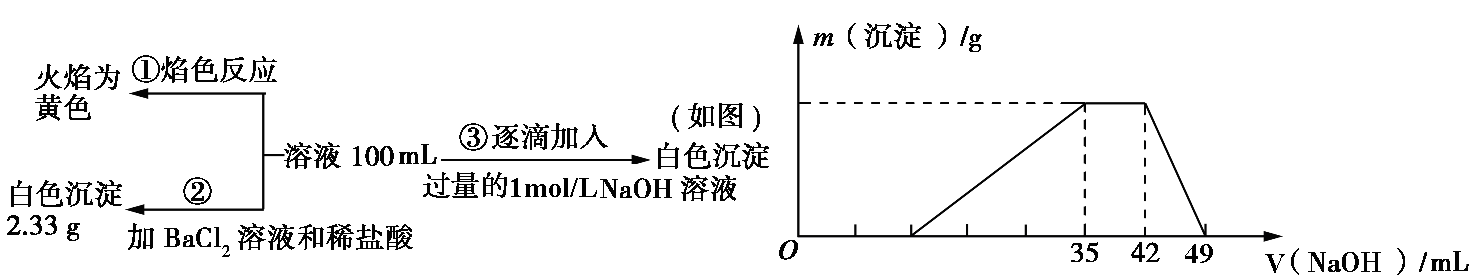
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有:。
(2)写出实验③图像中沉淀溶解阶段发生的离子反应方程式:
(3)分析图像,在原溶液中c(NH)与c(Al3+)的比值为。
NO是否存在?填(“存在”“不存在”或“不确定”)。
19. 高锰酸钾是一种典型的强氧化剂。完成下列填空:
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①8MnO+5Cu2S+44H+==10Cu2++5SO2↑+8Mn2++22H2O(已配平)
②MnO+CuS +H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是(填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
MnO4-+Fe2++H+=Mn2++Fe3++H2O
(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为g。需要的玻璃仪器有
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(4)用软锰矿制备K2MnO4的化学方程式是:。
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为。
20.氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
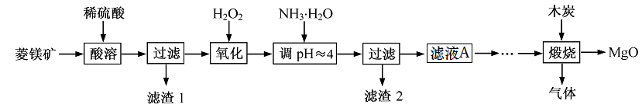
- 为了加快菱镁矿的溶解,在酸溶阶段可以采取的措施有(任写一条)
。
MgCO3与稀硫酸反应的离子方程式为。
(2)加入H2O2氧化时,发生反应的离子方程式为。
(3)滤渣2 的成分是(填化学式)。滤液A的主要成分有(填化学式)
(4)煅烧过程存在以下反应:
2MgSO4(s)+C(s) 2MgO(s)+2SO2(g)+CO2(g) ∆H1
2MgO(s)+2SO2(g)+CO2(g) ∆H1
MgSO4(s)+C(s) MgO(s)+SO2(g)+CO(g) ∆H2
MgO(s)+SO2(g)+CO(g) ∆H2
那么CO2(g) +C(s) 2CO(g) ∆H
2CO(g) ∆H 。
。
21.对甲乙苯是一种重要的有机原料,用该物质可合成其他物质。

图Z171
已知:①1 mol D与足量钠反应可生成1 mol氢气;
②D、E、F每种分子中均只含有一种含氧官能团。
③G是一种有机高分子化合物。
回答下列问题:- 对甲乙苯的系统命名为________________;A的结构简式为________________。
- A→B的反应类型为________________;F中含氧官能团的名称为________________。
- 1 mol E和足量银氨溶液反应,生成沉淀的物质的量为______________。
- D+F→G的化学方程式为____________________________________________
- H比D相对分子质量小14,H的同分异构体能同时满足如下条件:
①苯环上有两个取代基;
②遇氯化铁溶液显紫色;
③核磁共振氢谱为六组峰,且峰面积比为2∶2∶2∶2∶1∶1。
写出H的这种同分异构体的简式:______________。


 6. 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )
6. 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )  下列说法正确的是( )
下列说法正确的是( )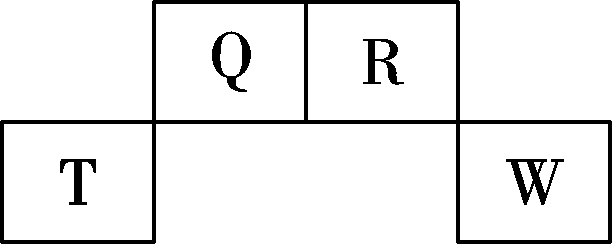 13.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8∶3,下列说法正确的是( )
13.短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8∶3,下列说法正确的是( )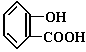 与适量NaOH溶液反应制备
与适量NaOH溶液反应制备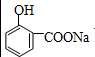
 16.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是 ( )
16.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是 ( ) (1)下列收集Cl2的正确装置是________。
(1)下列收集Cl2的正确装置是________。

![]() Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
