
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016年第一次全国大联考【江苏卷】
化学试题
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,时间120分钟。
2.答题前考生务必用0.5毫米黑色墨水签字笔填写好自己的姓名、班级、考号等信息
3.考试作答时,请将答案正确填写在答题卡上。第一卷每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;第Ⅱ卷请用直径0.5毫米的黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.以下数据可供解题时参考:
可能用到的相对原子质量: H 1 O 16 Mg 24 S 32 Cl 35.5 Ca 40 Fe 56 Zn 65
选择题
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一项符合题意)
1.化学与社会可持续发展密切相关。下列做法不合理的是( )
A.CO2和氢气合成甲烷,实现“碳循环”
B.提倡步行、骑自行车、乘公交车等“低碳”出行方式
C.采用纳米TiO2光触媒技术将装修材料中释放的HCHO转化为无害物质
D.将造纸废水通过高压水井压到地下或溶洞中,减少对地表水的污染
2.下列有关氧元素及其化合物的表示正确的是( )
A.质子数为8、中子数为10的氧原子:![]()
B.氧原子的结构示意图:![]()
C.水分子的电子式:![]()
D.乙醛的结构简式: CH3COH
3.下列说法正确的是( )
A.淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体
B.煤的汽化和液化能提高煤的利用率、减少污染
C.利用Al2O3制作的坩埚,可用于熔融烧碱
D.煤的干馏、石油的分馏为物理变化
4.铁与水蒸气高温下反应生成Fe3O4和H2。下列说法正确的是( )
A.元素H的单质存在H2、D2、T2三种同素异形体
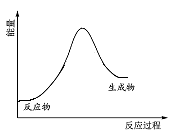 B.在该反应条件下,H2的还原性强于Fe的还原性
B.在该反应条件下,H2的还原性强于Fe的还原性
C.该反应的能量变化关系可以用右图表示
D.该反应中只有热能和化学能的转化
5.短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y原子基态时最外层电子数是次外层的3倍,Z是短周期中最活泼的金属元素, W与Y属于同一主族。下列叙述正确的是( )
A.原子半径:W>Z>Y
B.元素Y的简单气态氢化物的热稳定性比W的弱
C.元素W最高价氧化物的水化物为强酸
D.化合物从X2Y、ZY中化学键的类型相同
6.常温下,下列溶液中各组离子一定能够大量共存的是( )
A.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
B.水电离的c(H+)=10-12mol·L-1的溶液:K+、Ba2+、NH4+、Br-
C.![]() =0.1 mol·L-1的溶液:Na+、K+、SiO32—、NO3—
=0.1 mol·L-1的溶液:Na+、K+、SiO32—、NO3—
D.1.0 mol·L-1的CaCl2溶液:Na+、K+、Cl-、CO
7.下列实验操作正确的是( )
A.稀释浓硫酸时把水沿着烧杯内壁缓慢注入浓硫酸中,并用玻璃棒搅拌。
B.称量2.0gNaOH固体时先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体
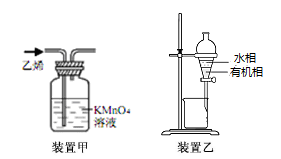
C.用装置甲除去乙烯中少量SO2气体
D.用装置乙分液,从分液漏斗下口放出有机相,关闭活塞再从分液漏斗上口倒出水相
8.下图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出)。下列说法错误的是( )
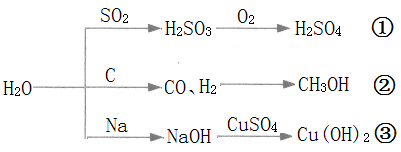
A.图中所示的反应均为氧化还原反应
B.途径①是硫酸型酸雨的形成的重要途径
C.工业上可用途径②先制取水煤气,再合成甲醇等有机物
D.把金属钠投入到硫酸铜溶液中,发生途径③反应,反应不生成铜单质
9.下列表示对应化学反应的离子方程式正确的是( )
A.向AlCl3溶液中滴加过量氨水:Al3++3OH-=Al(OH)3↓
B.向NaNO2溶液中滴加酸性KMnO4溶液:
5NO2-+2MnO4-+3H2O=5NO3-+2Mn2++6OH-
C.醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.向偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
10.一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是( )
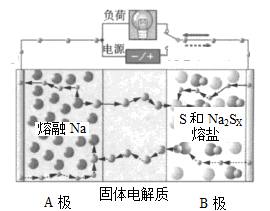
A.B极中硫填充在多孔的炭或石墨毡里,目的是为了增加导电性
B.电池放电时,A极电极反应为:
2Na++xS +2 e-= Na2SX
C.电池放电时,Na+向电极A极移动
D.电池放电的总反应为2Na+xS = Na2SX,每消耗1molNa转移2mol电子
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
11.下列有关说法正确的是( )
A.Hg(l) + H2SO4(aq) = HgSO4(aq) + H2(g)常温下不能自发进行,说明△H<0
B.在一密闭容器中发生2SO2+O2![]() 2SO3反应,平衡后增大压强,平衡会正向移动,
2SO3反应,平衡后增大压强,平衡会正向移动,![]() 的值增大
的值增大
C.已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度
D.H2O2分解产生1molO2,理论上转移的电子数约为2×6.02×1023
12.青蒿酸是合成青蒿素的原料,其可以由香草醛合成:
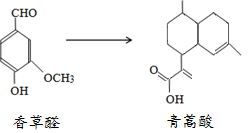
下列叙述正确的是( )
A.在一定条件,香草醛可与HCHO发生缩聚反应
B.两种物质各1mol分别和氢气反应,最多消耗氢气4mol和3mol
C.用FeCl3溶液可鉴别化合物香草醛和青蒿酸
D.青蒿酸分子中含有2个手性碳原子
13.下列设计的实验方案能达到实验目的的是( )
A.检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象。
B.检验溶液中是否含有NH4+:取少量待检验溶液,向其中加入浓NaOH溶液加热,再用湿润的红色石蕊试纸放置试管口,观察现象。
C.提纯含有少量苯酚的苯:向含有少量苯酚的苯加入过量浓溴水,振荡后静置过滤,除去三溴苯酚沉淀。
D.探究化学反应的限度:取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,根据溶液中是否含有碘单质和碘离子判断该反应有一定限度。
14.常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1mol·L-1pH为4的NaHA溶液中:c(HA-)>c(H2A)>c(A2-)
B.向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-)
C.0.10mol·L-1KHC2O4溶液中:c(OH-)=c(H+) +c(H2C2O4)-c(C2O42-)
D.0.10mol·L-1Na2SO3溶液通入少量SO2:c(Na+)=2
15.在体积为2 L的恒容密闭容器中加入0.6mol的CO和H2混合气体,在不同温度下反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡,平衡时CH3OH 的体积分数随起始n(CO):n(H2)的变化关系如图所示。则下列结论正确的是( )
CH3OH(g)达到平衡,平衡时CH3OH 的体积分数随起始n(CO):n(H2)的变化关系如图所示。则下列结论正确的是( )
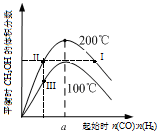
A.反应CO(g)+2H2(g)![]() CH3OH(g)的△H<0
CH3OH(g)的△H<0
B.图示a点n(CO):n(H2)=0.5,CO转化率最高
C.若在状态Ⅰ和Ⅱ时,再向体系中充入He,重新达
到平衡: c(CH3OH,状态Ⅱ)=c(CH3OH ,状态Ⅰ)
D.正反应速率ν正:ν正(状态Ⅱ)>ν正(状态Ⅲ)
非选择题(共80分)
16.(12分)TiCl4是一种重要的工业原料,在露置于空气中会产生大量烟雾,工业上以TiCl4为原料可制备纳米二氧化钛。
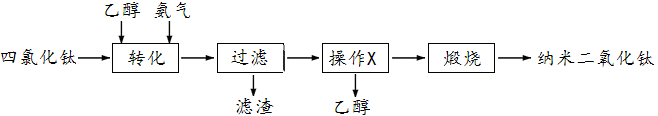
 (1)溶解四氯化钛需要过量乙醇提高四氯化钛转化率,使其生成Ti(OC2H5)4,乙醇另一个作用是▲。
(1)溶解四氯化钛需要过量乙醇提高四氯化钛转化率,使其生成Ti(OC2H5)4,乙醇另一个作用是▲。
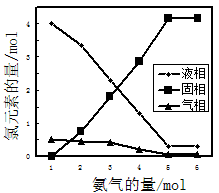
(2)向溶液中匀速通入氨气,溶液中氯元素在固、液、气三相中变化如图,在固相中氯元素存在形式为▲(填化学式)。实验中不能用氨水替代氨气,其原因是▲(用离子方程式表示)。
(3)操作X的名称为▲;煅烧前不需要除去固体含有的杂质,直接煅烧可获得合格产品,其原因是▲。
(4)检验产物二氧化钛粉末是否为纳米级的方法是▲。
17. (15分) )药物I可以通过以下方法合成:
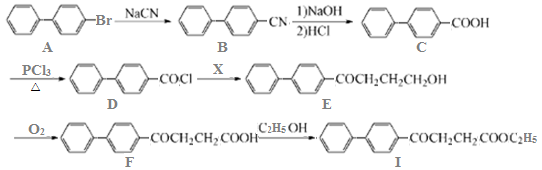
已知:![]()
(1)化合物E中的含氧官能团为___▲___和___▲___(填官能团的名称)。
(2)化合物X的结构简式为__▲___;由C→D的反应类型是:_▲____。
(3)写出同时满足下列条件的F的一种同分异构体的结构简式__▲_____。
Ⅰ.分子含有2个苯环 Ⅱ.能发生银镜反应和水解反应
 Ⅲ.分子中含有6种不同化学环境的氢
Ⅲ.分子中含有6种不同化学环境的氢
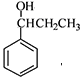
(4)苯丙醇(结构简式见右图)为强效利胆药,请写出以甲苯和C2H5ZnBr为原料制备苯丙醇的合成路线流程图(无机试剂可任选)。合成路线流程图示例如下:
![]()
18.(12分)以碳酸镁(含少量FeCO3)为原料制取硫酸镁晶体,并测定Mg2+含量:将原料完全溶于一定量的稀硫酸中,加足量的试剂X把Fe2+转化为Fe3+,用氨水调节溶液的pH,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。
(1)50.00mL 2.00 mol·L-1的稀硫酸充分与原料充分反应至多产生气体体积(标准状况下)为▲。
(2)试剂X可能为▲。
A.氯水 B.CaO C. SO2 D. H2O2
(3)已知:Ksp=1.0×10-39,Ksp=1.0×10-12。室温下,若溶液中c(Mg2+)=1.00 mol·L-1,欲使溶液中的Fe3+沉淀完全(c(Fe3+)≤1×10-6mol·L-1),需调节溶液pH范围为▲。
(4)常采用下列方法测定结晶硫酸镁中Mg2+的含量:
已知:①在pH为9~10时,Mg2+、Zn2+均能与EDTA(H2Y2-)形成配合物
②在pH为5~6时,Zn2+除了与EDTA反应,还能将Mg2+与EDTA形成的配合物中的Mg2+“置换”出来: Zn2++MgH2Y=ZnH2Y+Mg2+
步骤1:准确称取得到的硫酸镁晶体1.20g加入过量的EDTA,配成100mL pH在9~10之间溶液A
步骤2:准确移取20.00mL溶液A于锥形瓶中,用0.10mol·L-1Zn2+标准溶液滴定,滴定到终点,消耗Zn2+标准溶液的体积为18.00mL
步骤3:准确移取20.00mL溶液A于另一只锥形瓶中,调节pH在5~6;用0.10mol·L-1Zn2+标准溶液滴定,滴定至终点,消耗Zn2+标准溶液的体积为25.00mL。
计算该结晶硫酸镁中Mg2+的质量分数(请给出计算过程)▲。
19.(15分)实验室用下图所示装置制备AlCl3溶液,并用AlCl3溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后煅烧沉淀制备新型的超导材料和发光材料七铝十二钙(12CaO·7Al2O3)。已知AlCl3易水解,易升华。

(1)实验室用氯酸钾和浓盐酸制备氯气,其离子方程式为▲;C装置的作用▲。
(2)氯气与废铝屑反应生成的AlCl3蒸气溶解在B中浓盐酸,为了防止AlCl3蒸气凝华堵塞导管,实验中可采取的措施是▲、▲。
(3)AlCl3溶液溶解CaCO3时,AlCl3溶液和碳酸钙粉末的混合方式为▲。
(4)实验要控制碳酸钙和AlCl3的量, 要求n(CaCO3):n(AlCl3)>12:7,其原因是▲。
(5)用白云石(主要成分为CaCO3、MgCO3)制备纯净碳酸钙的实验方案为:将一定量的白云石煅烧,▲。
(实验中需用到的试剂有:硝酸铵溶液,氨气,二氧化碳;需要用到的仪器:pH计。
已知:镁的化合物不溶于硝酸铵溶液;pH值为11~12时得到较纯净碳酸钙沉淀)。
20.(14分)研究CO、CO2的开发和应用对建设文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH2=-28.5 kJ·mol-1
则C(s) + CO2(g)=2CO(g) △H=▲kJ·mol-1。
(2)电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g)![]() HCOOCH3(g)+2H2(g)
HCOOCH3(g)+2H2(g)
第二步:HCOOCH3(g)![]() CH3OH(g)+CO(g)
CH3OH(g)+CO(g)
该两步反应常温下均不能自发进行,其原因是▲。
在工业生产中,为提高CO的产率,可采取的合理措施有▲(写两条措施)。
(3)节能减排是要控制温室气体CO2的排放。
①氨水可用于吸收低浓度的CO2。请写出氨水吸收足量CO2的化学方程式为:▲。
②利用太阳能和缺铁氧化物可将富集到的廉价CO2热解为碳和氧气,实现CO2再资源化,转化过程如图所示,若生成1mol缺铁氧化物同时生成▲mol氧气。
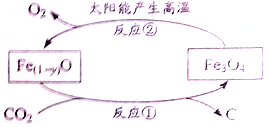
③固体氧化物电解池(SOEC)用于高温电解CO2/H2O,既可高效制备合成气(CO+H2),又可实现CO2的减排,其工作原理如图。
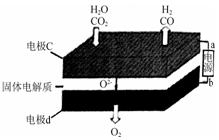
在c极上反应分两步进行:首先水电解产生氢气,然后氢气与CO2反应产生CO。
写出电极c上发生的电极反应式:▲。
若电解得到的1:1的合成气(CO+H2)则通入的CO2和H2O物质的量比值为▲。
21.(12分)【选做题】本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.【物质结构与性质】
含有NaOH的Cu(OH)2悬浊液可用于检验醛基,其反应如下:
2CH3CHO+ 2Cu(OH)42-2CH3COO-+Cu2O↓+5H2O
(1)Cu2+基态核外电子排布式为▲;配合物Cu(OH)42-中与形成配位键的原子是
▲(填元素符号)。
(2)乙醛中碳原子的轨道杂化类型是▲;1mol乙酸分子中含有σ键的数目为▲。
(3)与H2O互为等电子体的一种阴离子为▲(填化学式)。H2O与CH3CHO能够互溶,除了它们都是极性分子外,还因为▲。
B.【实验化学】
乙酰苯胺为无色晶体,有“退热冰”之称。其制备原理为:
![]()
已知:①苯胺易被氧化; ②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
| 试剂名称 | 熔点℃ | 沸点℃ | 溶解度(20 ℃) |
| 苯胺 | -6.2 | 184.4 | 稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 | 16.7 | 118 | 易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 | 114~116 | 280~290 | 0.46g |
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度,小火加热1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。
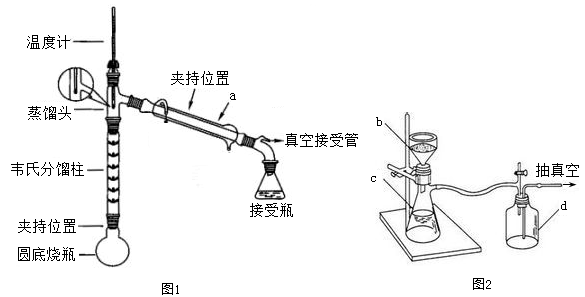
图1 图2
(1)步骤1中使用过量的冰醋酸目的是▲。
(2)步骤2中韦氏分馏柱的作用是▲。
(3)步骤2中控制温度为▲℃。
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是▲,当过滤的溶液具有强酸性、强碱性或强氧化性时要用▲代替布氏漏斗,停止抽滤时的操作为▲。