
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
人民大附中高三年级第二学期查漏补缺练习(三模)
理科综合能力测试(2015-05-26)
可能用到的相对原子质量:H 1 C 12 O 16 Br 80 Cu 64
6.化学与生活、社会密切相关,下列说法不正确的是
A.硅酸凝胶经干燥脱水后得到“硅胶”,常用作干燥剂,也可以用作催化剂的载体
B.金属表面形成的氧化物都能起到保护内层金属的作用
C.煤与氢气作用生成液体燃料,也可以间接液化,先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇
D.含氮和磷的大量污水任意排放向近海海域会出现水华、赤潮等污染问题
7.下列解释实验现象的反应方程式正确的是
A.向硫酸铝溶液中滴加过量的氨水:Al3++ 4OH— == AlO22—+ 2H2O
B.金属铜与浓硝酸反应:3Cu + 8H+ + 2NO3—== 3Cu2+ + 2NO↑+ 4H2O
C.实验室制备氢氧化铁胶体:Fe3++ 3H2O == Fe(OH)3(胶体)+ 3H+
D.向苯酚钠溶液中通入少量的二氧化碳气体:2C6H5ONa + CO2 + H2O == 2C6H6O + Na2CO3
8.下列说法不正确的是
A.油脂是油和脂肪的统称,都是高级脂肪酸与甘油形成的酯
B.棉花、羊毛、蚕丝和麻等是天然纤维
C.高聚物![]() 中的官能团是酯基
中的官能团是酯基
D.可以用溴水鉴别乙醛和乙烯
9.已知0.1 mol·L-1的二元酸H2A溶液的pH=4.0,则下列说法中正确的是
A. 在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:cNa++cH+=cHA-+cOH-+2cA2-
D.在Na2A溶液中一定有:cNa+>cA2->cH+>cOH-
10.下列各项内容中,排列顺序正确的是
① 固体的热稳定性:Na2CO3>NaHCO3
② 相同物质的量浓度的下列溶液中NH4+的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
③ 微粒半径:K+>S2->F
④ 给出质子的能力:CH3COOH>C2H5OH>H2O
⑤ 氢化物的沸点:H2Se>H2S>H2O
A.①③B.②④C.①②D.③⑤
11.下列各图示实验操作合理的是
A.图1为证明非金属性强弱:S>C>Si
B.图2为制备少量氧气
C.图3为配制一定物质的量浓度的硫酸溶液
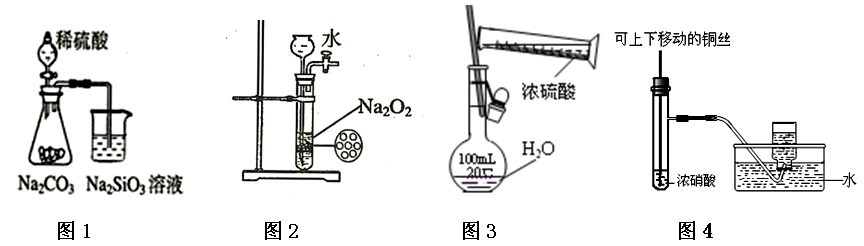 D.图4为制备并收集少量NO2气体
D.图4为制备并收集少量NO2气体
12.向密闭容器中充入物质的量浓度均为 0.1 mol/L的CH4和 CO2,在一定条件下发生反应
 CH4(g)+CO2(g)
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
A.平衡时CO与H2的物质的量比为1:1
B.p1、p2、p3、p4由大到小的顺序为p1
C.1100℃,p4条件下,该反应10min时达到平衡点X,则ν(CO2) = 0.008 mol•L-1•min-1
D.随着温度升高,该反应的平衡常数减小
25.(17分)
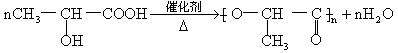
某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为![]() ,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。(图中部分反应条件及产物没有列出)
,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。(图中部分反应条件及产物没有列出)
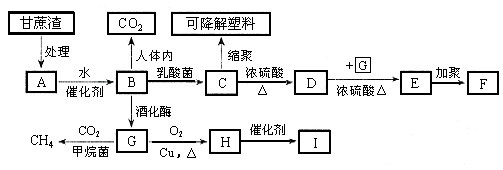
(1)写出下列物质的结构简式:
高分子化合物F;
六元环状化合物I。
(2)C→D的反应类型为____________________。
(3)写出下列反应的化学方程式:
A→B_________________________________________________________
C→可降解塑料_________________________________________________。
(4)H分子所含官能团的名称是___________________,实验室中常用于检验该官能团的试剂的名称是(只写一种)_______________________。
(5)满足与E有相同的官能团的同分异构体有种(不包括顺反异构)。
写出其中一种同分异构体的结构简式。
26.(14分)
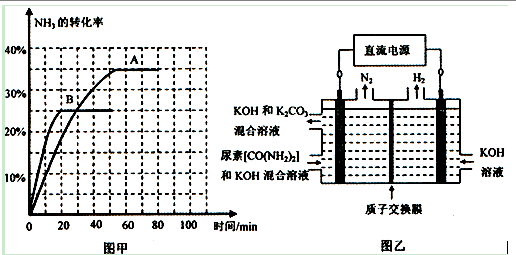
氨气是一种重要的化工产品,是生产铵盐、尿素等的原料。现有如下两种合成氨的途径:
I.N2(g) +3H2(g)![]() 2NH3(g)△H=-92. 4 kJ·mol-1
2NH3(g)△H=-92. 4 kJ·mol-1
II.2N2(g)+6H2O(l)![]() 4NH3(g)+3O2(g)ΔH = +1530.0kJ/mol
4NH3(g)+3O2(g)ΔH = +1530.0kJ/mol
(1)根据上述反应,写出表示H2燃烧热的热化学方程式。
(2)2NH3(g)![]() N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有:。
N2(g) +3H2(g)在恒容密闭容器中达到平衡的标志有:。
①单位时间内生成3n mol H2同时生成2n mol NH3
②用NH3、N2、H2表示反应速率比为2∶1∶3
③混合气体的密度不再改变
④混合气体压强不再改变
⑤混合气体平均相对分子质量不再改变
(3)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2]。
![]()
t℃时,向容积恒定为2L的密闭容器中加入0.10 molCO2和0. 40 molNH3 ,70 min开始达到平衡。反应中CO2(g)的物质的量随时间变化如下表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2) /mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
①20 min时,υ正(CO2) 80 min时υ逆(H2O)(填“>”、“=”或“<”)。
②在100 min时,保持其它条件不变,再向容器中充入0. 050 mo1CO2和0. 20 molNH3,重新建立平衡后CO2的转化率与原平衡相比将(填“增大”、“不变”或“减小”)。
③上述可逆反应的平衡常数为(保留二位小数)。
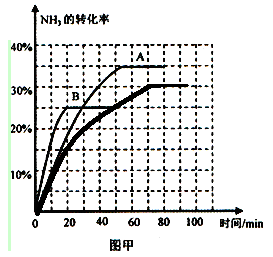
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图像。保持其它条件不变,则(t+10)℃下正确的图像可能是(填图甲中的“A”或“B”)。
27.(12分)
用软锰矿(MnO2)、黄铁矿(FeS2)酸浸生产硫酸锰(MnSO4),并进一步制取电解二氧化锰(EMD)的工艺流程如下:
I. 将软锰矿、黄铁矿和硫酸按一定比例放入反应釜中,搅拌,加热保温反应一定时间。
II. 向反应釜中加入MnO2、CaCO3试剂,再加入Na2S溶液除掉浸出液中的重金属。
III. 过滤,向滤液中加入净化剂进一步净化,再过滤,得到精制MnSO4溶液。
IV. 将精制MnSO4溶液送入电解槽,电解制得EMD。
请回答下列问题:
(1)步骤I中搅拌、加热的目的是。完成酸浸过程中反应的离子方程式:
FeS2+ MnO2+=== Mn2+ + Fe2+ + S + SO42-+
(2)步骤II中加入MnO2用于将浸出液中的Fe2+转化为Fe3+,该反应的离子方程式是。加入CaCO3将浸出液pH调至pH=5,从而除掉铁,请解释用CaCO3除铁的原理:。
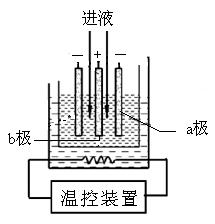
(3)步骤IV中用如图所示的电解装置电解精制的MnSO4溶液,
生成EMD的是极(填“a”或“b”),
生成EMD的电极反应式是。
(4)EMD可用作碱性锌锰电池的材料。已知
碱性锌锰电池的反应式为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。
下列关于碱性锌锰电池的说法正确的是(填字母序号)。[来源:学+科+网]
A.碱性锌锰电池是二次电池
B.碱性锌锰电池将化学能转化为电能
C.正极反应为:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.碱性锌锰电池工作时,电子由MnO2经外电路流向Zn极
28.(15分)
某实验小组做乙醛和新制氢氧化铜的反应时,发现NaOH的用量对反应产物有影响,于是他们采用控制变量的方法,均使用0.5mL40%的乙醛溶液进行下列实验。
| 编号 | 2%CuSO4溶液的体积 | 10%NaOH溶液的体积 | 振荡后 的现象 | pH | 加乙醛水浴加热后的沉淀颜色 |
| 1 | 2 mL | 3滴 | 浅蓝绿色沉淀 | 5~6 | 浅蓝绿色沉淀 |
| 2 | a | 15滴 | 浅蓝色沉淀 | 7~8 | 黑色沉淀 |
| 3 | 1 mL | 1 mL | 蓝色悬浊沉淀较少 | 9~10 | 红褐色沉淀 |
| 4 | b | 2 mL | 蓝色悬浊沉淀较多 | 11~12 | 红色沉淀 |
| 5 | 1 mL | 3 mL | 蓝紫色溶液 | 12~13 | ———— |
(1)上表中a、b应为(填字母序号)。
A.15滴,1 mL B.2 mL,1 mL
C.15滴,2 mL D.2 mL,2 mL
(2)查阅资料可知,实验1中的浅蓝绿色沉淀的主要成份为Cu2(OH)2SO4,受热不易分解。
写出生成Cu2(OH)2SO4反应的化学方程式。
基于实验1、2的现象可以得出结论:NaOH用量较少时,。
(3)小组同学推测实验3中的红褐色沉淀可能是CuO和Cu2O的混合物,其依据是。
(4)由实验4可以得出结论:当NaOH的用量较大时,新制氢氧化铜可以与乙醛发生反应,生成Cu2O红色沉淀。该反应的化学方程式为。
(5)为了进一步证明实验4中红色沉淀的成分,该小组同学查阅资料得知:Cu2O在碱性条件下稳定,在酸性溶液中可转化为Cu2+、Cu。并进行了以下实验。
ⅰ.将实验4反应后的试管静置,用胶头滴管吸出上层清液。
ⅱ.向下层浊液中加入过量稀硫酸,充分振荡、加热,应观察到的现象是。
(6)小组同学继续查阅资料得知:Cu(OH)2可与OH-继续反应生成蓝紫色溶液([Cu(OH)4]2-),由此提出问题:[Cu(OH)4]2-能否与乙醛发生反应,生成红色沉淀?设计实验解决这一问题,合理的实验步骤是。
基于上述实验,该小组同学获得结论:乙醛参与反应生成红色沉淀时,需控制体系的pH>10。
高三化学三模参考答案2015.5
6. B 7. C8.D9.C10.C11.A12.D
阅卷标准:除特别标明分值的空,其余每空2分;不出现0.5分和负分,最低0分。
3.简答题中文字表述中划线部分为给分点。
4.其他合理答案可酌情给分。
25.(17分)(1)
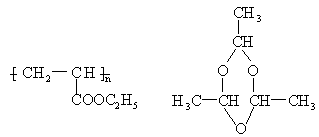
(2)消去反应
(3)![]()
(4)醛基(1分)新制氢氧化铜悬浊液(斐林Fehling试剂)或银氨溶液(硝酸银的氨溶液、托伦Tollens试剂)
(5) 15 CH3COOCH=CHCH3
 26.(12分)
26.(12分)
(1)H2(g)+1/2O2(g)![]() H2O(l) H= -285.8kJ/mol
H2O(l) H= -285.8kJ/mol
(2)C
(3)>增大76.53图如下 B
27.(14分)(1)加快反应速率,充分接触(1分)
FeS2+4MnO2+ 8H+===4Mn2++Fe2++S +SO42-+4H2O
(2)MnO2+4H++2Fe2+===Mn2++2Fe3++2H2O
Fe3++3H2O![]() Fe(OH)3 + 3H+,(1分)加入CaCO3后,由于CaCO3(s)
Fe(OH)3 + 3H+,(1分)加入CaCO3后,由于CaCO3(s)![]() Ca2+(aq) + CO32-(aq),CO32-+2H+===CO2↑+H2O(或CaCO3与H+反应)(1分),使得Fe3+的水解平衡向正反应方向移动,Fe3+转化为Fe(OH)3沉淀而被除去。
Ca2+(aq) + CO32-(aq),CO32-+2H+===CO2↑+H2O(或CaCO3与H+反应)(1分),使得Fe3+的水解平衡向正反应方向移动,Fe3+转化为Fe(OH)3沉淀而被除去。
(3)b(1分)Mn2++2H2O-2e-===MnO2+4H+
(4)BC
28.(15分)
(1)B
(2)2NaOH+2CuSO4===Cu2(OH)2SO4↓+Na2SO4
乙醛未参与氧化反应,(或是含铜元素的化合物在发生变化)
(3)此题答案可从“现象”或“理论”两个角度提出依据。
依据现象提出依据:实验2中的黑色沉淀可能是CuO;实验4中的红色沉淀可能是Cu2O,所以实验3中的红褐色沉淀,可能是CuO和Cu2O的混合物。
依据理论提出依据:当NaOH用量逐渐增多时,产生的Cu(OH)2一部分受热分解生成黑色的CuO;另一部分被乙醛还原为Cu2O红色沉淀,所以实验3中的红褐色沉淀,可能是CuO和Cu2O的混合物。
(4)CH3CHO + 2Cu(OH)2+NaOH![]() CH3COONa + Cu2O↓ + 3H2O
CH3COONa + Cu2O↓ + 3H2O
(5)溶液变为蓝色,有红色固体
(6)将1 mL 2%CuSO4溶液与3 mL(或>3 mL)10%NaOH溶液混合振荡后(或取实验5的蓝紫色溶液)(1分),加入0.5 mL 40%的乙醛溶液(1分),水浴加热(1分) (3分)