
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
宁城县高三年级统一考试(2016.03.20)
化 学 试 题
时间:90分钟 分值:100分
可能用到的相对原子质量:C:12 H:1 Fe:56 Cl:35.5 Cu:64 S:32 O:16
Na:23 Cr:52 Ca:40
请将正确答案写在答题卡上。
一、选择题(每题只有一个正确答案,每题3分,计42分)
1、化学与人类生活密切相关,下列与化学有关的说法不正确的是
A.开发和推广新能源是实现低碳生活的途径之一
B.化学药品着火,要立即用水或泡沫灭火器灭火
C.食品添加剂虽能改善食物味道等,但需限量使用
D.化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶
2、用NA表示阿伏加德罗常数,下列叙述中不正确的是( )
①32 g S8单质(S8分子结构如右图)中含有的S—S键个数为NA![]()
②电解精炼铜时转移了NA个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA
④2 mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2NA
⑤2.9 g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.02NA(2CaSO4·H2O式量为290)
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
A.①②③④⑤ B.①③④⑤⑥ C.②③⑤⑥ D.③④⑤⑥
3、常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是( )
A.①和②混合溶液中:c(H+)=3.0 mol·L-1
B.①和④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
C.②和③混合溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D.四种溶液稀释100倍,溶液的pH:③>④>②>①
4.用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是( )
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤
④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成Al(OH)3沉淀 ⑥加入过量烧碱溶液
A.①⑥⑤③B.②③④③C.②③⑤③D.①③⑤③
5.芳香化合物M的结构简式为 ,关于有机物M的说法正确的是
A.有机物M的分子式为C10H12O3
B.1 molNa2CO3最多能消耗1 mol有机物M
C.1 mol M和足量金属钠反应生成22.4 L气体
D.有机物M能发生取代、氧化和加成反应
6.现有X、Y、Z三种常见短周期元素,Y、Z为同周期金属元素,且X和Y的某种化合物为淡黄色固体M,Y、Z的最高价氧化物对应的水化物可以反应生成盐N和水。下列说法不正确的是
A.固体M能与水反应生成X单质和一种强碱
B.Z单质的薄片在酒精灯上加热能熔化,但不滴落
C.Y的最高价氧化物对应的水化物和盐N均能抑制水的电离
D.M和N中均含有离子键和共价键
7.分子式为C9H12O,苯环上有两个取代基且含羟基的化合物,其可能的结构有
A.9种 B.12种 C.15种 D.16种
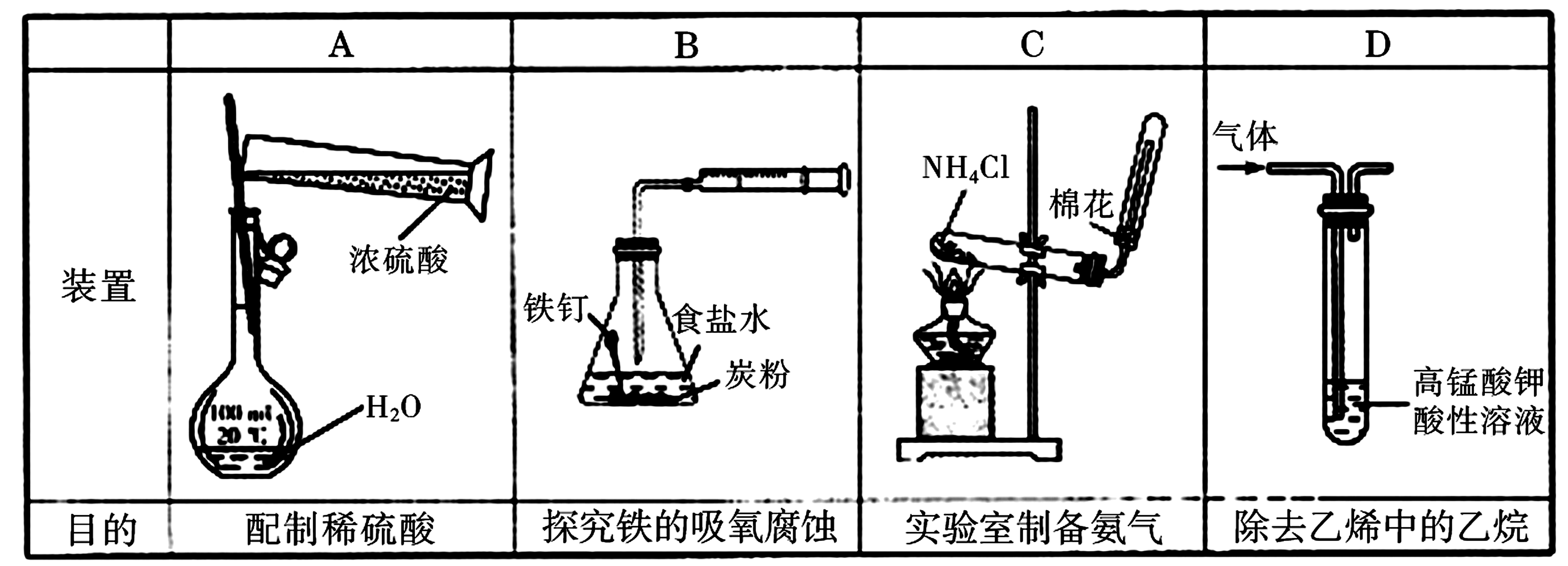
8.下列操作或仪器的选用正确的是
9、常温下,下列各组离子在指定溶液中一定能大量共存的是( )
①pH=0的溶液:Na+、C2O42﹣、MnO4﹣、SO42﹣
②pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣、S2﹣、SO32﹣
③水电离的H+浓度c(H+)=10﹣12mol·L﹣1的溶液中:Cl﹣、CO32﹣、NO3﹣、NH4+、SO32﹣
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl﹣、K+、SO42﹣
⑤使石蕊变红的溶液中:Fe2+、MnO4﹣、NO3﹣、Na+、SO42﹣
⑥中性溶液中:Fe3+、Al3+、NO3﹣、I﹣、Cl﹣、S2﹣.
A.①③⑤ B.③②⑥ C.②④ D.①④⑤
10.下列说法中,不正确的是( )
①同一元素的不同核素互称为同位素
②化学键可以使离子相结合,也可以使原子相结合
③金属腐蚀的实质是金属原子失去电子被还原的过程
④Ksp不仅与难溶电解质的性质和温度有关,而且还与溶液中的离子浓度有关
⑤铅蓄电池在放电过程中,负极质量减少,正极质量增加
⑥Al和Fe在一定条件下都能与某些氧化物反应
⑦干冰和氨都属于弱电解质
⑧汽油和花生油的主要成份都是油脂
A.①③④⑦⑧ B.②③④⑤⑧ C. ③④⑤⑦⑧ D.①③⑤⑥⑦
11、 镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:xMg+Mo3S4![]() MgxMo3S4,下列说法正确的是 ( )
MgxMo3S4,下列说法正确的是 ( )
A.电池放电时,Mg2+向负极迁移
B.电池放电时,正极反应为Mo3S4+2xe-+xMg2+![]() MgxMo3S4
MgxMo3S4
C.电池充电时,阴极发生还原反应生成Mo3S4
D.电池充电时,阳极反应为xMg-2xe-![]() xMg2+
xMg2+
12、已知NH4CuSO3与足量的10mol/L硫酸液混合微热,产生下列现象:
①有红色金属生成
②产生刺激性气味的气体
③溶液呈现蓝色
据此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B.NH4CuSO3中硫元素被氧化
C.刺激性气味的气体是氨气
D.1mol NH4CuSO3完全反应转移0.5mol电子
13.已知如下物质的溶度积常数:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;
ZnS:Ksp=1.6×10-24。下列说法正确的是( )
A.同温度下,CuS的溶解度大于ZnS的溶解度
B.将足量CuSO4溶解在0.1 mol·L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol·L-1
C.因为H2SO4是强酸,故CuSO4+H2S![]() CuS↓+H2SO4不能发生
CuS↓+H2SO4不能发生
D.除去工业废水中的Cu2+,可以选用FeS作沉淀剂
14、部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:
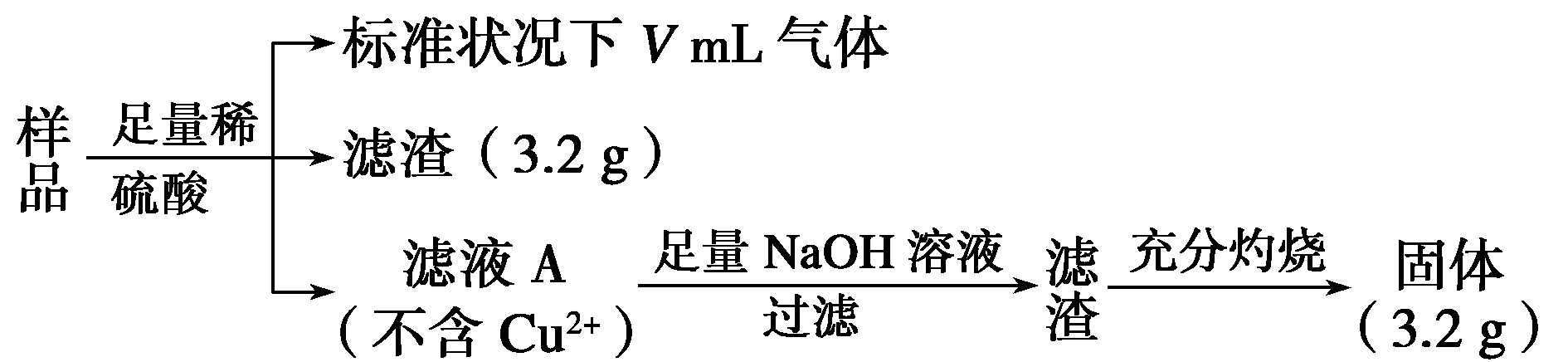
下列说法正确的是( )
A.V=44.8
B.原样品中Fe元素的质量分数为38.89%
C.滤液A中的阳离子为Fe2+、Fe3+、H+
D.样品中CuO的质量为4.0 g
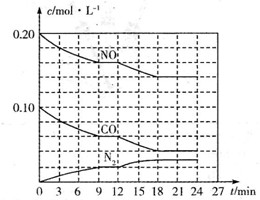
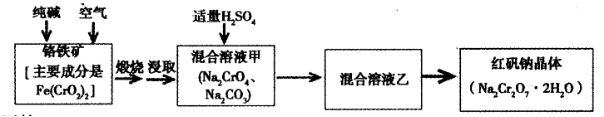
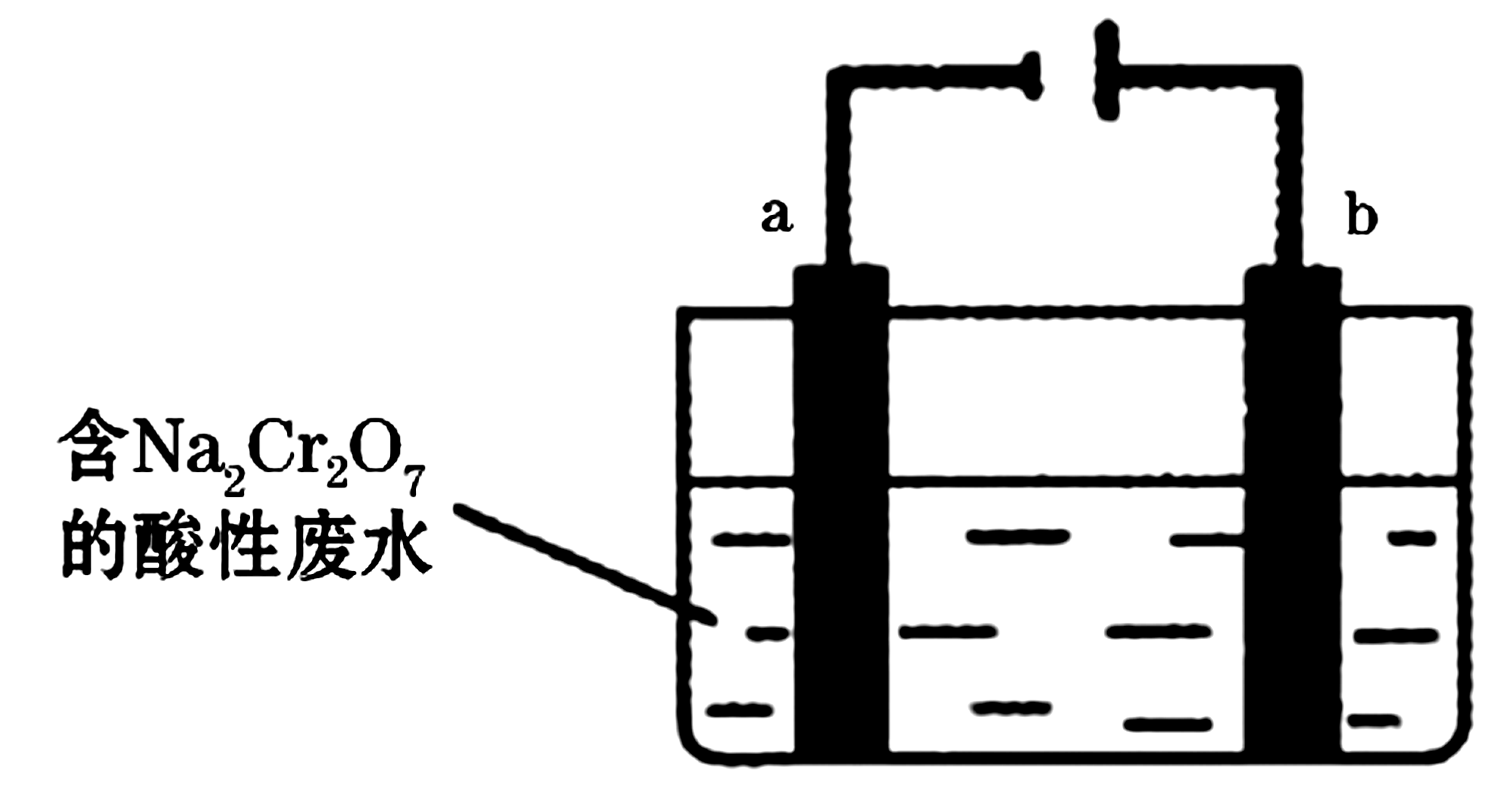
15.(15分)为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
19.【化学——选修3:物质结构与性质】(15分)
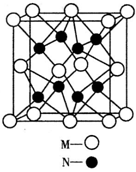 M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素。M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素。M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子。请回答下列问题:
4、化合物A的分子式为C9H15OCl,分子中含有一个六元环和一个甲基,环上只有一个取代基;F分子中不含甲基:A与其它物质之间的转化如图所示: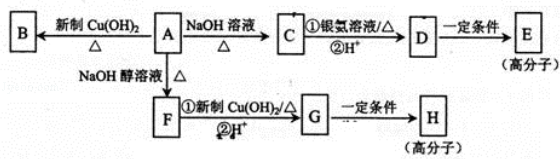
(1)A→F的反应类型是 ;G中官能团的名称是 .
(2)A→C的反应方程式是 .
(3)H的结构简式是 ,E的结构简式是 .
(4)有的同学认为B中可能没有氯原子,你的观点是
,你的理由 .
(5)某烃的含氧衍生物X符合下列条件的同分异构体中,核磁共振氢谱显示为2组峰的是 ;只含有两个甲基的同分异构体有 种.
①相对分子质量比C少54 ②氧原子数与C相同 ③能发生水解反应.
高三考试化学参考答案
一、选择题
1B 2C 3D 4B 5D 6C 7C 8B 9C 10C 11B 12D 13D 14B
二、非选择题
15(15分)
(1)-746.5(3分)
(2)①4.4×10-3(2分) D(2分) ②22.2%(2分) 3.4(2分)
(3)2c(SO![]() )+c(HSO
)+c(HSO![]() )(2分)
)(2分)
(4)1.0×10-7(3分)
16(14分)
(1)+2
(2)FeO·Cr2O3
(3)粉碎矿石,升高温度。
(4)① 少量不能除尽Na2CO3等杂质,过量会生成Na2Cr3O10等副产物。
② Na2Cr2O7和Na2SO4
(5)2H+ + 2e- = H2↑,Cr2O![]() + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
+ 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O
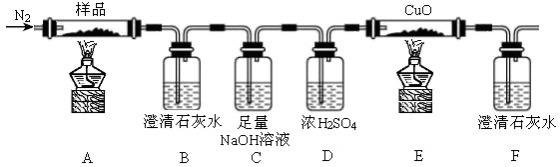
17.(14分)(1)检查装置的气密性(1分)
(2)不需要 (1分) 因为N2不断通入,B、F瓶溶液不会倒吸。(1分)
(3)CO2 (1分) E中黑色固体变成红色,F中溶液变浑浊 (2分)
(4)焰色反应(1分) 透过蓝色的钴玻璃观察到紫色火焰 (1分)
(5)FeO 和Fe (2分) 3FeO +10H++NO3-=3Fe3++NO↑+5H2O (2分)
Fe+4H++NO3-=Fe3++NO↑+2H2O (2分)
18(15分)、(1)直接液化技术 间接液化技术(各1分)
(2)2FeS2+7O2+2H2O4H++2Fe2++4SO42—
4Fe2++O2+4H+4Fe3++2H2O(各2分)
(3)焦炉煤气、粗氨水、煤焦油(3分,每个1分)
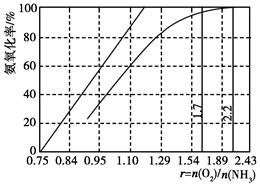
(4)1.25(2分)
O2太少不利于NH3的转化,r值为2.2时NH3氧化率已近100%(2分)
19(15分)
20(15分)
(1)消去反应( 1分);碳碳双键和羧基;(2分)
(2) ;(2分)
(3) ; ;(各2分)
(4)同意;在碱性环境下氯原子有可能水解,使得B中没有氯原子;(各1分)
(5)HCOOC(CH3)3;5.(各2分)