
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2016届净月实验校高三年级
“百炼成钢,只争朝夕”第二次模拟考试
化学试题
考试时间:90分钟 试题满分:100分
命题人: 审题人:
第Ⅰ卷(选择题 共50分)
相对原子质量:H:1 C:12 O: 16 N:14 Cu:64 Fe:56 Ag:108
一、选择题:(本题共25小题,每小题2分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.下列说法正确的是
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.依据丁达尔效应可将分散系分为溶液、胶体与浊液
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
2.含有下列各组离子的溶液中,通入过量SO2气体后仍能大量共存的是
A.H+、Ca2+、Fe3+、N03-B.Ba2+、Cl-、Al3+、H+
C.K+、NH4+、I-、HS-D.Na+、C032-、K+、N03-
3.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.25℃和101kp的条件下,4.9L甲烷完全燃烧生成的水的分子数为0.4NA
B.用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA
C.Na2O2与足量H2O反应生成标况下11.2LO2,转移电子的数目为2 NA
D.标准状况下,2.24LHF中所含电子数为NA
4.图表归纳是学习化学的一种常用方法,某同学归纳的下表与图中对应关系正确的是
| 选项 | X | Y | Z | 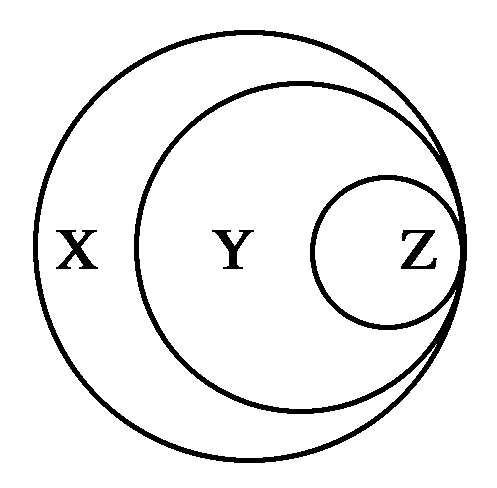 |
| A | 胶体 | 混合物 | 淀粉溶液 | |
| B | 化合物 | 酸性氧化物 | 一氧化氮 | |
| C | 气态氢化物 | 化合物 | 液溴 | |
| D | 强电解质 | 强酸 | 硫酸 |
5.化学在工业生产和日常生活中有着重要的应用。下列说法正确的是
A.CO2、NO2和SiO2都是酸性氧化物,都是大气污染物
B.Na2O2、H2O2所含化学键完全相同,都能作供氧剂
C.常温下,浓硫酸、浓硝酸与铁均能发生钝化,均能用铁罐储运
D.NaClO和明矾都能作消毒剂或净水剂,加入酚酞试液均显红色
6.下列叙述中错误的是
A.氧化性;Na+![]() >S2
>S2![]() >F
>F![]()
C.稳定性:HF>HCl>HBr>HID.酸性:HClO4>H2SO4>H2CO3>H2SiO3
7.能正确表示下列反应的离子方程式是
A.用过量氨水吸收工业尾气中的SO2:2NH3·H20+SO2![]() 2NH4++SO32-+H2O
2NH4++SO32-+H2O
B.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO![]() +6H++5H2O2=2Mn2++5O2↑+8H2O
+6H++5H2O2=2Mn2++5O2↑+8H2O
C.用铜做电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+=2Fe3++3H2O
8.下列过程没有发生化学反应的是
A.用食醋除去暖水瓶中的薄层水垢 B.石油的分馏和煤的干馏
C.用二氧化氯(ClO2)为自来水消毒 D.液氨作制冷剂
9.关于硅的下列叙述中,正确的是
A.晶体硅与金刚石分子都是正四面体结构 B.硅酸盐都不溶于水
C.硅与酸、碱都不能发生反应 D.原硅酸和硅酸对应的酸酐都是二氧化硅
10.关于下列各装置图的叙述中,正确的是
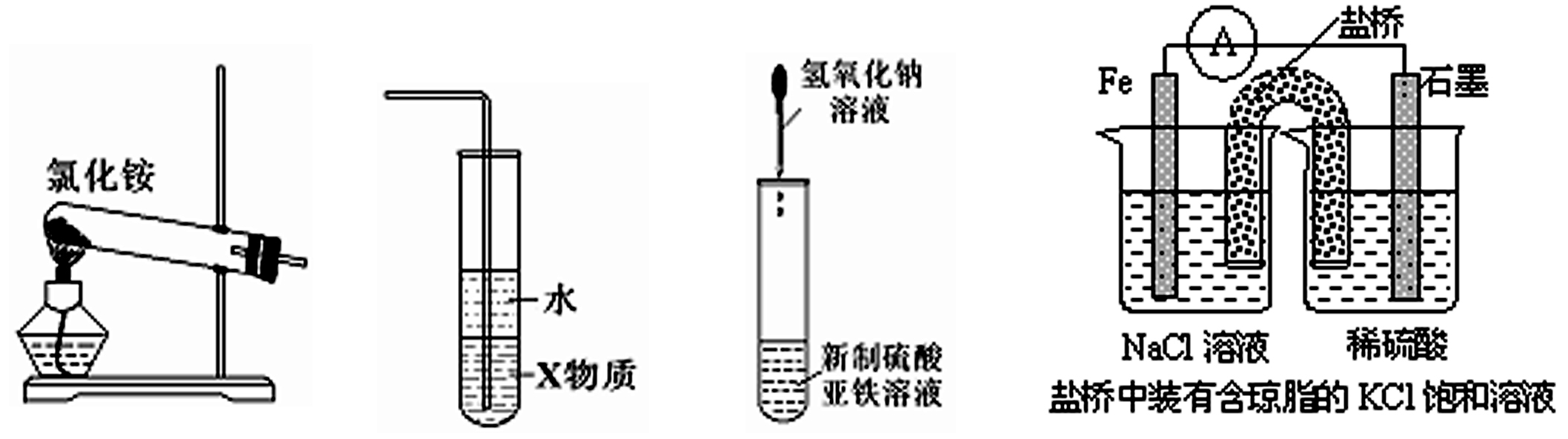
① ② ③ ④
A.实验室用装置①制取氨气
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸
C.装置③可用于制备氢氧化亚铁并观察其颜色
D.装置④左侧烧杯中c(Cl-)减小
11.有机物A的分子式为C5H10O2,其在氢氧化钠溶液中加热水解得B、C两种物质,已知B能与盐酸反应生成E,E能发生银镜反应,而C不能发生银镜反应。则A可能的结构有
12. 在一定温度和压强条件下发生了反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是
CH3OH(g)+H2O(g) △H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是
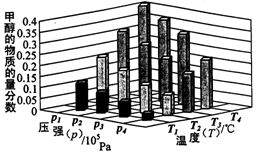 A.P3>P2T3>T2
A.P3>P2T3>T2
B.P2>P4T4>T2
C.P1>P3T3>T1
D.P1>P4T2>T3
13.在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
| a(干燥气体) | b(液体) | |
| A | NO | 水 |
| B | CO2 | 饱和NaHCO3溶液 |
| C | Cl2 | 饱和NaCl溶液 |
| D | NH3 | 1 mol·L-1盐酸 |
14.下列实验中所选用的仪器或实验基本操作合理的是
①用l0mL量筒量取5.2 mL稀硫酸; ②用酒精洗涤粘有硫粉的试管: ③用托盘天平称量10.1 g氯化钠晶体 ④用过滤的方法除去淀粉胶体中的氯化钠溶液:⑤用饱和NaHCO3溶液除去CO2中的少量SO2
A.①②③④ B.②③④ C.③④⑤ D.①③⑤
15.夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏。“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,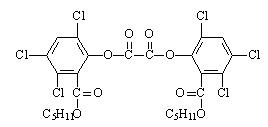 草酸二酯(CPPO)结构简式如右图。下列说法正确的是
草酸二酯(CPPO)结构简式如右图。下列说法正确的是
A.草酸二酯的分子式为C26H22Cl6O8
B.1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解), 最多消耗6molNaOH
C.草酸二酯水解可以得到两种有机物
D.1mol草酸二酯与氢气完全反应,需要氢气10mol
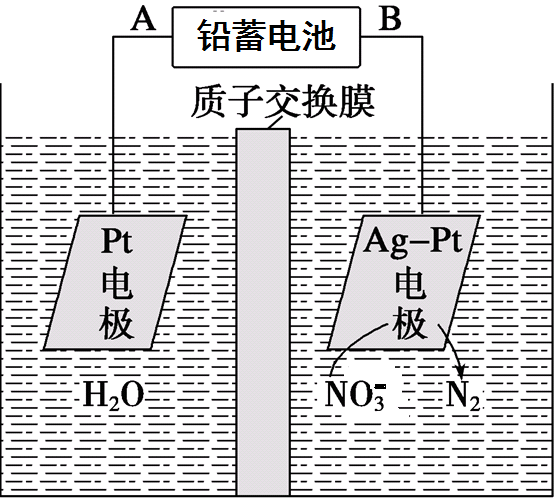 16.电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,下列说法不正确的是
16.电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO的原理如图所示,下列说法不正确的是
A.铅蓄电池的A极为正极,电极材料为PbO2
B.该电解池的总反应方程式为:
![]() 2H2O + 4NO3-2N2↑+ 5O2↑+ 4OH-
2H2O + 4NO3-2N2↑+ 5O2↑+ 4OH-
C.该电解池的阴极反应式为:
2NO3-+ 12H+ + 10e-= N2↑ + 6H2O
D.若电解过程中转移2mol电子,则交换膜右侧电解液的质量减少5.6g
17.下列现象或事实不能用同一原理解释的是
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硝酸
D.SO2和Na2SO3溶液都能使氯水褪色
18.有FeO、Fe2O3的混合物若干克,在足量H2气流中,加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,需1 mol·L-1的盐酸的体积至少为
A.0.05 L B.0.1 LC.0.2 L D.1 L
19.下图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
下列说法中不正确的是
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质
20.有A、B、C、D四种短周期元素在周期表中位置如图所示。已知:A2+与C原子的电子数相差2。下列推断不正确的是
| …… | C | |||
| A | B | …… | D |
A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中常作催化剂。
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
21.下列实验装置能达到相关实验目的的是
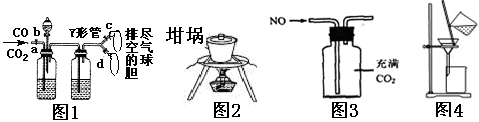
A.图1可用于分离收集CO和CO2B.图2用于从食盐水中提取NaCl晶体
C.图3用于收集NOD.图4用于氢氧化铁胶体和硫酸钠溶液的分离
22.在25℃、1.01×105Pa下,将22gCO2通入到750mL1.0mol·L-1的NaOH溶液中充分反应,放出xkJ热量。在该条件下1molCO2通入到2L 1.0mol·L-1的NaOH溶液中充分反应,放出ykJ热量,则CO2与NaOH反应生成NaHCO3的热化学反应方程式为
A.CO2(g)+NaOH(aq)=NaHCO3(aq) △H = -(2y-x)kJ·mol-1
B.CO2(g) + NaOH(aq) = NaHCO3(aq) △H = -(4x-y)kJ·mol-1
C.CO2(g) + NaOH(aq) = NaHCO3(aq) △H = -(2x-y)kJ·mol-1
D.CO2(g) + NaOH(aq) = NaHCO3(aq) △H = -(8x-2y)kJ·mol-1
23.依据下列实验现象,得出的结论正确的是
| 操作 | 实验现象 | 结论 | |
| A | 向NaBr溶液中加入氯水,再加入淀粉KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
| B | 将铝片放入盐酸中 | 产生气泡的速率开始时较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
| D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
24.恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g)![]() MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2) / mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ(CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.若升高温度,反应的平衡常数变为1.0,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)=0.6 mol
25.Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
A.1∶7 B.1∶9 C.1∶5 D.2∶9
第Ⅱ卷(非选择题 共50分)
二、非选择题:本题包括4小题,共50分。
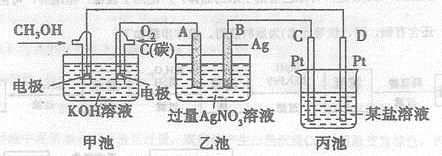
26.(8分)下图是一个化学过程的示意图。
ΔH= +117.6 kJ/mol;
+H2(g),
反应②:t1
II.一定的条件下,合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
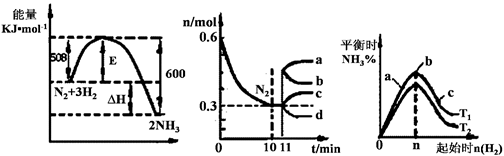
图
图1 图2 图3
(4)升高温度,该反应的平衡常数 (填“增大”或“减小”或“不变”)。
(5)由图2信息,计算10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
(6)图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1T2(填“>”或“=”或“<”)
28.(13分)无水三氯化铁易升华,有强烈的吸水性,是一种用途比较广泛的盐。
(1)实验室中可将FeCl3溶液 、 、过滤、洗涤干燥得FeCl3·6H2O;再 ,得到无水FeCl3。
(2)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
①为抑制FeCl3水解,溶液X为 。
②上述流程中FeCl3能被异丙醚萃取,其原因是 ;检验萃取、分液后所得水层中是否含有Fe3+的方法是 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是 。
④为测定所得草酸铁晶体的纯度,实验室称取ag样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于右图所示仪器 (填“甲”或“乙”)中;下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是 。
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
29.(15分)工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HClO→CH2(OH)CH2Cl。以乙烯为原料制取PVC等产品的转化关系如图所示。
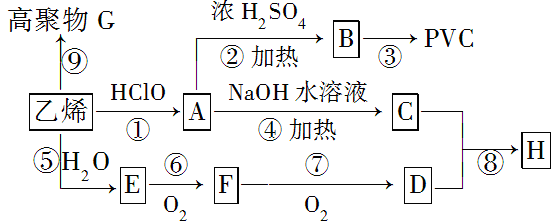
试回答下列问题:
(1)写出有机物B和G的结构简式:B____________,G_________;
(2)②、⑤、⑦的反应类型分别是_______________,_____________,______________;
(3)写出D的同分异构体的结构简式_____________,_____________;
(4)写出反应⑥的化学方程式__________________________________;
(5)写出C与D按物质的量之比为1∶2反应生成H的化学方程式:
______________________________________________________________。
答 案
一、选择题:
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 |
| D | B | A | D | C | B | A | D | D | B | D | D | D | D | B | D | C | B | D | A | A | B | D | B | A |
二、非选择题
26. (8分) (1)CH3OH(1分)
电解
4Ag++2H2O====4Ag+O2↑+4H+(1分)27.(14分)
(1)CO2(g)+![]() (g)
(g)![]() (g)+ H2O(g);ΔH= +158.8 kJ/mol;(2分)
(g)+ H2O(g);ΔH= +158.8 kJ/mol;(2分)
K= K1·K2;(2分)(2)CD(2分)
(3)(1分)
(4) 减小(1分)(5)0.045mol/(L·min) (2分) d(2分)
(6)c(1分)<(1分)
28.(13分)(1)蒸发(浓缩)、冷却(结晶);将FeCl3·6H2O在HCl的气氛中加热脱水 (每空1分)
(2)①(浓)盐酸 (1分) ②FeCl3在异丙醚中的溶解度大于其在水中的溶解度;(2分)取少量溶液,向其中滴加少量KSCN溶液,若溶液变红,则含有Fe3+。(或其他合理方法)(2分)
③除去杂质、减少草酸铁晶体的溶解损耗 (2分) ④甲(1分);c(2分)
29.(共15分)
(1)![]() (各2分)
(各2分)
(2)消去反应 加成反应 氧化反应(各1分)
(3)HCOOCH3 CH2(OH)CHO(各2分)
(4)2CH3CH2OH+O22CH3CHO+2H2O(2分)
(5)CH2(OH)CH2(OH)+2CH3COOH![]() CH3COOCH2CH2OOCCH3+2H2O(2分)
CH3COOCH2CH2OOCCH3+2H2O(2分)