
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
吉林省吉林大学附属中学2016届高三化学上学期第一次摸底考试试题
试卷满分:100分 考试时间:90分钟
注意事项:
1.请考生将姓名、班级、考号与座位号填写在答题纸指定的位置上;
2.客观题的作答:将正确答案填涂在答题纸指定的位置上;
3.主观题的作答:必须在答题纸上对应题目的答题区域内作答,在此区域外书写的答案无效;在草稿纸、试卷上答题无效。
可能用到的相对原子质量:D-2 N-14 O―16 Na-23 Mg-24 Al-27 Fe-56 Cu-64
第Ⅰ卷(客观题50分)
一、选择题(本题共包括10小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.运输汽油的车上,贴有的危险化学品标志是
A. B.
B. C.
C. D.
D.
2.若NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,6.72 L NO2与水充分反应转移电子数为0.1NA
B.18 g D2O中含有的质子数目为10NA
C.常温常压下,1 mol氦气中含有的核外电子数为2 NA
D.ag某气体含分子数为b,cg该气体在标况下的体积为22.4ab/(c NA) L
3.下列解释事实或实验现象的化学用语正确的是
A.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+ 3H+
Fe(OH)3↓+ 3H+
B.酸性KI淀粉溶液久置后变蓝 4I-+O2+2H2O=2I2+4OH-
C.实验室盛装NaOH溶液的试剂瓶不能用玻璃塞SiO2+2OH-= SiO32-+H2O
D.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
4.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是
A.冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物
B.HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸
C.漂白粉、福尔马林、冰水、王水、氯水均为混合物
D.Na2O、NaOH、Na2CO3、NaCl都属于钠的含氧化合物
5.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色溶液中: Al3+、Cl-、MnO4-、SO42-
B.含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、SCN-
C.0.1 mol·L-1AgNO3溶液:H+、K+、SO42-、I-
D.使酚酞变红色的溶液:CO32-、Cl-、F-、K+
6.在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:
2MnO+16H++5Na2O2===2Mn2++5O2↑+8H2O+10Na+。下列判断正确的是
A.O2是还原产物,Mn2+是氧化产物 B.Na2O2既是氧化剂,又是还原剂
C.标准状况下,产生22.4 L O2时反应转移2 mol e-D.通常用浓盐酸酸化高锰酸钾溶液
7.在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;若加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度(mol/L)为
A. B. C. D.
8.下列是关于氯水的叙述,正确的是
A.新制氯水中只含Cl2和HClO分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡冒出,该气体为Cl2
D.氯水放置数天后,pH值将增大
9.某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。
下列化合物中符合上述条件的是
A.NaCl B.Na2O2C.Na2SO4D.SiO2
10.化学是一门与社会、生活、科研密切相关的自然科学。下列有关叙述中,不正确的是
A.利用化学反应可实现12C到14C的转化
B.天然气、煤气大量泄漏遇到明火会爆炸
C.大量使用燃煤发电是形成雾霾的主要原因
D.晶体硅可用作半导体材料
二、选择题(本题共包括10小题,每小题3分,共30分。每小题只有一个选项符合题意)
11.下列有关说法中错误的是
A.氢氟酸不能盛放在玻璃试剂瓶中
B.由沙子制备光伏材料时的反应之一为SiO2+2C![]() Si+2CO↑
Si+2CO↑
C.灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应
D.玻璃、水晶、陶瓷的主要成分均是硅酸盐
12.某研究小组对离子方程式xR2++ yH++ O2= mR3++ nH2O的分析研究,下列说法中错误的是
A.根据电荷守恒,得出x与y的和一定等于m
B.根据原子守恒,得出x和m的数值一定相等
C.根据电子得失守恒,得出x=4的结论
D.根据氧还反应关系得出:R2+是还原剂,O2是氧化剂,R3+是氧化产物,H2O是还原产物
13.有一粗硅,含杂质铁,取等质量的样品分别投入足量的稀盐酸和足量的稀氢氧化钠溶液中,放出等量的H2,则该粗硅中铁和硅的关系正确的是
A.物质的量之比为1∶1 B.质量之比为4∶1
C.物质的量之比为1∶2 D.质量之比为2∶1
14.海水开发利用的部分过程如图所示。下列说法错误的是
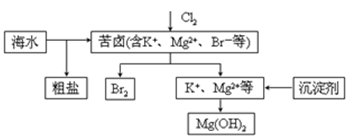
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
15.中学常见物质A、B、C、D、E、X,存在下图转化关系(部分生成物和反应条件略去)。
下列推断不正确的是
![]()
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B
16.高铁酸钠(Na2FeO4)是一种饮用水的高效消毒剂,可由下列方法制得:
Fe2O3+3Na2O2高温2Na2FeO4+Na2O,关于该反应说法正确的是
A.Na2FeO4属于共价化合物B.在Na2FeO4中Fe为+4价,具有强氧化性
C.生成l mol Na2FeO4,有6 mol电子转移 D.反应中Na2O2是氧化剂
17.有一瓶无色气体可能含有CO2、HBr、NO2、HCl、SO2中的一种或几种。将此气体通入足量稀氯水中,恰好完全反应,得无色透明溶液,把此溶液分成两份,分别加入盐酸酸化了的BaCl2溶液和硝酸酸化了的AgNO3溶液,均出现白色沉淀,以下结论正确的是
A.不能确定原气体中是否含有SO2
B.原气体中肯定有HCl
C.原气体中肯定没有CO2
D.原气体中肯定没有HBr、NO2
18.在15.2 g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4 g沉淀,则下列表示气体X组成的选项中合理的是
A.0.3 mol NO、0.1 mol NO2 B.0.3 mol NO2、0.1 mol NO
C.0.6 mol NO D.0.3 mol NO2
19.用右图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| D | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
20.下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是
h
A.a-b-c-d-e-f-g-h B.a-c-b-d-e-h-i-f C.a-d-e-c-b-h-i-gD.a-e-d-c-b-h-i-g
第Ⅱ卷(主观题50分)
三、非选择题(本题共包括5小题,共50分)
21.(12分)
Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色。
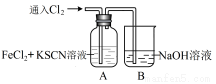
(1)B中反应的离子方程式是 ;
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验。取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 ;
(3)资料显示:SCN-的电子式为![]() 。甲同学猜想SCN﹣可能被Cl2氧化了,他进行了如下研究。
。甲同学猜想SCN﹣可能被Cl2氧化了,他进行了如下研究。
①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,由此证明
SCN﹣中被氧化的元素是 ;
②甲同学通过实验证明了SCN﹣中氮元素转化为NO3﹣,已知SCN﹣中碳元素没有被氧化,若SCN﹣与Cl2反应生成1mol CO2,则转移电子的物质的量是 mol;
Ⅱ.8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒。有少量因爆炸冲击发生泄漏。这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染。
请写出NaCN的电子式________,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3﹣,同时放出NH3,该反应的离子方程式为 。
22.(8分)化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80 g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式 ;
(2)甲与AlCl3反应得到NaAlH4的化学方程式 ;
(3)NaAlH4与水发生氧化还原反应的化学方程式 ;
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
23.(7分)某化学研究性学习小组讨论Fe3+溶液和SO32-溶液之间发生怎样的反应,提出了两种可能,写出预计反应的离子方程式:
一是发生氧化还原反应 ,二是发生彻底互促水解反应 。
为了证明发生怎样的反应,同学们设计并进行如下实验,请填写下列空白:
实验Ⅰ:取5 mL FeCl3浓溶液于试管中,逐滴加入某Na2SO3浓溶液至过量,观察到无气泡产生,无沉淀生成,但溶液颜色最终变为红褐色。这种红褐色液体是 。
向红褐色液体中逐滴加入稀盐酸至过量,可观察到溶液最终变为黄色。将所得溶液加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是
。
实验Ⅱ:将FeCl3和Na2SO3溶液分别稀释后,重复实验Ⅰ,产生的现象完全相同。
同学们由上述实验得出的结论是 。
指导老师看过上述实验步骤后认为该设计有缺陷,应在开始实验前对某主要药品进行检验,该主要药品为 ;检验的目的是 。
24.(13分)无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为 ;
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种
工艺流程示意如下:
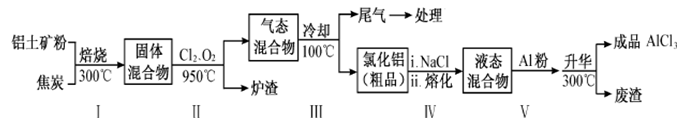
已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是 (只要求写出一种);
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是 ;
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1kJ ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2kJ ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为 ;
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为 ;
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是 。
25.(10分)考生可以任选一题作答
Ⅰ【化学—选修3:物质结构与性质】(15分)A、B、C、D为原子序数依次增大的四种元素,A2﹣和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为 ;
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是
,A和B 的氢化物
所属的晶体类型分别为 和 ;
(3)C和D反应可生成组成比为1︰3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 ;
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a = 0.566 nm,F的化学式为 ,列式计算晶体F的密度(g.cm-3) 。
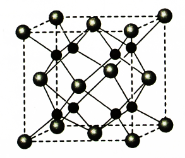
Ⅱ【化学---有机化学基础】
菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如下:
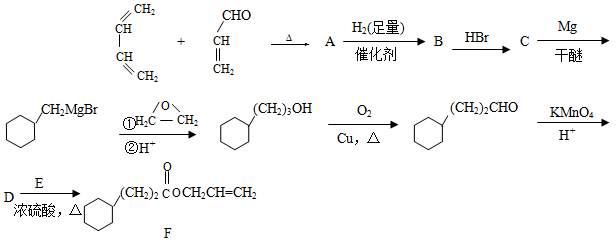
已知: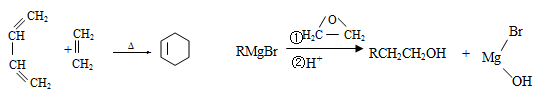
(1)A的结构简式为_________________,A中所含官能团的名称是______________________;
(2)由A生成B的反应类型是____________,E的某同分异构体只有一种相同化学环境的氢,该同分异构体的结构简式为_________________;
(3)写出D和E反应生成F的化学方程式____________________________________________;
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试剂任选)。
合成路线流程图示例:![]()
吉大附中高中部2015-2016学年上学期高三年级
第一次摸底考试化学试题参考答案及评分标准
注:化学方程式和离子方程式的书写反应物和产物均正确,计量数错误扣1分,全正确满分,其他情况均为0分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | C | C | B | D | C | A | B | B | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | D | A | B | C | A | D | D | B | C | D |
21.(12分)
Ⅰ(1) Cl2+2OH﹣═Cl﹣+ClO﹣+H2O (2分)
(2) Fe3+(2分)
(3)① 硫元素(也可写-2价硫元素,或-2价S) (2分)
② 16(2分)
Ⅱ. Na+[![]() (2分) CN﹣+H2O2+H2O═NH3↑+HCO3﹣(2分)
(2分) CN﹣+H2O2+H2O═NH3↑+HCO3﹣(2分)
22.(8分,每空2分)
(1)NaH(2分)
(2)4NaH+AlCl3=NaAlH4+3NaCl(2分)
(3)NaAlH4+2H2O=NaAlO2+4H2↑(2分)
(4) 3NaH+Fe2O3=2Fe+3NaOH(2分)
23.(7分)①2Fe3++SO32-+H2O =2Fe2++SO42-+2H+(1分)
②2Fe3++3SO32-+3H2O =2Fe(OH)3↓+3SO2↑(1分,不写“↓”和“↑”不扣分,产物写H2SO3也得分)
③Fe(OH)3胶体(1分,不写胶体不得分)
④Ba2++SO42-=BaSO4↓(1分)
⑤Fe3+和SO32-在溶液中既发生氧化还原反应,又发生互促水解反应(1分)
⑥Na2SO3溶液(1分,不写“溶液”也得分)
⑦判断反应前Na2SO3溶液是否已经部分被氧化(1分)
24.(13分)(1)Al3++3H2O![]() Al(OH)3(胶体)+3H+(2分,不写胶体扣1分)
Al(OH)3(胶体)+3H+(2分,不写胶体扣1分)
(2)①防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率。
(2分,答对一点得2分)
②Fe或铁(2分);
③Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g) ΔH=+174.9kJ/mol;(2分,不写“+”不得分)
④NaCl、NaClO、Na2CO3(3分,少写一个扣1分,错写不得分) ;
⑤除去FeCl3,提高AlCl3纯度(产率)(2分)。
25.Ⅰ【化学—物质结构与性质】(共计10分,每空1分)
(1)O(1分);1s22s22p63s23p3(或[Ne] 3s23p3)(1分)
(2)O3(1分);O3为极性分子且相对分子质量较大,范德华力大(1分,答对一点得满分);
分子晶体(1分);离子晶体(1分)
(3)三角锥形(1分);sp3(1分)
(4)Na2O(1分);![]() (1分)
(1分)
25.Ⅱ【化学---有机化学基础】(共计10分,除特殊标出外,每空2分)
(1)![]() (1分),碳碳双键、醛基(1分,少写或错写不得分)。
(1分),碳碳双键、醛基(1分,少写或错写不得分)。
(2)加成(或还原)反应(2分);CH3![]() CH3,(2分)
CH3,(2分)
(3)
![]() —(CH2)2COOH+CH2=CHCH2OH
—(CH2)2COOH+CH2=CHCH2OH![]()
![]() —(CH2)2COO CH2CH= CH2+H2O
—(CH2)2COO CH2CH= CH2+H2O
(2分,不写条件不得分,不写H2O不得分,)
(4)CH3CH2Br![]() CH3CH2MgBr
CH3CH2MgBr CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
(2分,不写条件0分,其他合成途径均0分,)