
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
顺义区2016届高三第一次统练
理科综合能力测试
本试卷共14页,共300分。考试时长150分钟。考生务必将答案答在答题卡上,在试卷上作答无效。
以下数据可供解题时参考:
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5
第一部分(选择题 共120分)
本部分共20小题,每小题6分,共120分。在每小题列出的四个选项中,选出最符合题目要求的一项。
6. 下列变化过程不涉及化学反应的是
| A | B | C | D |
 |  |  |  |
| 陶瓷的烧制 | 活字印刷排版术 | 鞭炮和烟火的燃放 | 司母戊鼎表面出现铜绿 |
7.下列有关性质的比较,不能用元素周期律解释的是
A.密度: Na>K B.稳定性:HCl>HBr
C.还原性:I¯>Br¯ D.碱性:KOH>NaOH
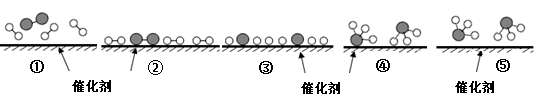
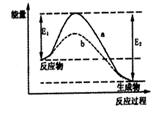
8. N2和 H2在催化剂表面合成氨的微观历程及能量变化的示意图如下,用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是
分别表示N2、H2、NH3,下列说法正确的是
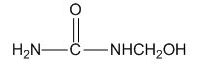
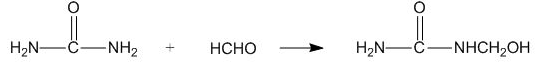 9. 脲醛塑料(UF),俗称“电玉”,可制得多种制品,如日用品、电器元件等, 在一定条件下合成脲醛塑料的反应如下,下列说法中正确的是
9. 脲醛塑料(UF),俗称“电玉”,可制得多种制品,如日用品、电器元件等, 在一定条件下合成脲醛塑料的反应如下,下列说法中正确的是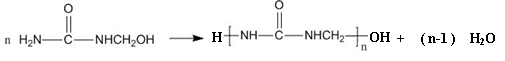
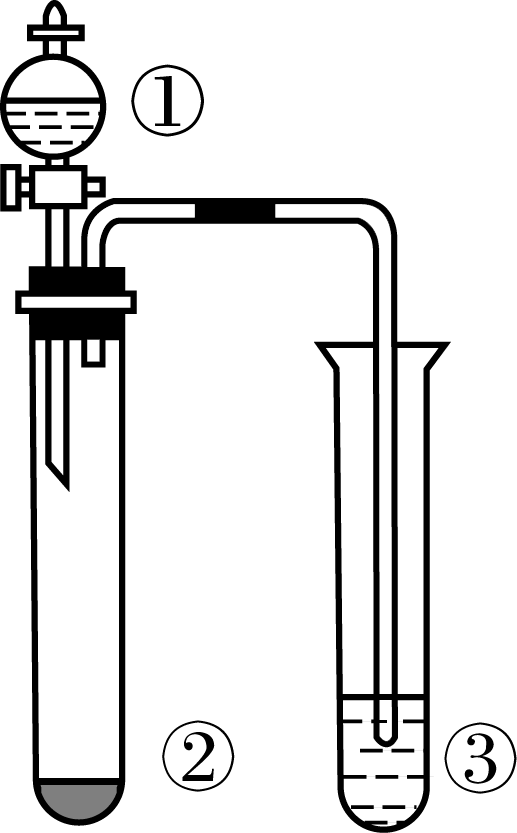 11.下表所列实验探究,利用右图所示实验装置,能得出相应实验结论的是
11.下表所列实验探究,利用右图所示实验装置,能得出相应实验结论的是| 选项 | ① | ② | ③ | 实验结论 |
| A | 水 | 电石 | CuSO4溶液 | 乙炔具有还原性 |
| B | 浓硝酸 | Cu | KI-淀粉溶液 | 氧化性:NO2>KI |
| C | 浓盐酸 | KMnO4 | KI-淀粉溶液 | 氧化性:KMnO4>Cl2>I2 |
| D | 稀硫酸 | Na2S | AgNO3与AgCl的浊液 | 溶解度:AgCl>Ag2S |
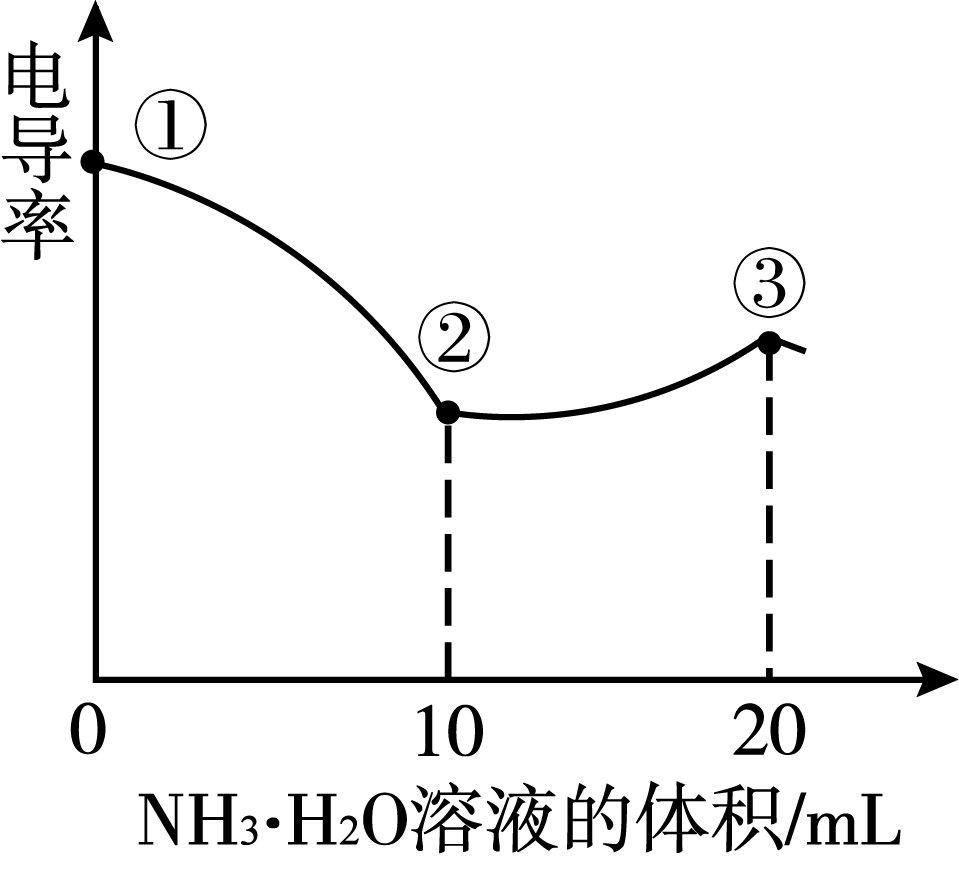 12. 电导率可用于衡量电解质溶液导电能力大小,且电导率越
12. 电导率可用于衡量电解质溶液导电能力大小,且电导率越 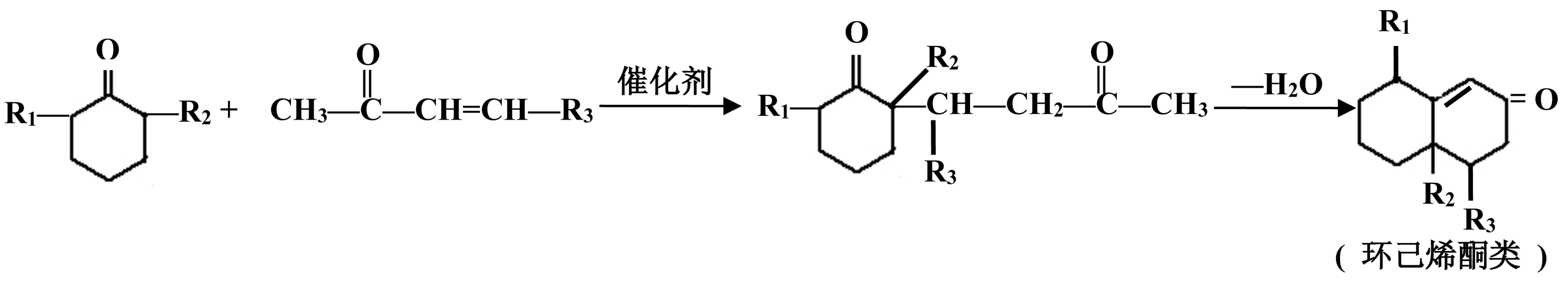
Ⅰ步:
Ⅱ步:
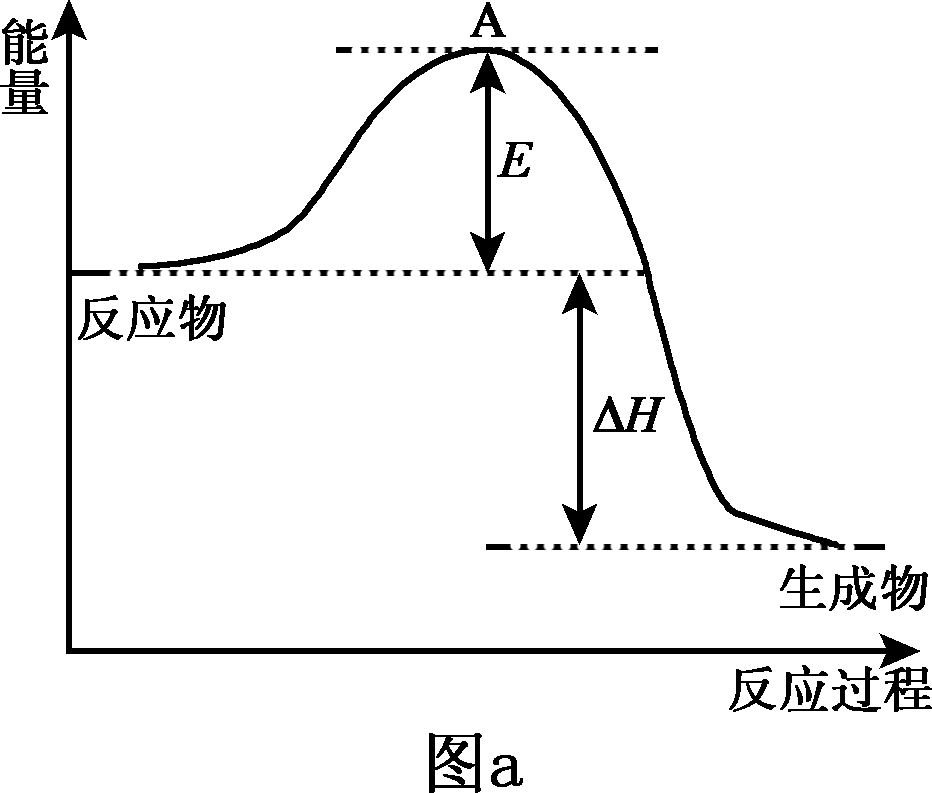
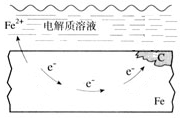
(3)钢铁锈蚀图示如图c所示:
① 用箭头画出图c中电子的运动方向
② 请你分析高铁铁轨锈蚀的原因是 。
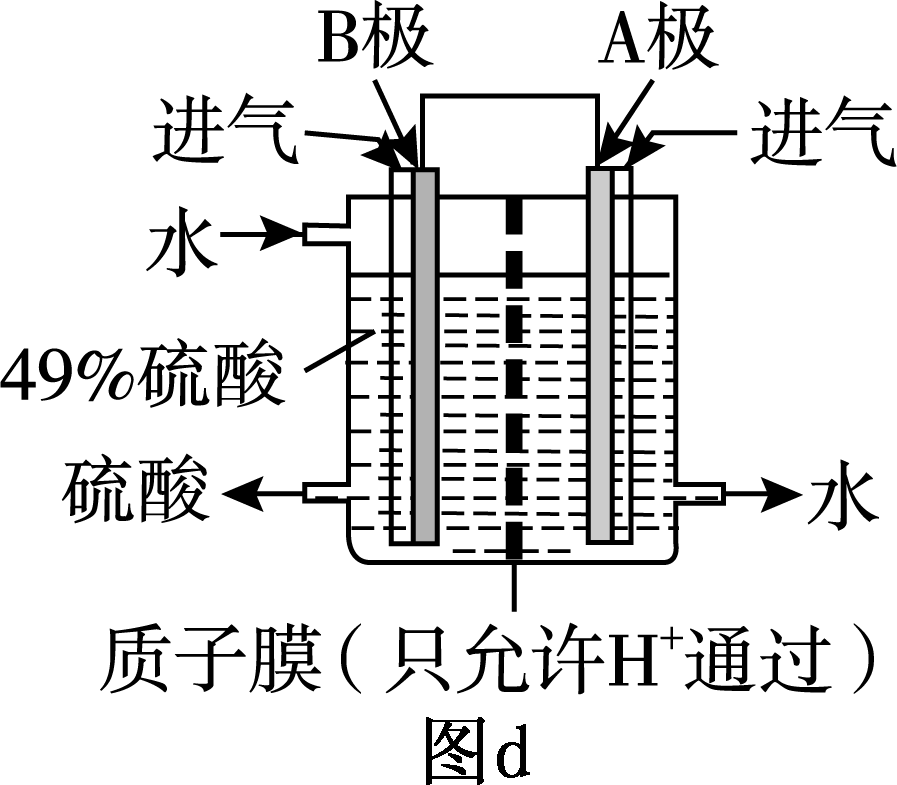
(4)我国的科技人员为了消除SO2的污染,利用原电池原理,变废为宝,设计由SO2和O2
来制备硫酸,设计装置如图d所示,电极A、B为多孔的材料。
① A极为 (填“正极”或“负极”)。
② B极的电极反应式是 。
27. (14分) 某含锰矿物的主要成分有MnCO3、MnO2、FeCO3、SiO2、Al2O3等。已知FeCO3、MnCO3难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,主要物质转化关系如下:
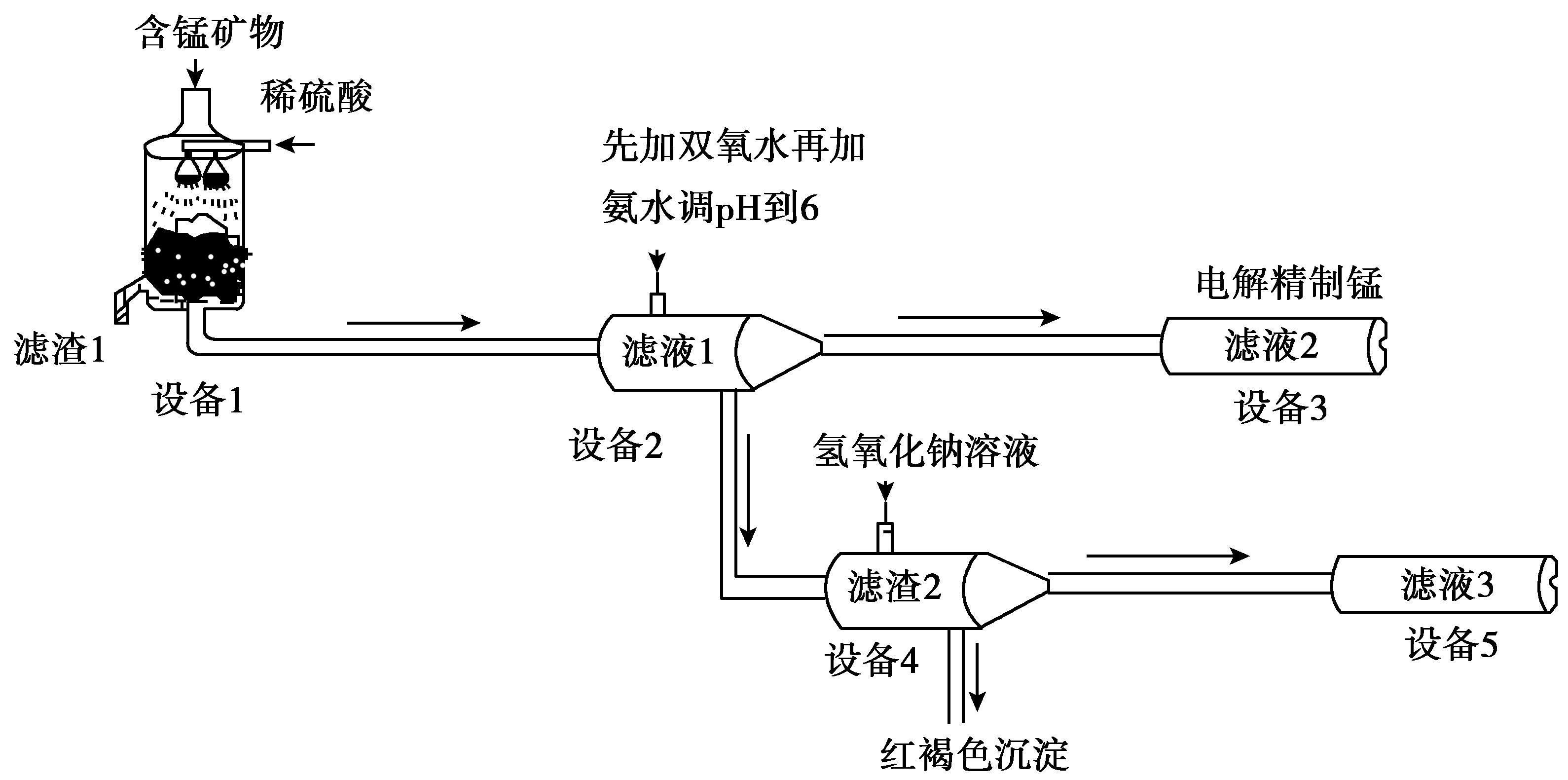
(1)设备1中反应后,滤液1里锰元素只以Mn2+的形式存在,且滤渣1中也无MnO2。滤渣1的主要成分是 (填化学式)。
(2)设备1中发生氧化还原反应的离子方程式是 。
(3)设备2中加足量双氧水的作用是 。
设计实验方案检验滤液2中是否存在Fe2+: 。
(4)设备4中加入过量氢氧化钠溶液,沉淀部分溶解,。用化学平衡移动原理解释原因: 。
(5)设备3中用阴离子膜法提取金属锰的电解装置图如下:
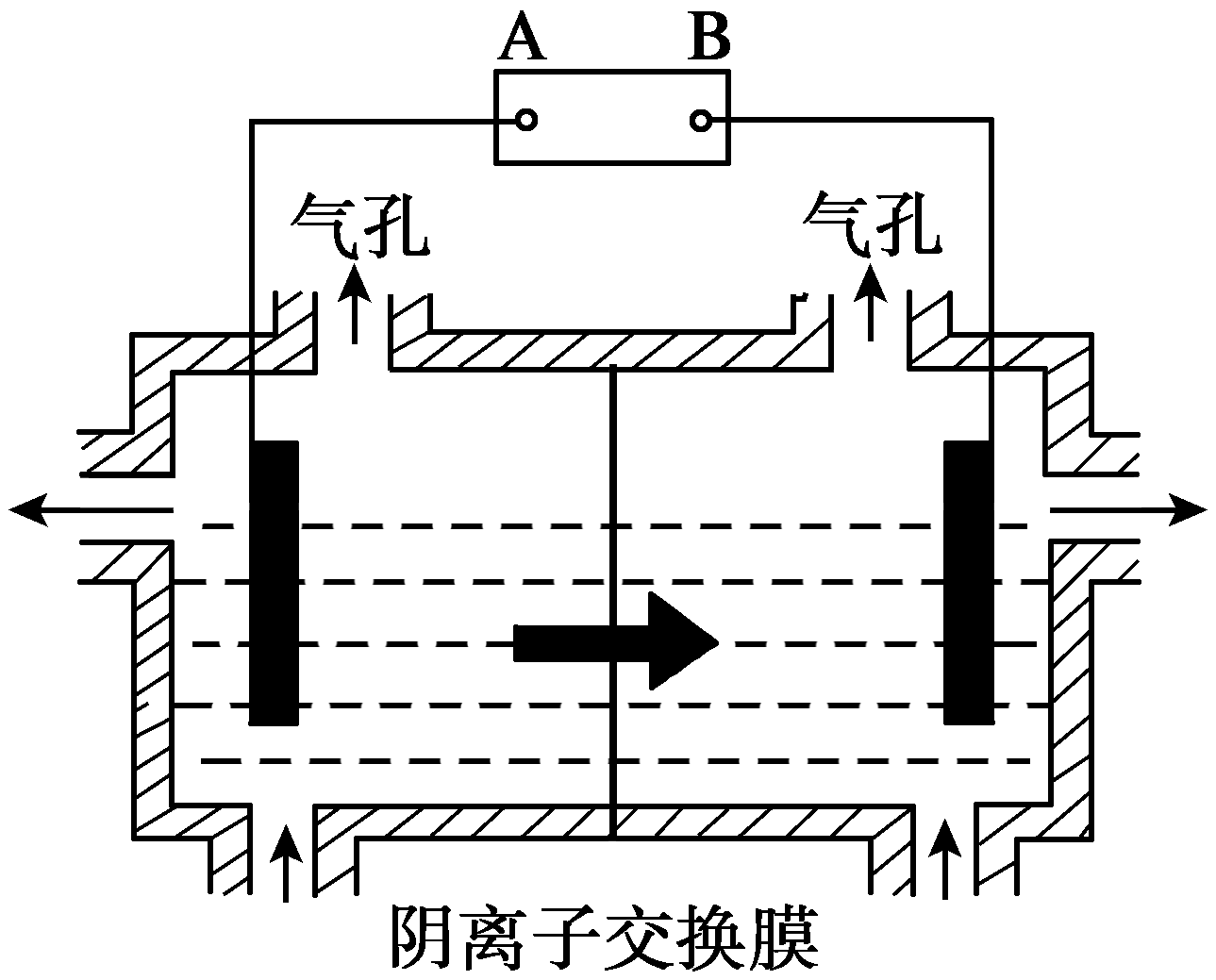
① 电解装置中箭头表示溶液中阴离子移动的方向,则A电极是直流电源的 极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为 。
② 该工艺之所以采用阴离子交换膜,是为了防止Mn2+进入阳极区发生副反应生成MnO2造成资源浪费,写出该副反应的电极反应式 。
28.(14分)某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
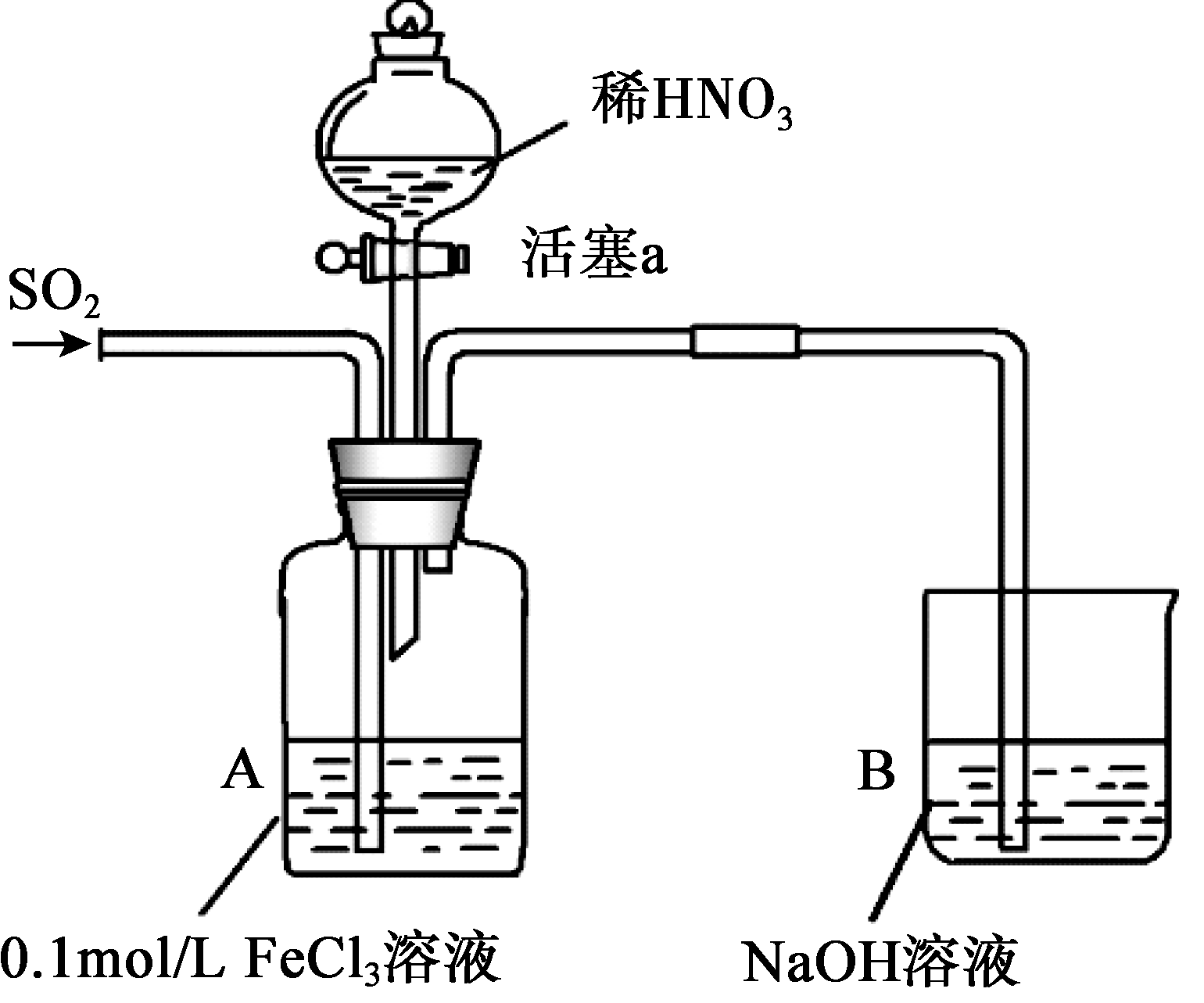
实验记录如下:
| 实验序号 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
| II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
| III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a。 | A中浅绿色溶液最终变为黄色。 |
| IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中注入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学用语和简单文字叙述): 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3++ 6SO2![]() Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
(3)实验II中发生反应的离子方程式是 。
(4)实验III中,浅绿色溶液变为黄色的原因是 。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的方程式是 。
(6)综合上述实验得出的结论是:在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。请从微粒变化的角度解释 。
顺义区2016届高三第一次统练
理科综合能力测试答案
第一部分第二部分(选择题 共120分)
6.B 7.A 8.C 9.B 10 .D 11.C 12.D
第二部分(非选择题 共180分)
25. (16分) ( 每空 2 分 )
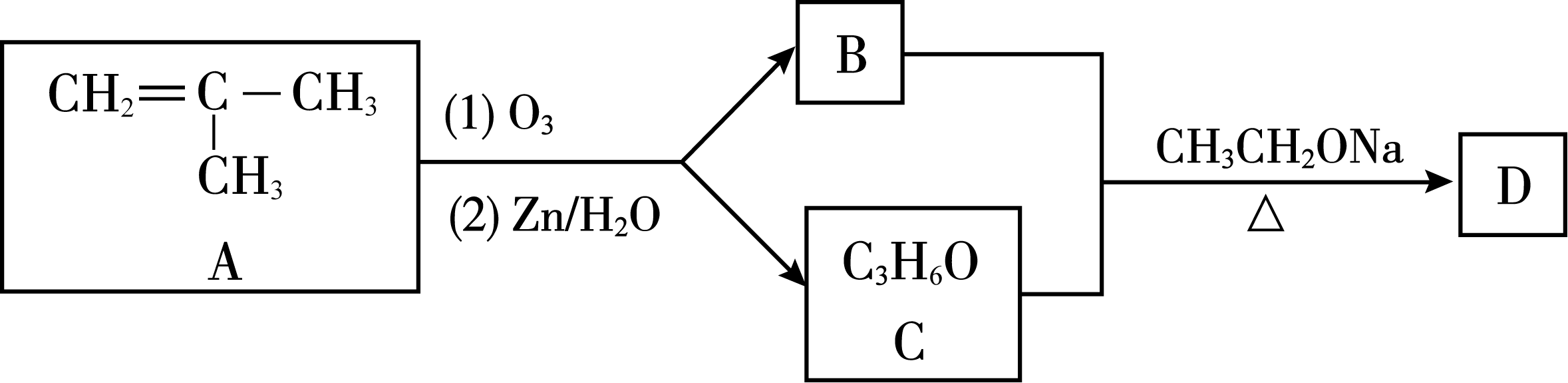
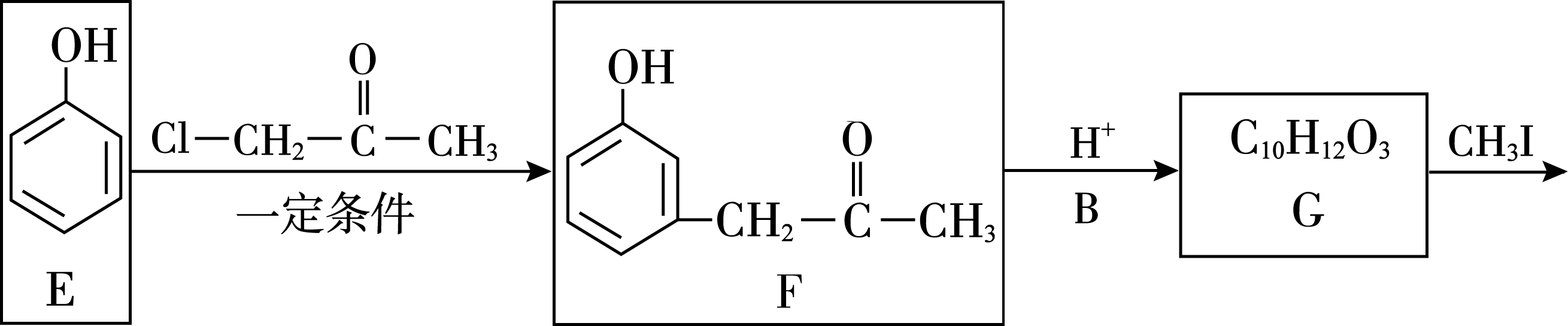
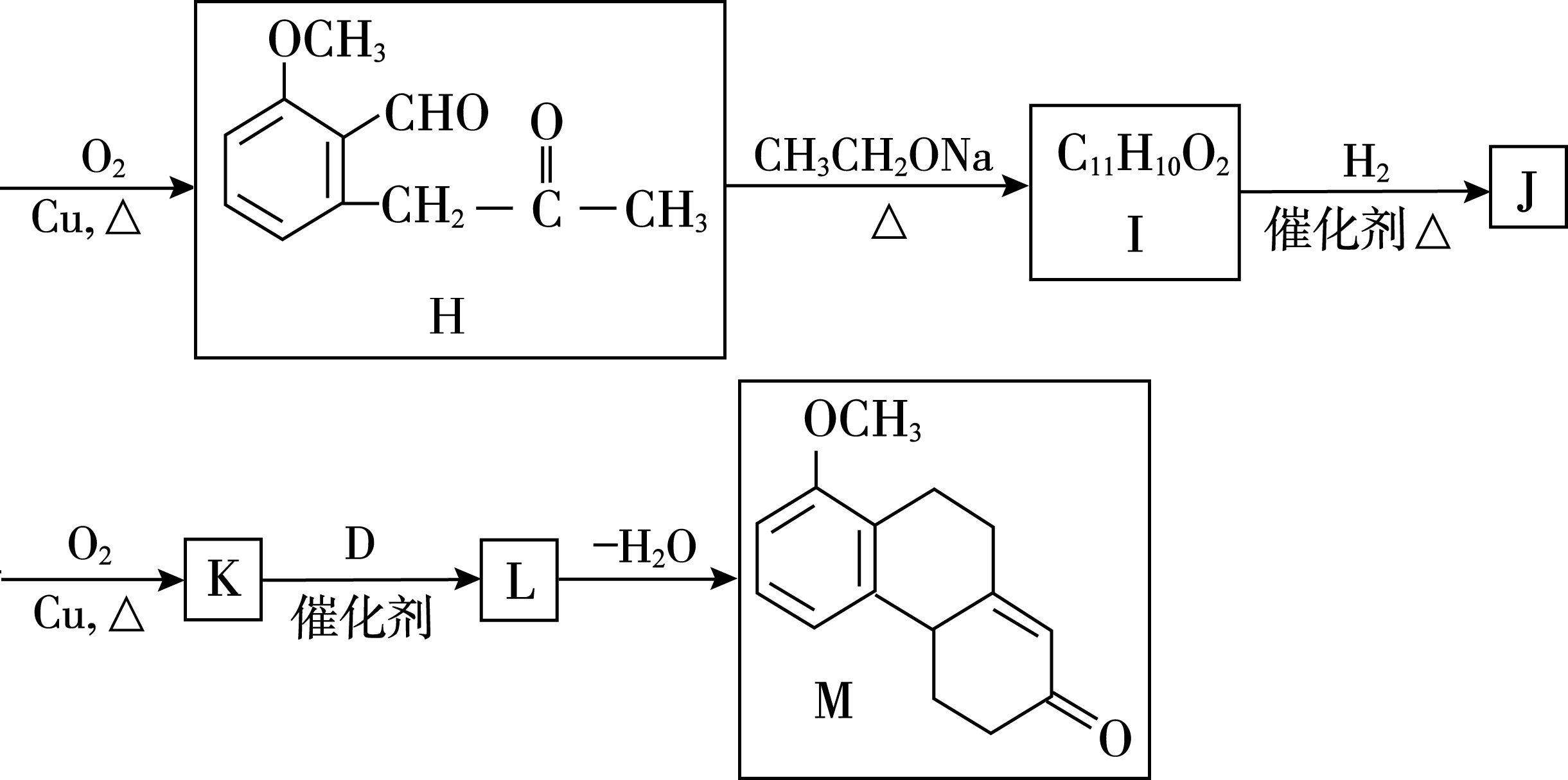
(1)2-甲基-1- 丙烯 ( 或2-甲基丙烯或甲基丙烯 )
(2)醛基
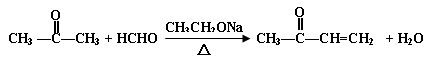
(3)
(4)取代反应
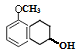
(5)
(6)
(7)5种,
CH—CH2—O—C—H CH—O—C—H
—C—O—C—H
26.(14分)
(1)SO2+H2O![]() H2SO32H2SO3 + O2
H2SO32H2SO3 + O2![]() 2H2SO4……………………………(2分)
2H2SO4……………………………(2分)
(或2SO2+O2![]() 2SO3SO3 + H2O = H2SO4)
2SO3SO3 + H2O = H2SO4)
(2)①-198 …………………………………………………………………………(2分)
因为催化剂改变了反应历程,使活化能E降低 ……………………………(2分)
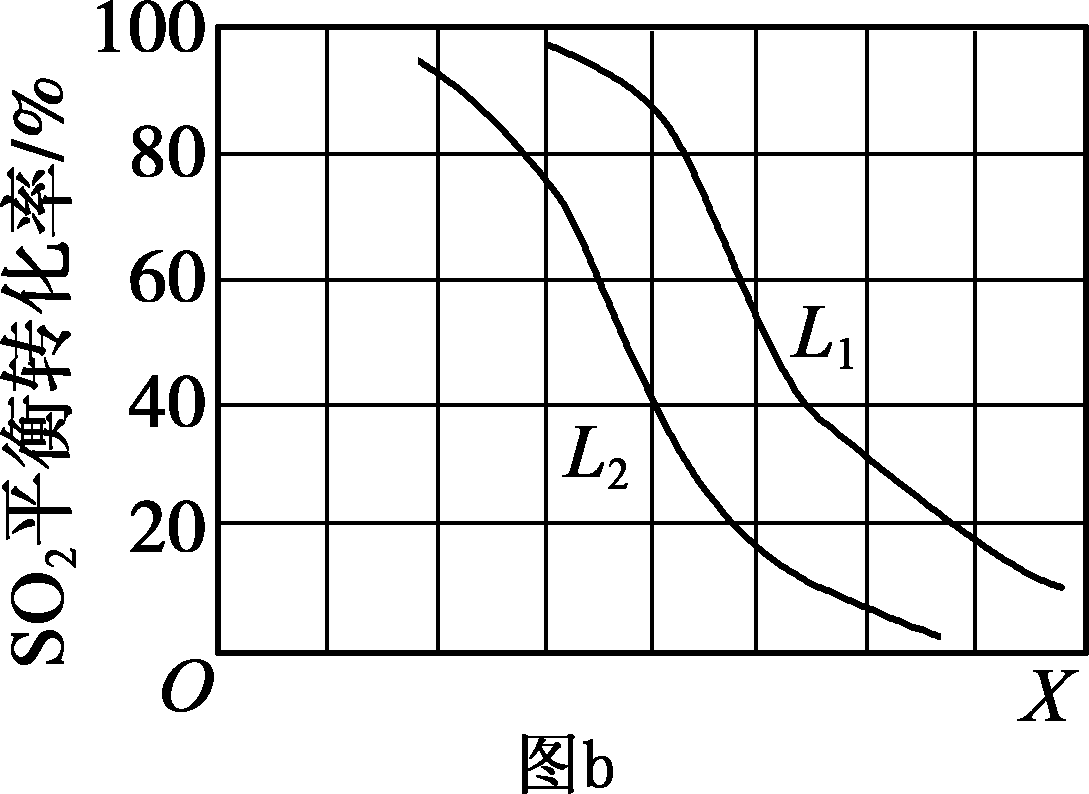
② a. 温度 …………………………………………………………………………(1分)
b.L1>L22SO2+O2![]() 2SO3反应的ΔH=-198 kJ/mol,是放热反应。当压强一定时,温度升高,平衡左移,SO2平衡转化率减小。………………(2分)
2SO3反应的ΔH=-198 kJ/mol,是放热反应。当压强一定时,温度升高,平衡左移,SO2平衡转化率减小。………………(2分)
 (3)① ……………………………………………………………………………………(1分)
(3)① ……………………………………………………………………………………(1分)
② Fe-2e- =Fe2+ ; 由于电解质溶液中有H2CO3溶液,电离出氢离子,2H++2e-=
H2↑发生析氢腐蚀。电解质中又溶于氧气,O2+4e- + 2H2O =4OH-,发生吸氧腐蚀。
……………………………………………………………………………………(2分)
(4)① 正极 ……………………………………………………………………………(1分)
②SO2+2H2O-2e-═SO42-+4H+……………………………………………………(1分)
27.(14分)
(1)SiO2………………………………………………………………………………(2分)
(2)2Fe2+ + MnO2+4H+ = 2Fe3++Mn2++2H2O …………………………………(2分)
或2FeCO3+MnO2+8H+= 2Fe3++Mn2++CO2↑+4H2O
(3)将Fe2+完全氧化为Fe3+……………………………………………………………(2分)
取滤液2,加入铁氰化钾溶液,如果有蓝色沉淀产生,则有Fe2+,否则没有Fe2+。
……………………………………………………………(2分)
(4)滤渣2中存在Al(OH)3,存在电离平衡: Al3++3OH—![]() Al(OH)3
Al(OH)3![]() AlO2—+H++H2O
AlO2—+H++H2O
加入NaOH溶液,H+被中和,浓度减低, Al(OH)3不断溶解。……………………(2分)
(5)①负极 ………………………………………………………………………………(1分)
4OH——4e—=2H2O+O2↑ ………………………………………………………(1分)
② Mn2++2H2O-2e-=MnO2+4H+……………………………………………(2分)
28. (14分)
(1)Fe3++3H2O![]() Fe(OH)3+3H+;加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解。
Fe(OH)3+3H+;加入盐酸,增大c(H+),平衡左移,抑制Fe3+水解。
………………………………………………………………………………(2分)
(2)Fe3+和SO2生成红棕色的Fe(SO2)63+反应速率较快:Fe3++6SO2![]() Fe(SO2)63+;而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液。…………………(3分)
Fe(SO2)63+;而反应2Fe3++SO2+2H2O=2Fe2++SO42-+4H+反应缓慢,但是反应限度较大,使溶液中c(Fe3+)降低,平衡逆向移动,红棕色逐渐褪去,最终得到浅绿色溶液。…………………(3分)
(3)Ba2+ + SO42- = BaSO4↓ …………………………………………………………(2分)
(4)3Fe2++4H++ NO3-= 3Fe3++NO↑+2H2O …………………………………………(2分)
(5)2NO+ O2= 2NO2…………………………………………………………(2分)
(6)实验II中溶液中检出Fe2+和SO42-,说明Fe3+氧化SO2生成SO42-,氧化性Fe3+>SO42-;实验III中溶液变黄色、IV中检出Fe3+和NO生成,说明酸性条件下NO3-氧化Fe2+,氧化性NO3->Fe3+;所以,在酸性条件下,氧化性强弱是:NO3->Fe3+>SO42-。……………(3分)