
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
温馨提示:理科综合共300分,考试用时150分钟。化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。祝各位考生考试顺利!
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将正确答案填涂在答题卡相应位置上。如需改动,用橡皮擦干净后,再选涂其他答案标号。
2.本卷共6题,每题6分,共36分。每小题给出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 P 31 S 32 Cl 35.5 K 39 Ca 40 Fe 56 Cu 64 Zn 65 Br 80 I 127
1.化学与社会、生产、生活紧切相关。下列说法正确的是( )。
A.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质
B.石油干馏可得到石油气、汽油、煤油、柴油等
C.从海水中提取物质都必须通过化学反应才能实现
D.纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污
2.下列说法正确的是( )。
A.强电解质一定易溶于水
B.常温下,强酸和弱酸的浓度相同时,强酸中水的电离程度比弱酸的水的电离程度小
C.对可逆反应,升高温度一定存在v(正)>v(逆)
D.钢铁在海水中发生电化腐蚀时,铁是正极被氧化
3.下列单质或化合物性质的描述正确的是( )。
A.NaHSO4水溶液显中性
B.SiO2与酸、碱均不反应
C.NO2溶于水时发生氧化还原反应
D.Fe在足量Cl2中燃烧生成FeCl2和FeCl3
4.实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是( )。
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液、水 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、0. 1000 mol·L-1盐酸 |
5.某种碳酸饮料中主要含柠檬酸、碳酸、白砂糖、苯甲酸钠等成分,常温下测得其pH约为3.5,下列说法不正确的是( )。
A.常温下,该碳酸饮料中KW的值大于纯水中KW的值
B.该碳酸饮料中水的电离受到抑制
C.柠檬酸的电离会抑制碳酸的电离
D.打开瓶盖冒出大量气泡,是因为压强减小,降低了CO2的溶解度
6.某原电池装置如下图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )。
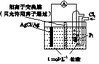
A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或或签字笔将答案写在试卷上。
2.本卷共4题,共64分。
7.(14分) V、W、X、Y、Z是原子序数依次递减的五种常见元素。X元素是地壳中含量最多的元素,Y、Z组成气态化合物M的水溶液呈碱性,W的单质在X2中燃烧的产物可使品红溶液褪色,V是一种历史悠久,应用广泛的金属元素。请回答:
(1)Y元素在周期表中的位置是 ;写出X、Z两种元素组成的一种化合物的一种用途 。
(2)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且属于氧化还原反应,请写出该反应的化学方程式 。
(3)X、Y、Z三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。常温下该盐的水溶液的pH 7(填“大于”、“小于”或“等于”)。
(4)W(s)+O2(g) WO2(g);![]() H1W(g)+O2(g) WO2(g);
H1W(g)+O2(g) WO2(g);![]() H2
H2
则![]() Hl(填“>”或“<”或“=”)
Hl(填“>”或“<”或“=”)![]() H2。
H2。
(5)有人设想寻求合适的催化剂和电极材料,以Y2、Z2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式 ;放电时溶液中H+移向 (填“正”或“负”)极。
(6)若将V金属投入到硫酸溶液中,生成了浅绿色溶液N。写出N的溶液与K2Cr2O7酸性溶液反应的离子方程式: 。
8.(18分)化合物A是合成天然橡胶的单体,分子式为C5H8。A的一系列反应如下(部分反应条件略去):
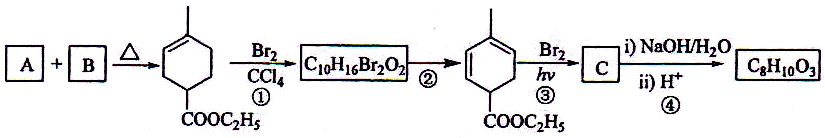
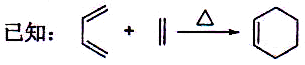
回答下列问题:
(1)A的结构简式为 ,化学名称是 。
(2)B的分子式为 。
(3)②的反应方程式为 。
(4)①和③的反应类型分别是 , ;
(5)C为单溴代物,分子中有两个- CH2-,写出④中第一步反应的化学方程式为 。
(6)写出所有A的同分异构体中不含聚集二烯(C=C=C)结构单元的链状二烯烃的同分异构体的结构简式 。
9.(18分)溴化钙是一种溴化物,用于石油钻井,也用于制造溴化铵及光敏纸、灭火剂、制冷剂等。制备CaBr2·2H2O的主要流程如下:
(1)制备FeBr2时可用如下实验装置(部分夹持装置略去),水浴加热。
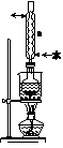
仪器a的名称是________,与液溴的反应温度不能超过40℃的原因是
。
(2)滤渣的成分可能是 。
(3)试剂M是 ,加入M的目的是 。
(4)操作Ⅱ的步骤为蒸发浓缩、 、 、洗涤、干燥
(5)溴化钙晶体中溴离子的检验:将少量溴化钙晶体溶于水,加入 ,实验现象为 ,发生反应的离子方程式为 。
(6)将氨气通入石灰乳,加入溴,于65°C进行反应也可制得溴化钙,此反应中还会生成一种无色气体,写出反应的化学方程式 。
(7)制得的CaBr2·2H2O可以通过以下方法测定纯度:称取5.00g样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却,称量。得到2.00g固体,则CaBr2·2H2O的质量分数为 。
10.(14分)尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为______________________________。
(2)当氨碳比=4时,CO2的转化率随时间的变化关系如下图所示。
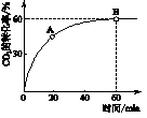
①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”、“小于”或“等于”)。
②NH3的平衡转化率为________。
③一定温度下,在一个容积不变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母,下同)。
a.容器中的压强不变b.3mol N—H键断裂的同时断裂2 molH—O键
c.c(CO2)=c(H2O)d..c(CO2)的浓度保持不变
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图所示。
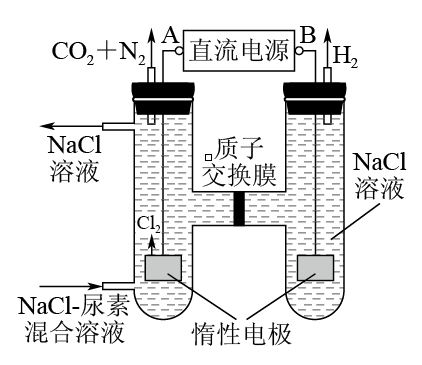
①电源的负极为________(填“A”或“B”)。
②阳极室中发生的反应依次为____________________________________________、_______________________________________________。
③电解结束后,阴极室溶液的pH与电解前相比将________(填“增大”、“减小”或“不变”);若两极共收集到气体11.2 L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
和平区2014-2015学年度第二学期高三年级第四次质量调查
理科综合化学学科试卷参考答案
第Ⅰ卷
选择题本卷共6小题,每题6分,共36分。
1.D 2.B 3.C 4.B 5.A 6.D
第Ⅱ卷
本卷共4小题,共64分。
7.(共14分)
(1)第2周期VA族(2分);
绿色氧化剂(H2O2)(或溶剂(H2O)或其它合理答案)(2分)
(2)3NO2+H2O== 2HNO3+NO(2分)
(3)小于(1分)
(4)>(2分)
(5)N2+ 6e-+ 8H+==2NH4+(2分) 正(1分)
(6)6Fe2++ Cr2O72-+14H+==6Fe3++ 2Cr3++7H2O(2分)
8.(共18分)
(1)![]() (2分)2—甲基—1,3—丁二烯(或异戊二烯)(2分)
(2分)2—甲基—1,3—丁二烯(或异戊二烯)(2分)
(2)C5H8O2(2分)
(3)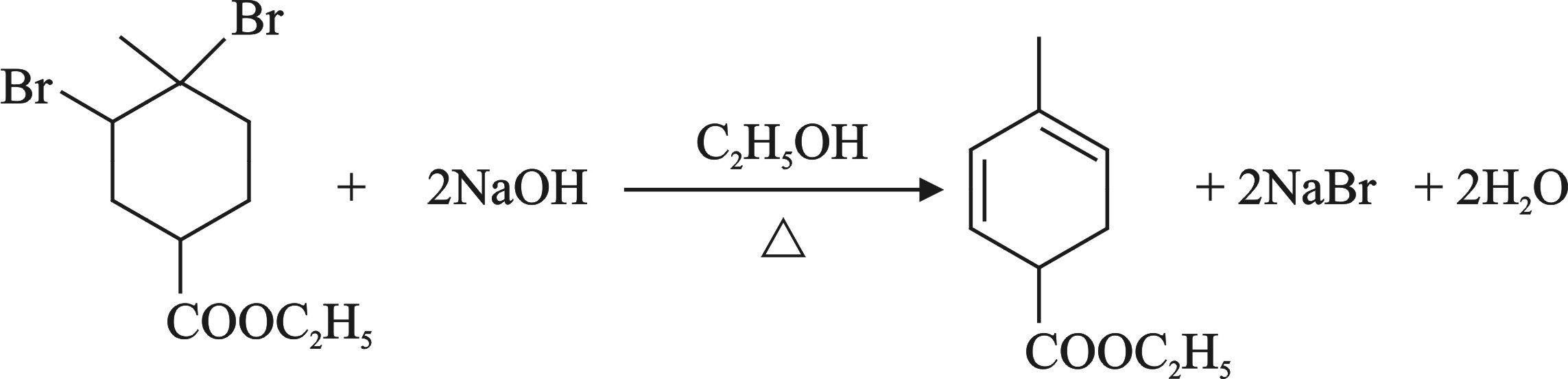 (2分)
(2分)
(4)加成反应(1分) 消去反应(1分)
(5)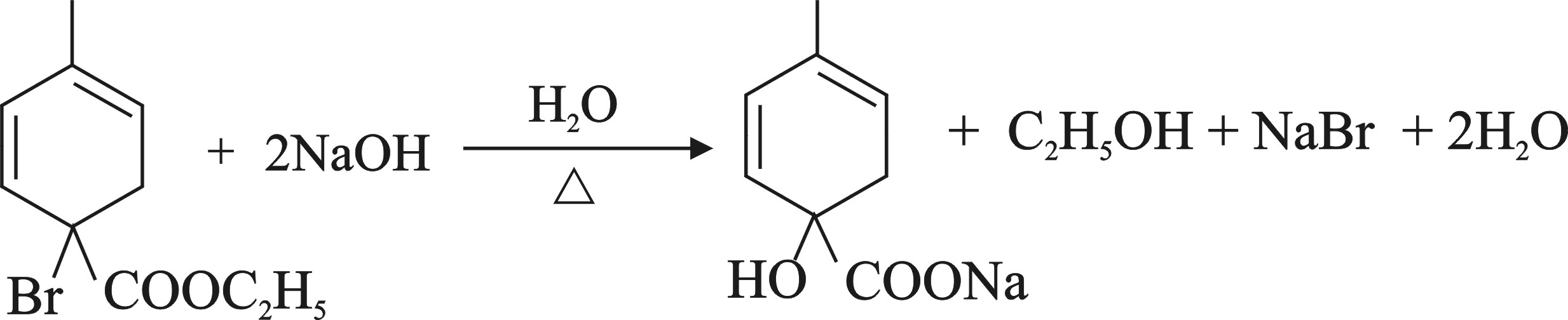 (2分)
(2分)
(6)![]() (2分)
(2分)![]() (2分)
(2分)![]() (2分)
(2分)
9.(共18分)
(1)冷凝管;(1分)防止液溴挥发,使原料利用率降低。(2分)
(2)Fe、 Fe(OH)2、Fe(OH)3(2分)
(3)HBr(1分),除去过量的Ca(OH)2(1分)
(4)冷却结晶、过滤(2分)
(5)硝酸酸化的AgNO3溶液 ;(2分)产生淡黄色浑浊(1分);
Br-+Ag+=AgBr↓(2分)
(6)3 Ca(OH)2+ 3Br2+ 2NH3= 3CaBr2+ N2↑+ 6H2O(2分)
(7)94.40%(2分)
10.(共14分)
(1)2NH3+CO2![]() CO(NH2)2+H2O (2分)
CO(NH2)2+H2O (2分)
(2)①小于(1分)
②30%(1分)
③a d(2分)
(3)①B(1分)
②2Cl--2e-===Cl2↑(2分)
CO(NH2)2+3Cl2+H2O===N2+CO2+6HCl(2分)
③不变(1分) 6.0(2分)