
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
南开区2014~2015学年度高三理科综合能力测试(二)
(化学部分)
理科综合共300分,考试用时150分钟。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至2页,第Ⅱ卷3至6页,共100分。
第Ⅰ卷
注意事项:
1.答第I卷前,考生务必将自己的姓名、准考号、科目涂写在答题卡上。
2.每题选出答案后,用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。I卷答案答在试卷上无效。
3.本卷共6题,每题6分,共36分。在每题列出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5
1.化学与社会、生产、生活密切相关。下列说法不正确的是
A.通过红外光谱分析可以区分乙醇与乙酸乙酯
B.煎炸食物的花生油和牛油都是可皂化的饱和酯类
C.淀粉可用于制备葡萄糖、酿制食醋,还可作药片的赋形剂
D.利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法
2.下列叙述正确的是
A.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
B.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
C.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2
D.实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法
3.25℃时,下列分子或离子在指定溶液中一定能大量共存的一组是
A.pH=1的溶液中:K+、Cr2O72—、C6H5OH、CO32—
B.c(H+) =1×10—13mol/L的溶液中:Cu2+、Na+、Cl—、SO42—
C.0.1 mol/L NH4HCO3溶液中:K+、Na+、Cl—、NO3—
D.0.1 mol/L Na2SiO3溶液中:K+、Cl—、NO3—、CO2
4.下列溶液中粒子的物质的量浓度关系正确的是
A.20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,
所得溶液中:c(CH3COO—) >c(Cl—) >c(CH3COOH) >c(H+)
B.0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:
c(Na+) >c(CO32—) >c(HCO3—) >c(OH—)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c(H+) +c(Cl—) >c(NH4+) +c(OH—)
D.0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:
c(OH—) >c(H+) +c(CH3COOH)
5.在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:
![]() X(g) + Y(g) 2Z(g) △H< 0,一段时间后达到平衡。反应过程中测定的数据如下表:
X(g) + Y(g) 2Z(g) △H< 0,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前2 min的平均速率v(Z) = 2.0×10—3mol/(L·min)
B.该温度下此反应的平衡常数K=144
C.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
D.其他条件不变,降低温度,反应达到新平衡前v(逆) >v(正)
6.如右图所示,将纯Fe棒和石墨棒插入1 L 饱和NaCl溶液中。
下列说法正确的是
A.去掉电源,将M、N用导线直接相连,则Fe棒上产生气泡
B.M接电源负极,N接电源正极,Fe棒不会被腐蚀,属于牺牲
阳极的阴极保护法
C.M接电源正极,N接电源负极,将石墨棒换成Cu棒,电
解质溶液换成CuSO4溶液,则可实现在铁棒上镀铜
D.去掉电源,将M、N用导线直接相连,烧杯中的溶液换成经酸化的3% NaCl溶液,
向Fe电极区滴入2滴K3[Fe(CN)6]溶液,反应一段时间后,烧杯中产生蓝色沉淀
第Ⅱ卷
注意事项:
1.答卷前将密封线内的项目填写清楚。用钢笔或圆珠笔直接答在试卷上。
2.本卷共4题,共64分。
| 题号 | 7 | 8 | 9 | 10 | 总分 |
| 得分 |
| 得分 | 评卷人 |
7.(14分)短周期元素形成的常见非金属固体单质A与常见金属
单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E。D既能溶于强酸,也能溶于强碱。E是一种无色、有臭鸡蛋气味的气体,E在足量空气中燃烧产生有刺激性气味的气体G,G在大气中能导致酸雨的形成。E被足量NaOH溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)单质A是一种黄色晶体,质脆,易研成粉末。组成单质A的元素在周期表中的位置是_______________,D的化学式是________,F中存在的化学键类型是____________。
(2)B与NaOH溶液反应的化学方程式为_____________________________________。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物的化学式为_______________,当生成2 mol ClO2时,转移电子_______mol。
(4)工业上,E常用氨水吸收,产物为酸式盐。一定条件下向该盐溶液中通入空气,得到单质A并使吸收液再生,写出再生反应的化学方程式:
_________________________________________________。
(5)溶液F显_____性,用离子方程式解释原因:______________________________。
(6)H与过氧化钠的结构和化学性质相似,H的电子式为_______________________。
| 得分 | 评卷人 |
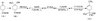
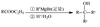
已知:
请回答下列问题:
(1)A所含官能团的名称是__________________________。
(2)A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式:
_______________________________________________________________。
(3)B的分子式为______________;写出同时满足下列条件的B的链状同分异构体的结构简式:_____________________________________。
① 核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
(4)B C、E F的反应类型分别为_______________、_______________。
![]() (5)C D的化学方程式为______________________________________________。
(5)C D的化学方程式为______________________________________________。
(6)试剂Y的结构简式为___________________。
(7)通过常温下的反应,区别E、F和G的试剂是___________和____________。
(8)G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式:____________________________。
| 得分 | 评卷人 |
Ⅰ. 从海水中提取食盐和溴的过程如下:

(1)请列举海水淡化的三种方法:_____________、_____________、_____________。
(2)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42—等杂质。某次除杂操作时,往粗盐水中先加入过量的______(填化学式),至沉淀不再产生后,继续加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42—,已知Ksp(BaSO4) = 1.1×10—10、Ksp(BaCO3) = 5.1×10—9,请分析滤液中仍含有SO42—的原因是:___________________________________________________________。将提纯后的NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、_______、_______或H2、_______。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br—,其目的为____________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为:
__________________________________________________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是__________________________________。
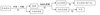 Ⅱ. 按以下实验方案可从海洋动物炳海鞘中提取具有抗肿瘤活性的天然产物。
Ⅱ. 按以下实验方案可从海洋动物炳海鞘中提取具有抗肿瘤活性的天然产物。
(5)下列叙述正确的是________________(填序号)。
c. 步骤③需要用到坩埚 d. 步骤④需要蒸馏装置
Ⅲ. 海水淡化后剩余的浓海水经过一系列工艺流程可以获取其他产品,如Mg(OH)2等。浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl— | SO42— |
| 浓度/(g·L—1) | 63.7 | 28.8 | 144.6 | 46.4 |
(6)理论上,1 L浓海水最多可得到Mg(OH)2的质量为____________ g。
| 得分 | 评卷人 |
10.(14分)NOx是汽车尾气中的主要污染物之一。
(1)在实验室里,用铜与浓硝酸反应可制得NO2,现将NO2和O2同时通入水中,当
n(NO2) : n(O2)== _______时,二者恰好完全反应生成HNO3。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
①写出该反应的热化学方程式:_________________________________________。
②随温度升高,该反应化学平衡常数的变化趋势是________________。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:______________________________________________。
②当尾气中空气过量时,转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:
12MgO< 20CaO< 38SrO< 56BaO。原因是_________________________________________
_____________________________________________________,元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
①Pt电极上发生的是_______________(填“氧化”或“还原”)反应。
②写出NiO电极的电极反应式:________________________________________。
南开区2015年高三理科综合能力测试(二) (化学答案)
1B 2D 3C 4A 5C 6D
7.(14分)
(1)第三周期第ⅥA族 Al(OH)3 离子键 (每空1分,共3分)(2)2Al + 2NaOH + 2H2O === 2NaAlO2 + 3H2↑ (2分)
一定条件
(3)Na2SO4 2 (每空1分,共2分)(4)2NH4HS + O2 ========== 2NH3·H2O + 2S↓ (2分)
(5)碱 (1分)
![]()
![]() S2—+ H2O HS— + OH—(2分)
S2—+ H2O HS— + OH—(2分)
(6) (2分)
8.(18分)
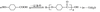 (1)羰基、羧基 (2分)
(1)羰基、羧基 (2分)
(2) (2分)
![]() (3)C8H14O3(每空2分,共4分)
(3)C8H14O3(每空2分,共4分)
(4)取代反应 酯化反应(或取代反应) (每空1分,共2分)
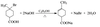 (5)
(5)
(2分)
(6)CH3MgX(X = Cl、Br、I) (2分)
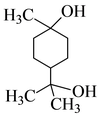 (7)NaHCO3溶液 Na (其他合理答案均可) (2分)
(7)NaHCO3溶液 Na (其他合理答案均可) (2分)
(8) (2分)
9.(18分)
Ⅰ.(1)蒸馏法、电渗析法、离子交换法(合理答案均可) (3分)
(2)BaCl2(1分)
BaSO4和BaCO3的Ksp相差不大,当溶液中存在大量CO32—时,BaSO4(s)会部分转化为BaCO3(s)(或其他合理答案) (2分)
Cl2 NaOH NaClO (3分)
(3)富集溴元素 (1分)
(4)Br2 + SO2 + 2H2O === 4H+ + SO42—+ 2Br—(2分)
强酸对设备的严重腐蚀 (1分)
Ⅱ.(5)a、b、d (3分)
Ⅲ. (6)69.6 (2分)
10.(14分)
(1)4(或4 : 1) (2分)
(2)①N2(g) + O2(g) === 2NO(g) △H=+ 183 kJ · mol-1(4分)
催化剂
(3)①2CO + 2NO ===== N2 + 2CO2(2分)
②根据Mg、Ca、Sr和Ba的质子数,得知它们均为ⅡA族元素。同一主族的元素,从上到下,原子半径逐渐增大 (2分)
(4)①还原 (1分)
②NO + O2—-2e—=== NO2(2分)
△
(以上答案仅供参考,合理答案均给分)