
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
广元市高2013级第二次高考适应性统考
化学试题
可能用到的相对原子量:H-1 C-12 O-16 Mg-24 N-14 Cu-64 Al-27
第I卷(选择题 共42分)
一、选择题(共7小题,每小题6分。每题给出的四个选项中,只有一项是符合题目要求的。)
1.化学与生产和生活密切相关,下列说法正确的是
A.聚乙烯塑料的老化是因为发生了加成反应
B.水晶项链和餐桌上的瓷盘都是硅酸盐制品
C.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质
D.在清洗地板时,84消毒液和洁厕灵(主要成分是盐酸)不能混合使用
2.下列说法或推理正确的是
A.将Fe(N03)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变红,则Fe(N03)2晶体已氧化变质
B.常温下,pH都为11的氢氧化钠溶液和氨水均加水稀释100倍,pH都变为9
C.25℃时,Ksp( BaC03)>Ksp( BaCrO4),则沉淀水体中的Ba2+选择Na2CrO4比Na2CO3好
D.将CH3CH2Br与NaOH溶液共热,冷却后取出上层溶液,加入AgNO3溶液,产生沉淀,则
CH3CH2Br在NaOH溶液中发生了水解
3.下列离子方程式正确的是
A.向FeBr2洛液中通入足量氯气:2Fe2++4Br-+3Cl=2Fe3++2Br2+6Cl-
B.Cl2通入水中:Cl2+H20 = 2H++Cl-+ClO-
C.用铜作电极电解CuSO4溶液:2Cu2+,+2H20=2Cu+O2+4H'
D。明矾溶液中滴入Ba(OH)2溶液使S042-恰好完全沉淀:2Ba2++3OH-+Al3++2S042-= 2BaS04
+Al(OH)3
4.NA为阿伏伽德罗常数的值。下列叙述正确的是 .
B.丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA
C.25C时pH=11的Na2C03溶液中水电离出的OH-的数目为0.001NA
D.氧原子总数为0.2NA的S02和O2的混合气体,其体积为2.24L
5.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着
锌,在另一边附着二氧化锰。电池总反应为:Zn+2MnO2+H20=Zn0+2Mn0(OH)。下列说法不正
确的是
A.该电池Zn为负极,Mn02为正极
B-该电池的正极反应为:MnO2+e一+H2O=Mn0(OH)+OH-
C.导电时外电路电子由Zn流向Mn02,内电路电子由MnO2流向Zn
D.电池工作时水分子和OH都能通过薄层纸片
6.室温条件下在醋酸、醋酸钠混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol.L-1时,c(CH3COOH)、
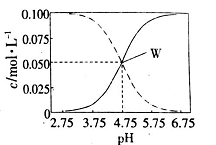 c(CH3COO-)与pH的关系如图所示。下列有关叙述正确的是
c(CH3COO-)与pH的关系如图所示。下列有关叙述正确的是
B.向W点所表示的1.0L溶液中通人0.05molHCl气体(溶液体
积变化可忽略):c(H+)=c(CH3COOH)+c(OH-)
C.pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l
D.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)-
7.在一固定容积的密闭容器中发生如下反应CO(g)+H2O(g)![]() CO2(g)+H2(g)。当充人lmolH2O(g)和1molCO (g)反应达到平衡时,有1/2的CO转化为C02。在相同条件下,若将1molCO (g)和2mol H2O(g)重新充入同一反应容器中,当反应达到平衡后,混合气体中CO2的体积分数可能为
CO2(g)+H2(g)。当充人lmolH2O(g)和1molCO (g)反应达到平衡时,有1/2的CO转化为C02。在相同条件下,若将1molCO (g)和2mol H2O(g)重新充入同一反应容器中,当反应达到平衡后,混合气体中CO2的体积分数可能为
第Ⅱ卷(非选择题 共58分)
8.(15分)A、B、C、D、E、F、G元素原子序数依次增大。已知B原子最外层有3个未成对电子.C原子最外层电子数与核外电子总数之比为3:4,E与C同主族,F-、D+、A+的半径逐渐减小,化合物AF
常温下为气体,G的基态原子核外M能层填满电子,N能层只有1个电子。据此回答下列问题:
量,该反应的热化学方程式为____。
9.(14分)固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验
探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO2)2、NO2、O2乙:Mg0、N02、02丙:Mg3N2、O2丁:MgO、NO2、N2
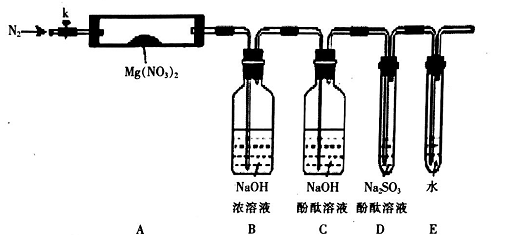
①根据实验和剩余固体的质量经分析可初步确认猜想____ 是正确的。
②根据D中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧
化还原反应生成 (填写化学式),溶液颜色会褪去;小组讨论认定分解产物中有O2
存在,未检测到的原因是 (用化学方程式表示),B、C装置中均盛放NaOH但作用不
一样.C中滴有酚酞NaOH的作用是
③小组讨论后达成的共识是上述实验设计仍不完善,需改进装置进一步研究。
10.(15分)香料G的一种合成工艺如下图所示:
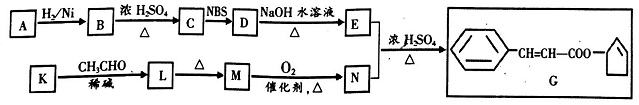
核磁共振氢谱显示A有两种峰,其面积之比为1:1。
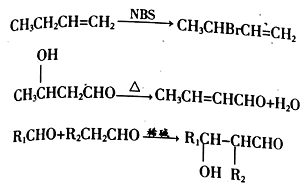
请回答下列问题:
(不考虑立体异构)。(①能发生银镜反应②能与溴的四氯化碳溶液加成③苯环上有2个对位取代
基)F的任意一种结构简式为
1l.(14分)钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。
利用钛铁矿制备锂离子电池电极材料(钛酸锂LiTi5012和磷酸亚铁锂LiFePO4)的工业流程如
下图所示:
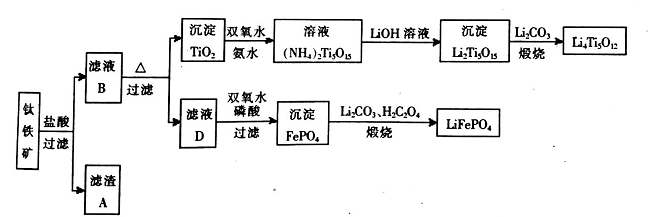
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(2)滤渣A的成分是____ 。滤渣A的熔点大于干冰的原因是 。
(3)滤液B中TiOCI42-转化生成Ti02的离子方程式是 。
(4)由滤液D制备LiFeP04的过程中,所需17%双氧水与H2C204的质量比是 。
(5)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+
3LiFePO4![]() LiTi5012+3FePO4。该电池充电时阳极反应 .
LiTi5012+3FePO4。该电池充电时阳极反应 .
