
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
天津市耀华中学2015届高三第二次校模拟考试
理综 化学试卷
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷两部分,第Ⅰ卷1至3页,第Ⅱ卷4至7页,共100分。
第Ⅰ卷
注意事项:
1.每题选出答案后,用铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
2.本卷共6题,每题6分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求的。
以下数据可供解题时参考:相对原子质量:H -1 C-12 N-14 O-16
1.化学与生产、生活、社会密切相关,下列说法不正确的是( )
| A.只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂 | ||
| B.发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 | ||
| C.蛋白质、淀粉、纤维素、油脂等都能在人体内水解并提供能量 | ||
| D.纯净的二氧化硅是现代光学及光纤制品的基本原料 |
2.下列叙述不正确的是( )
| A | .因为氯气具有酸性,所以可与烧碱或石灰乳反应制备含氯消毒剂 | |
| B | .除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液 | |
| C | .过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:2 | |
| D | .植物油的不饱和程度高于动物油,植物油更易氧化变质 |
3.在不同温度下,向VL密闭容器中加入0.5 mol NO和0.5 mol活性炭,发生反应:
2NO(g)+C(s)![]() N2(g)+CO2 (g) △H=-QKJ·mol-1(Q>0),达到平衡时的数据如下:
N2(g)+CO2 (g) △H=-QKJ·mol-1(Q>0),达到平衡时的数据如下:
| 温度/℃ | n (C)/mol | n(CO2)/mol |
| T1 | 0. 15 | |
| T2 | 0. 375 |
下列有关说法正确的是( )
A.由上述信息可推知:T1>T2
B.T2℃时,若反应达平衡后再缩小容器的体积,c(N2)/c(NO)增大
C.T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率增大
D.T1℃时,该反应的平衡常数![]()
4.下列实验操作能达到实验目的的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验蔗糖水解产物中的葡萄糖 | 取1 mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液,加入几滴新制Cu(OH)2,加热 |
| B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
| C | 验证Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol/L NaOH溶液中加入几滴1 mol/L MgCl2溶液,生成白色沉淀,再加入几滴1 mol/L FeCl3溶液 |
| D | 硅酸胶体的制备 | 向Na2SiO3溶液(饱和溶液1 : 2用水稀释)中加入几滴酚酞,再逐滴滴入盐酸,边加边振荡,至溶液红色变浅并接近消失 |
5. 25℃时,0.1mol/L 的CH3COOH溶液pH=3,0.1mol/L 的HCN溶液pH=4.下列说法正确的是( )
| A | .CH3COOH与HCN均为弱酸,酸性:HCN>CH3COOH | |
| B | .25℃时,水电离出来的c(H+)均为 10-9mol/L的两种酸,酸的浓度: HCN>CH3COOH | |
| C | .25℃时,浓度均为0.1 mol/L 的CH3COONa和NaCN溶液中,pH大小: CH3COONa>NaCN | |
| D | .25℃时,量取100m LpH=3的CH3COOH溶液加水稀释到1000m L,所得溶液由水电离的c(OH-)>10-10mol/L |
6.下列坐标图均涉及到平衡原理,其中相关描述正确的是( )

A.图①表示室温下,用0.1 mol/L氨水吸收HCl气体时,溶液的粒子浓度随吸收HCl的变化,实线表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性
B.图②表示![]() ,正逆反应的平衡常数随温度的变化
,正逆反应的平衡常数随温度的变化
C.图③表示反应![]() 在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
在恒温恒压装置中达平衡时,N2的物质的量与通入NH3的物质的量的变化关系
D.图④表示![]() 的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
的离子的浓度关系,当处于b点时,蒸发部分的水后,可以到达平衡线的a点处
第Ⅱ卷
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题纸上。
2.本卷共4题,共64分。
7.(14分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示。
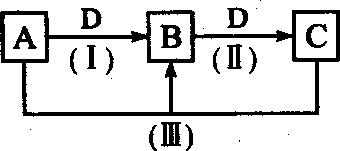
请回答下列问题。
①A中所含化学键类型为 ,D的电子式为 。
②25℃时,浓度均为0.1 mol/L的B、C溶液,pH较大的是 (填溶质的化学式)溶液,写出B溶液中显电中性的原因: (用B溶液中有关微观粒子的浓度关系表示)。已知B溶液的pH=a,则其水电离出来的H+的浓度为: 。
8.(18分)高分子化合物材料PET聚酯和PMMA的合成路线如下:
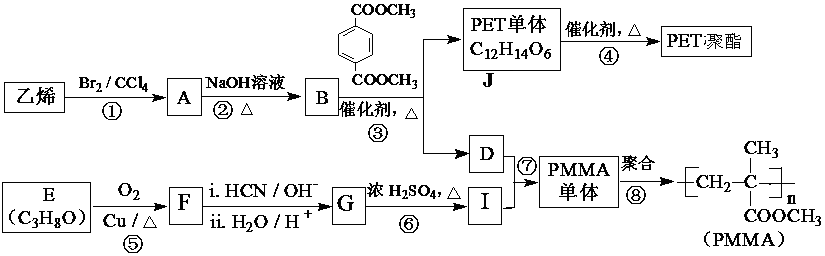
已知:![]()
⑴PMMA单体的化学名称 。
⑵F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为________________________。
反应⑤、⑥的 反应类型________________、________________
⑶ G的分子式__________________, G中官能团的名称________________________。
2分子G可形成环状化合物,写出化学方程式___________________________。
⑷ I的某种同分异构体与I具有相同官能团,且为顺式结构,其结构简式是_________。
⑸写出与F互为同分异构体且含单官能团的所有有机物的结构简式______________。
⑹写出由PET单体制备PET聚酯并生成B的化学方程式 。
9.(18分)亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
取2mL0.1mol/L两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液。两支试管均产生白色沉淀。分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。
该温度下Ksp(AgNO2)=2×10-8;Ksp(AgCl)=1.8×10-10
则反应AgNO2(s) +Cl-(aq)![]() AgCl(s)+ NO2-(aq)的化学平衡常数K=
AgCl(s)+ NO2-(aq)的化学平衡常数K=
( 计算结果保留两位小数)。
㈡NaNO2性质探究
该兴趣小组同学用下图装置探究亚硝酸钠与硫酸反应产生的气体产物成分。
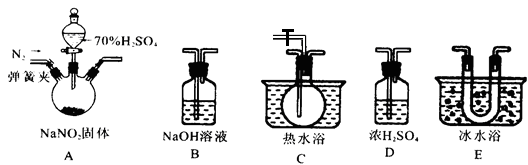
已知:①2NaNO2+H2SO4=Na2SO4+NO↑+NO2↑+H2O
②气体液化的温度:NO2 :21℃ (液化为暗褐色液体) 、 NO :–152℃
(1)为了检验装置A中生成的气体产物中的氮氧化物,仪器的连接顺序为(从左向右连接):A→______→______→ ______→______。
(2)反应前应打开弹簧夹,先通入一段时间氮气。通氮气的目的是______________。(3)再关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①如何确认A中产生气体是否含有NO _________。(写出实验操作、现象和结论)
②装置E的作用是_______________________。
③若向C中通入过量O2,则装置B中发生反应的化学方程式为___________________。10.(14分)氢气是一种理想的“绿色能源”,下图为氢能产生与利用的途径
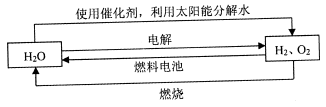
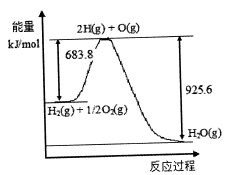 已知H2O(1) =H2O(g)△H= +44 kJ·mol-1,依据右图能量变化写出表示氢气的燃烧热的热化学方程式________________________________。
已知H2O(1) =H2O(g)△H= +44 kJ·mol-1,依据右图能量变化写出表示氢气的燃烧热的热化学方程式________________________________。①镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g)![]() LaNi5H6(s)
LaNi5H6(s)
△H<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件之一
是_____________。
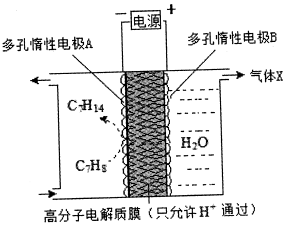
②一定条件下,如图所示装置可实现有机物的电化学储氢,总反应:
2C7H8+6 H2O(1)![]() 2C7H14+3O2(g)
2C7H14+3O2(g)
电解过程中产生的气体X为_________,电极A发生的电极反应式为____________。
天津市耀华中学2015届高三第二次校模拟考试
化学答案
1.C 2.A 3.D 4.D 5.B 6.C
7.(14分)
⑴4NH3+6NO =5N2+6H2O (2分)
⑵Al3++3AlO2-+6H2O=4 Al(OH)3↓ (2分)
⑶2:1 (1分) c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+) (2分)
⑷①离子键、共价键 (2分) ![]() (1分)
(1分)
② Na2C03(1分)c(Na+)+c(H+)=c(HCO)+2c(CO32-)+c(OH-) (2分)
10a-14 mol/L (1分)
8.(18分)⑴ 甲基丙烯酸甲酯(1分)
⑵![]() (2分)氧化反应、消去反应(2分)
(2分)氧化反应、消去反应(2分)
⑶ C4H8O3 羟基 羧基(3分) 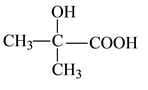 2分子成环酯化,方程式略(2分)
2分子成环酯化,方程式略(2分)
⑷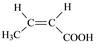 (2分)
(2分)
⑸ CH3CH2CHO、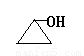 、
、![]() 、
、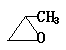 (全对4分)
(全对4分)
(6)(2分)
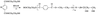
9.(18分)㈠⑴NO2-+H2O![]() HNO2+ OH-(2分)
HNO2+ OH-(2分)
c(OH-)-c(H+)或c(Na+)-c(NO2-)(2分)
⑵111.11(2分)
㈡(1) D E C B(3分);
⑵排除装置中的空气,防止一氧化氮被氧化(2分)
⑶①打开活塞,向C中通入O2,若出现红棕色气体,证明A中产生气体含有NO ;若无红棕色气体出现,则不含NO (3分)
②冷凝,使NO2完全液化(2分)
③4NO2+O2+4NaOH=4NaNO3+2H2O(2分)
10.(14分)
(1)D(2分) (2)=(2分) >(2分)
(3)H2(g)+1 /2O2(g) === 2H2O(l) ΔH=-285.8 kJ·mol-1(2分)
(4)①升高温度或降低压强 (2分)②O2(2分)
C7H8+6H++6e-===C7H14(2分)