
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
![]() 新疆乌鲁木齐2018届高三第一次诊断测试
新疆乌鲁木齐2018届高三第一次诊断测试
化学
注意事项:
1.本试卷为问答分离试卷,共10页,其中问卷8页,答卷2页。答案务必写或涂在指定位置上。
2.答题前,请考生务必将自己的学校、姓名、准考证号、科别等信息填写在答卷的密封区内。
3.可能用到的相对原子质量:H-1 O-16
第I卷(选择题共42分)
一、选择题(本大题共14个小题,每小题3分,共42分;每小题只有1个选项符合题意)
1.古“丝绸之路”我国商人运出的货物有:①丝绸 ②茶叶 ③白糖 ④瓷器 ⑤纸张 ⑥植物油⑦明矾 ⑧金银铜器等。下列说法正确的是
A.④、⑦、⑧都属于盐类
B.①、③、⑤、⑥都属于高分子化合物
C.①、②、⑤、⑥都属于蛋白质
D.①、②、③、⑤、⑥的主要成分都属于有机物
2.化学与生活密切相关,下列说法正确的是
A.防腐剂是一种影响化学反应速率的食品添加剂
B.高锰酸钾溶液、酒精、双氧水能杀菌消毒是利用了它们的强氧化性
C.小苏打做糕点的膨松剂是由于NaHCO3能与碱反应
D.维生素C对人体有益且人体不能合成,长期、大量服用有利于健康
3.设NA为阿伏伽德罗常数的值,下列说法正确的是
A.标准状况下,3.4 g D2O2所含极性键数目为0.2NA
B.25℃,pH =2的H2SO4溶液中,H+的数目为0.02 NA
C.标准状况下,2.24 L CCl4含有的分子数目为0.1NA
D.lmol OH-含有的电子数目为10NA
4.下列对应化学反应的离子方程式中正确的是
A.氧化钠投入水中:O2-+H2O =2OH-
B.FeCl3溶液与KI溶液反应:2Fe3++2KI= 2Fe2++I2+2K+
C.过量硫酸氢铵溶液与氢氧化钡溶液反应:Ba2++2OH-+SO42-+2H+=BaSO4↓+2 H2O
D.铜片投入稀硝酸:Cu +4H++NO3-= Cu2++NO2↑+2H2O
5.实验是化学研究的基础,下列各实验装置的叙述正确的是
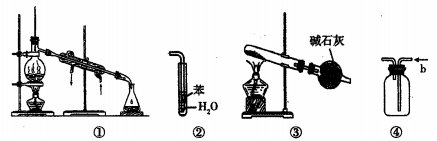
A.装置①常用于分离互不相溶液体混合物
B.装置②可用于吸收HC1气体,并防止倒吸
C.以NH4HCO3为原料,装置③可用于实验室制备少量NH3
D.装置④b口进气排空气法可收集CO2、NO等气体
6.分子式为C7H7Cl,且分子中含有苯环的同分异构体有(不考虑立体结构)
A.3种 B.4种 C.5种 D.6种
7.樱桃是一种抗氧化的水果,其表现抗氧化性的一种有效成分M的结构简式如图:![]() 下列有关M的说法中不正确的是
下列有关M的说法中不正确的是
A.M的分子式为C4H6O5
B.M中含有两种官能团,分别为羟基和羧基
C.标准状况下,0.1 moI M完全燃烧时消耗6.72 L O2
D.1mol M与足量金属钠反应生成3mol H2
8.下列反应类型相同的一组是
A.乙烯使溴水褪色,乙醇使酸性高锰酸钾溶液褪色
B.乙醇与浓硫酸共热至170℃,纤维素与浓硫酸共热
C.乙酸乙酯水解生成乙醇,氯乙烷( C2H5Cl)水解成乙醇
D.乙醇通过灼热的氧化铜粉末,石蜡油蒸汽通过灼热的碎瓷片
9.25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.含有大量NO3-的溶液:H+、K+、Cl-、SO32-
B.中性溶液:Fe3+、Al3+、NO3-、SO42-
C.![]() 的溶液:K+、AlO2-、CO32-、Na+
的溶液:K+、AlO2-、CO32-、Na+
D.由水电离出的c(H+) =10-12mol/L的溶液:Na+、K+、CO32-、SO42-
10.下图为海水利用的部分过程。下列有关说法正确的是
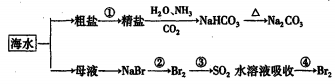
A.粗盐提取精盐的过程只发生物理变化
B.用澄清的石灰水可鉴别Na2CO3产品是否含有NaHCO3
C.在第②、④步骤中,溴元素均被还原
D.制取NaHCO3的反应是利用其溶解度小于NaCl
11. 一种锂铜可充屯电池,工作原理如图。在该电池中,非水系电解液和水系电解液被锂离子固体电解质陶瓷片(LISICON)隔开。下列说法不正确的是

A.陶瓷片允许Li+通过,不允许水分子通过
B.放电时,N为电池的正极
C.充电时,阴极反应为:Li++e-=Li
D.充电时,接线柱A应与外接电源的正极相连
12.在给定条件下,下列选项所示的物质闻转化均能实现的是
A.SiO2![]() SiCl4
SiCl4![]() Si
Si
B.S![]() SO3
SO3![]() H2SO4
H2SO4
C.CaCO3![]() CaO
CaO![]() CaSiO3
CaSiO3
D.NH3![]() NO
NO![]() HNO3
HNO3
13.下列实验方案能达到实验目的的是
| 实验目的 | 实验方案 | |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCI2溶液,观察是否有沉淀生成 |
| B | 证明酸性条件下H2O2氧化性强于l2 | 向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝;再加入10%的H2O2溶液,溶液立即变蓝色 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2 mL1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
14.一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s) + CO22CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
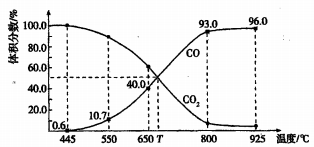
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
A.550℃时,若充入惰性气体,V正、V逆均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为40.0%
C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总
第Ⅱ卷(非选择题共58分)
二、【本题包括5个题,共58分)
15.(10分)X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一 半,Y、Z、W原子的最外层电子数之和为14。
16.(12分)电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
| 弱酸 | HCOOH | HCN | H2C03 |
| 电离常数(25℃) | Ka = 1. 77×10 -4 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
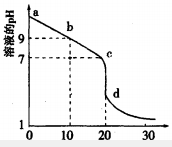
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为____mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中![]() =___________(保留三位有效数字)。
=___________(保留三位有效数字)。
17.(14分)三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷。某化学兴趣小组将无水三草酸合铁酸钾按如图所示装置进行实验。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
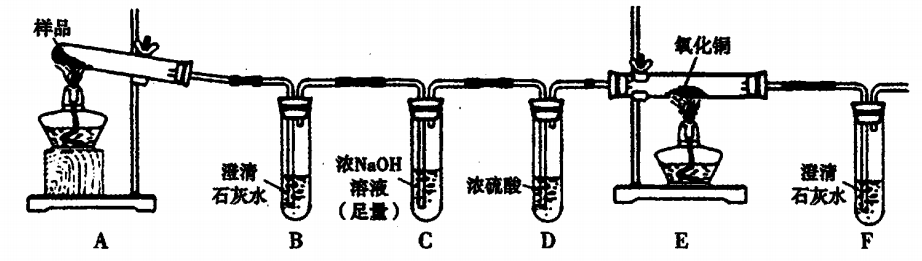
限选试剂:浓硫酸、1.0mol/L HNO3、1.0mol/L盐酸、1.0 mol/L NaOH.3% H2O2、0.1 mol/LKI、0.1mol/LCuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水。
I.若实验中,观察到B、F中溶液均变浑浊,则E中的现象是____,推测三草酸合铁酸钾分解的气体产物是____。该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。
Ⅱ.探究固体产物中铁元素的存在形式。
(l)提出合理假设:假设l____;假设2____;假设3____。
(2)设计实验方案并验证
①取适量固体产物于试管中,加入足量蒸馏水溶解,过滤分离出不溶固体。
②取少量上述不溶固体放入试管中,加入足量____溶液,充分振荡。若溶液颜色及加入的不溶固体无明显变化,则假设____成立。若溶液颜色明显改变,且有暗红色固体生成,则证明有____存在。
③取②所得暗红色固体于试管中,滴加过量____,振荡后静置。取上层清液于试管中,滴加适量____,再滴加____,若溶液基本无色,则假设____成立;若溶液呈____,则假设_____成立。
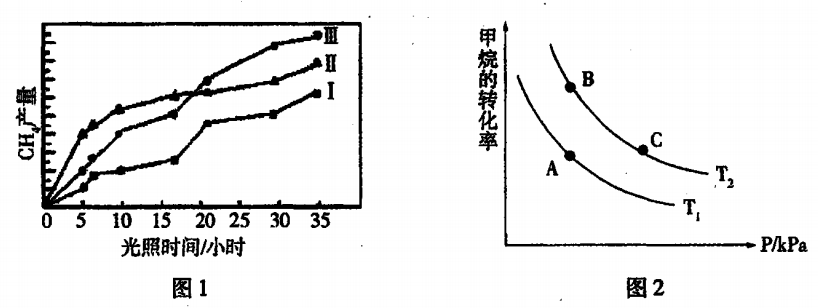
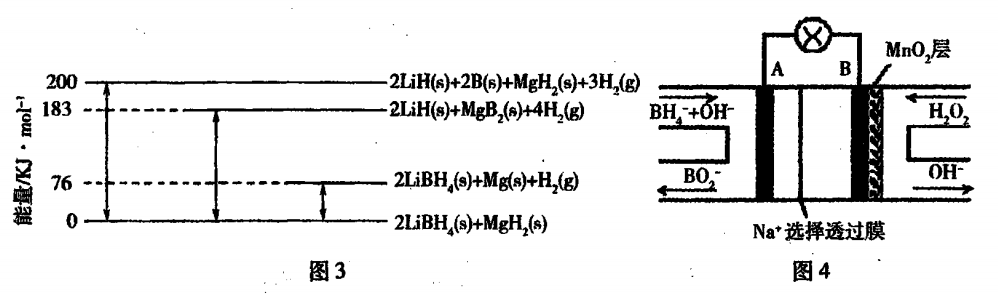
18.(11分)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。
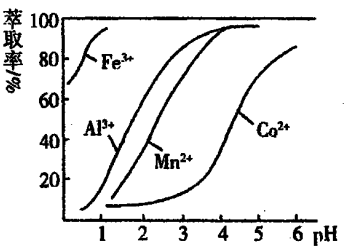
19.(11分)用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:
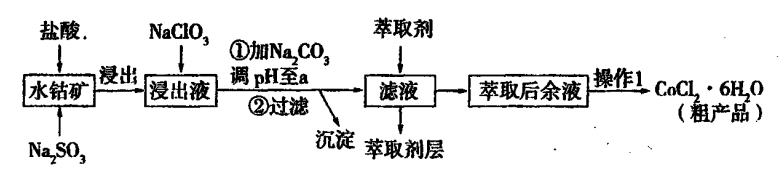
己知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe( OH)3 | Fe(OH)2 | Co(OH)2 | Al( OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
第I卷(选择题共42分)
一、选择题(本大题共14个小题,每小题3分,共42分;每小题只有1个选项符合题意)
1-10:DADCC BDCCD 11-14:DCBD
第Ⅱ卷(选择题共58分)
二、(本题包括5个题,共58分,除特殊说明外,每空1分)
15、(10分)
(3)2H2O+2F2=4HF+O2
(4)2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Al3++3HCO3-=Al(OH)3↓+3CO2↑
(5)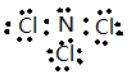 ;NCl3+3H2O=3HClO+NH3
;NCl3+3H2O=3HClO+NH3
16、(12分)
17、(14分)
I.黑色粉末变红,CO和CO2
II.(1)只有Fe;只有FeO;含有FeO和Fe;
(2)②CuSO4溶液,2,Fe;③HCl, 3%H2O2,20%KSCN,1,血红色,3(其它合理答案均可)
18、(11分)
(l)①v I
(2)①2;②-93 kJ/mol;(3)增大;BH4--8e-+8OH-=BO2-+6H2O(2分)
19、(11分)