
湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
山西大学附中
2016—2017学年高三年级五月(第十五次)模拟考试
理科综合化学试题
7.关于下列诗句或谚语,说法不正确的是( )
A.“忽闻海上有仙山,山在虚无缥缈间”的海市蜃楼是一种自然现象,与胶体知识有关
B.“水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化
C.“滴水石穿、绳锯木断”不包含化学变化
D.“落汤螃蟹着红袍”肯定发生了化学变化
8.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.50mL18.4mol.L﹣1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
B.某密闭容器盛有0.1molN2和0.3molH2,充分反应后转移电子的数目为0.6NA
C.若由CO2和O2组成的混合物中共有NA个分子,则其中的氧原子数为2NA
D.常温下1L0.1mol.L﹣1NH4NO3溶液中的氢原子数为0.4NA
9.常温常压时,下列叙述不正确的是( )
A.20mL0.1mol/L CH3COONa溶液与10mL0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO﹣)>c(Cl﹣)>c(CH3COOH)>c(H+)
B.含等物质的量的NaHC2O4和Na2C2O4的混合溶液:
2c(Na+)=3[c(HC2O4﹣)+c(C2O42﹣)+c(H2C2O4)]
C.PH=1的NaH SO4溶液:c(H+)=c(SO42﹣)+c(OH﹣)
D.CO2的水溶液:c(H+)>c(HCO3﹣)=2c(CO32﹣)
10.下面是几种常见的化学电源示意图,有关说法不正确的是( )
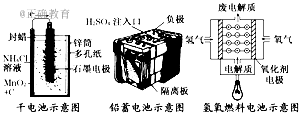
A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
11.下列各有机物的数目与分子式C4H7ClO2且能与NaHCO3溶液反应生成CO2的有机物的
数目(不考虑立体异构)相同的是
A.分子式为C5H10的烯烃 B.甲苯的一氯代物
C.相对分子质量为74的一元醇 D.立方烷(![]() )的二硝基取代物
)的二硝基取代物
12、五种短周期主族元素W、X、Y、Z、R的原子序数依次增大,W与X的原子序数之和
等于Y 的原子序数,X、Y同周期,Z的单质与冷水能剧烈反应生成W的单质,R的简单
离子在同周期元素的简单离子中半径最小,W2Y2常温下为一种液态化合物。下列说法正
确的是
A.原子半径为W
B.2 mol Z单质投人足量W2Y中,电子转移数为2×6.02×1023
C.电解熔融状态的R的氯化物,可制得R的单质
D.W、X、Y三种元素不能组成离子化合物
13.下列有关实验现象或亊实解释正确的是 ( )
| 选项 | 实验现象或事实 | 解释 |
| A | 检验待测液中SO42﹣时,先滴入稀盐酸,再滴入BaCl2溶液 | 先滴入盐酸可排除Ag+、CO32﹣、SO32﹣等离子干扰 |
| B | 制备乙酸乙酯时,导管应伸入试管至饱和Na2CO3溶液液面上方 | 乙酸乙酯易溶于碳酸钠溶液,防止发生倒吸 |
| C | 向Fe(NO3)2溶液中加入稀硫酸,试管口有红棕色气体产生 | 溶液中NO3﹣被Fe2+还原为NO2 |
| D | 含Mg(HCO3)2的硬水长时间充分加热,最终得到的沉淀物的主要成分为Mg(OH)2,而不是MgCO3 | Ksp(MgCO3)<Ksp[Mg(OH)2] |
26、(15分)根据下图所示各装置和实验室制取氧气的原理,回答下列问题:
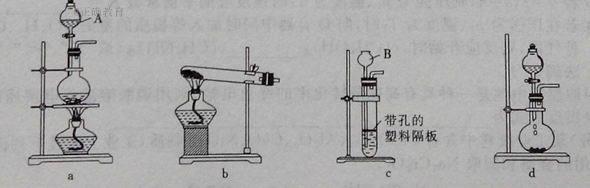
(6)用装置d制取氨气时,所需的化学药品是________________,氨气的电子式为__________。
27、(14分)CO、H2、CH3、OH均是清洁能源。
| 化学键 | C | O=O | C=O | C-O |
| E/(kJ • mol-1) | 958.5 | 497 | 745 | 351 |

28、(14分)某工业废料料中含有Cr(OH)3、Al2O3、CuO、NiO等物质,工业上通过下列流程回收其中有用的金属和制取Na2Cr2O7。
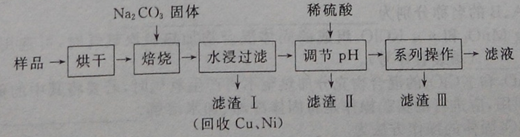
已知:
①“水浸过滤”后的溶液中存在Na2CrO4、NaAlO2等物质
②除去滤渣II后,溶液中存在反应2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
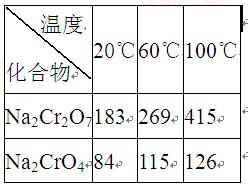
③Na2Cr2O7、Na2CrO4在不同温度下的溶解度(g/100 g H2O)如下表:
| 元素代号 | X | Y | Z |
| 第一电离能(kJ·mol-1) | 520 | 496 | 419 |
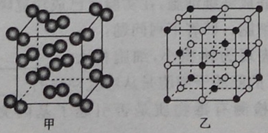
36.【化学—选修5 有机化学基础】(15分)
某芳香酸类物质F常用做香精的调香剂。F的—种合成路线如下:
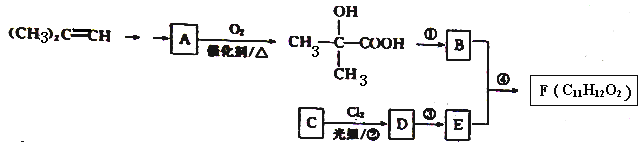
己知:A能发生银镜反应。回答下列问题:
化学答案
| 题号 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答案 | C | C | D | D | A | B | A |
26、(15分)(1)分液漏斗(1分)长颈漏斗(1分)
(2)b(l 分)
(3)过滤(1分)将蒸馏水沿玻璃棒慢慢地注入到过滤器漏斗中至液面浸没滤纸上的固体,待水流尽后重复操作2〜3次(2分)取最后一次洗涤液少许,向其中滴加几滴AgNO3溶液,若无沉淀生成,则证明MnO2固体已洗涤干净(2分)
(4)96 : 245 (2分)
(5)MnO2是粉状固体,不能稳定存在于装置中的塑料隔板之上(或不能控制反应速率)(2分)
(6)浓氨水、碱石灰(或浓氨水、生石灰或浓氨水、氢氧化钠固体)(2分)![]() (1分)
(1分)
27、(14分)(1)-566 (2分) -107 (2分) (2)①>(2分)
② >(2分) ③4. 5(2分) ④无法确定(2分)
(3)CH3OH+H2O-6e-==CO2↑+6H+(2分)
28、(14分)(1)A12O3+NaCO3![]() 2NaAlO2+CO2↑(2分)
2NaAlO2+CO2↑(2分)
(2)A1(OH)3+3H+==Al3++3H2O (2分)
⑶蒸发浓缩(1分)促进化学平衡2CrO42-+2H+![]() Cr2O72-+H2O向正反应方向移动,尽可能生成更多的Na2Cr2O7(2分) Na2Cr2O7(2分)
Cr2O72-+H2O向正反应方向移动,尽可能生成更多的Na2Cr2O7(2分) Na2Cr2O7(2分)
(4) Cr2O72-+14H++12e-==2Cr↓+7H2O (2分) (5)![]() (3分)
(3分)
35、⑴Li、Na、K (l分) ls22s22p63s23p64sl(1分) 金属键(1分)
(2)sp(l分) sp3 (1分) 直线形(1分)V形(1分) (3)120° (2分)
(4)4 (1分) 6 (2分)
(5)![]() ×100% (3分)
×100% (3分)
36、(1)2—甲基丙烯(或2一甲基—1—丙烯)(2分)②③④(2分)
(2)![]() (1分) 氯原子(1分)
(1分) 氯原子(1分)
(3)浓硫酸、加热(1分)
(4)CH2=C(CH3)COOH+ HOCH2![]()
![]() CH2=C(CH3)COOCH2
CH2=C(CH3)COOCH2![]() +H2O (2分)
+H2O (2分)
(5)4(2分)![]() (1分)
(1分)
(6)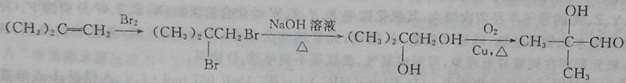 (3分)
(3分)