湖南省醴陵二中、醴陵四中2016-2017学年高二下学期期中联考化学试卷
03月05日
2015届高三化学模拟试卷
2015.5
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。共120分。考试用时100分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Fe-56 S-32 Ba-137 Cu-64
选择题(共40分)
单项选择题:本题包括10小题,每题2分,共计20分。每小题只有一个选项符合题意。
1、下列说法错误的是
A.使用可降解塑料聚二氧化碳,能减少白色污染
B.实施“煤改气”、“煤改电”等清洁燃料改造工程,有利于保护环境
C.雷雨过后感觉到空气清新是因为空气中产生了少量的二氧化氮
D.通常所说的三大有机合成材料是指塑料、合成纤维、合成橡胶
2、下列有关化学用语表示正确的是
A.HClO的结构式:H—Cl—O B.NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO
C.羟基的电子式:![]() D.异丙醇的结构简式:CH3CH2CH2OH
D.异丙醇的结构简式:CH3CH2CH2OH
3、25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:MnO、SO、K+、Fe3+
B.0.1 mol·L-1FeCl3溶液中:Mg2+、NH、SCN-、SO
C.滴入甲基橙显黄色的溶液中: Na+、ClO-、I-、SO
D.水电离产生的c(H+)=10-12mol·L-1的溶液中:K+、Na+、NO、CH3COO-
4、下列有关物质性质与应用对应关系错误的是
A.常温下,浓硫酸能使铝钝化,可用铝制容器贮运浓硫酸
B.二氧化硅熔点很高、硬度很大,可用于制造坩埚
C.氯化铁溶液能腐蚀铜,可用于制作印刷电路板
D.金属钠硬度小、密度小,可用于制造高压钠灯
5、用下列实验装置进行相应实验,能达到实验目的的是
浓硫酸
图1 图2 图3 图4
A.用图1所示装置验证浓硫酸具有强氧化性 B.用图2所示装置制取干燥的NH3
C.用图3所示装置制取并收集乙烯 D.用图4所示装置制取Cl2
6、设NA为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,11.2 L NO和11.2 L SO3的分子总数为0.5NA
B.0.1molBr2与足量H2O或NaOH反应转移的电子数均为0.1NA
C.0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA
D.在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA
7、下列指定反应的离子方程式正确的是
A.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO恰好沉淀完全:
2Ba2++4OH-+Al3++2SO=2BaSO4↓+AlO+2H2O
B.向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO
C.氧化亚铁溶于稀硝酸:3FeO + 8H+ + NO=3Fe3+ + NO↑+ 4H2O
D.4 mol·L-1的NaAlO2溶液和7 mol·L-1的盐酸等体积混合:
4AlO+7H++H2O=3Al(OH)3↓+Al3+
8、X、Y、Z、W四种物质在一定条件下具有如图所示的转化关系,下列判断正确的是
![]()
A.若图中反应均为非氧化还原反应,当W为一元强碱时,则X可能是NaAlO2
B.若图中反应均为非氧化还原反应,当W为一元强酸时,则X可能是NH3
C.若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2
D.若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl3
9、短周期元素A、B、C、D的原子序数依次增大,它们原子的最外层电子数之和为16,A与D同主族,B+与A2-具有相同的电子层结构,C原子的最外层电子数等于A原子最外层电子数的一半,则下列叙述正确的是
A.B2A2和B2A中阴阳离子的个数比相同
B.原子半径的大小顺序:r(D)>r(C)>r(B)>r(A)
C.D的简单气态氢化物的热稳定性比A的强
D.元素C的单质是一种高硬度、高熔点的金属
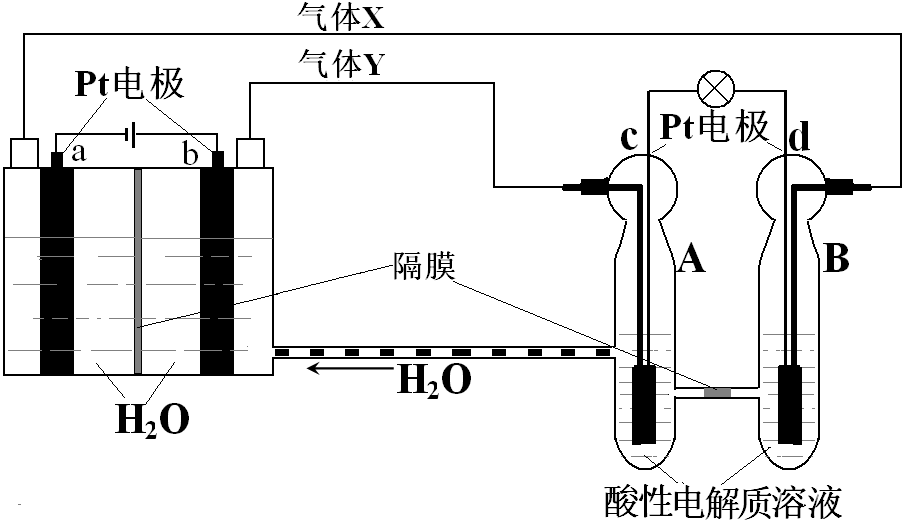
10、RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图。下列有关说法正确的是
A.转移0.1mol电子时,a电极产生标准状况下O21.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B池中的H+可以通过隔膜进入A池
 D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项时,只选一个且正确的得2分,选两个都正确的得满分,但选错一个,该小题就得0分。
11、下列有关说法正确的是
A.Na2CO3和NaOH都能抑制水的电离
B.0.1 mol·L-1Na2CO3溶液加水稀释,CO的水解程度增大,溶液pH减小
C.酸碱中和滴定实验中,锥形瓶需用待测液润洗2~3次后,再加入待测液
D.常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n
12、某药物中间体的合成路线如下。下列说法正确的是
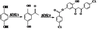
对苯二酚 2,5-二羟基苯乙酮 中间体
A.对苯二酚在空气中能稳定存在 B.1 mol该中间体最多可与11 mol H2反应
C.2,5-二羟基苯乙酮能发生加成、水解、缩聚反应
D.该中间体分子中含有1个手性碳原子
13、下列有关实验的说法错误的是
A.向品红溶液中通入气体X,品红溶液褪色,则气体X可能是Cl2
B.CO2中含少量SO2,可将该混合气体通入足量饱和NaHCO3溶液中除去SO2
C.用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色,说明该食盐试样中不含KIO3
D.向NaHCO3溶液中滴加酚酞试液,加热时溶液由淡红色变为红色,冷却后溶液由红色变为淡红色,说明HCO在水溶液中存在水解平衡
14、25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.在0.1 mol·L-1NH4Cl溶液中:c(H+)=c(NH3·H2O)+c(OH-)
B.10 mL 0.1 mol·L-1CH3COONa溶液与6 mL 0.2 mol·L-1盐酸混合:
c(Cl-) >c(Na+) >c(OH-) >c(H+)
C.0.1 mol·L-1NH4HSO4溶液与0.1 mol·L-1NaOH溶液等体积混合:
c(Na+) = c(NH) >c(H+) >c(OH-)
D.0.1 mol·L-1HCN溶液和0.05 mol·L-1NaOH溶液等体积混合(pH>7):
c(HCN) + c(H+) >c(OH-) + c(CN-)
15、一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
CO(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法正确的是
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B.丙容器的体积V>0.5L C.当温度为T1℃时,反应的平衡常数K=4.5
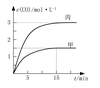 D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |
非选择题(共80分)
16、氯化亚铜是一种应用较广的催化剂,易水解。以低品位铜矿砂(主要成分CuS)为原料制备氯化亚铜的路线如下:
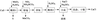
(1)酸溶1步骤中加入MnO2的作用是▲。
(2)除锰步骤Mn2+转化为MnCO3沉淀,该反应的离子方程式为▲。溶液中CuSO4转变为Cu(NH3)4CO3留在溶液中。
(3)蒸氨步骤会得到CuO固体,该步骤在减压条件下进行的原因是▲。
(4)写出合成步骤中发生反应的化学方程式▲。
(5)有工艺将合成步骤的NaCl与Na2SO3换为NH4Cl和(NH4)2SO3,则可获得一种可作为氮肥的副产品,其化学式为▲。
(6)洗涤步骤先用▲洗,再用无水乙醇洗涤。
17、药物F具有抗肿瘤、降血压、降血糖等多种生物活性,其合成路线如下:
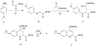 已知:
已知: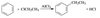
(1)原料A中含氧、含氮的官能团名称是▲、▲。
(2)写出中间产物E的结构简式▲。
(3)反应②、⑤的反应类型是▲、▲。
(4)物质B有多种同分异构体,写出满足下列条件的一种同分异构体的结构简式▲。
①属于α-氨基酸 ②苯环上有两种一氯代物 ③能发生银镜反应
④核磁共振氢谱显示其有7种不同化学环境的氢原子
(5)以![]() 和苯、乙醇为原料,可合成
和苯、乙醇为原料,可合成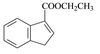 ,写出合成流程
,写出合成流程
图(无机试剂任用)。合成流程图示例如下:
![]()
18、黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]不溶于水和稀硫酸,制取黄钾铵铁矾的流程如下:

(1)溶液X是▲。
(2)检验滤液中是否存在K+的操作是▲。
(3)黄钾铵铁矾的化学式可通过下列实验测定:
①称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00 mL溶液A。
②量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32 g。
③量取25.00 mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体224mL,同时有红褐色沉淀生成。
④将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80 g。
通过计算确定黄钾铵铁矾的化学式(写出计算过程)。▲
19、高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下:
(1)浸出:浸出时温度控制在90℃~95℃之间,并且要连续搅拌3小时的目的是▲,植物粉的作用是▲。
(2)除杂:①向浸出液中加入一定量的碳酸锰矿,调节浸出液的pH为3.5~5.5;
②再加入一定量的软锰矿和双氧水,过滤;
③…
操作①中使用碳酸锰调pH的优势是▲;操作②中加入双氧水不仅能将Fe2+氧化为Fe3+,而且能提高软锰矿的浸出率。写出双氧水提高软锰矿浸出率的离子方程式▲。
(3)制备:在30 ℃~35 ℃下, 将碳酸氢铵溶液滴加到硫酸锰净化液中, 控制反应液的最终pH在6.5~7.0,得到MnCO3沉淀。温度控制35 ℃以下的原因是▲;该反应的化学方程式为▲;生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是▲。
(4)计算:室温下,Ksp(MnCO3)=1.8×10-11,Ksp(MgCO3)=2.6×10-5,已知离子浓度小于1.0×10-5mol·L-1时,表示该离子沉淀完全。若净化液中的c(Mg2+)=10-2mol/L,试计算说明Mg2+的存在是否会影响MnCO3的纯度。
20、脱去冶金工业排放烟气中SO2的方法有多种。
(1)热解气还原法。已知CO还原SO2生成S(g)和CO2过程中,每转移1mol电子需吸收2.0 kJ的热量,则该反应的热化学方程式为▲。
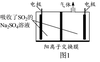 (2)离子膜电解法。利用硫酸钠溶液吸收SO2,再
(2)离子膜电解法。利用硫酸钠溶液吸收SO2,再
用惰性电极电解。将阴极区溶液导出,经过滤
分离硫磺后,可循环吸收利用,装置如图1
所示,则阴极的电极反应式为▲,阳极产
生气体的化学式为▲。
(3)氧化锌吸收法。配制ZnO悬浊液(含少量MgO、CaO),在吸收塔中封闭循环脱硫,发生的主要反应为ZnO+SO2 = ZnSO3(s),测得pH、吸收效率η随时间t的变化如图2所示。
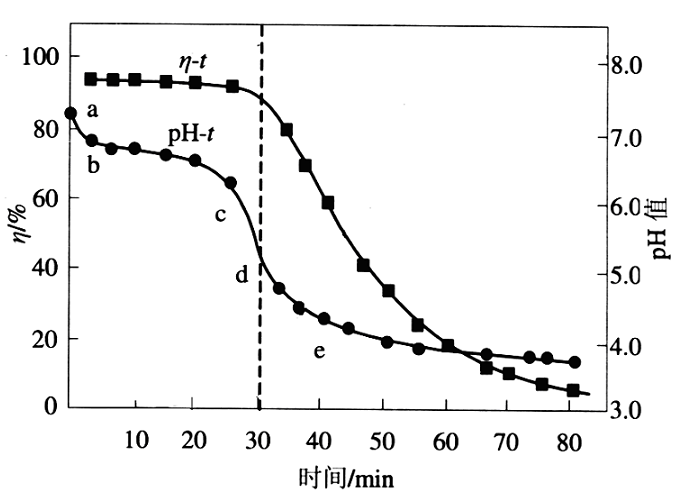
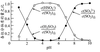
图2 图3
①该反应常温能自发进行的原因是▲。
②纯ZnO的悬浮液pH约为6.8,结合图2和图3,下列说法正确的是▲。
A.向ZnSO3与水混合体系中加稀硫酸,硫元素会以SO2形式逸出
B.pH-t曲线ab段发生的主要反应为ZnO+SO2=ZnSO3
C.pH-t曲线cd段发生的主要反应为ZnSO3+SO2+H2O = Zn (HSO3)2
D.pH=7时,溶液中c(SO) =c(HSO)
③为提高SO2的吸收效率η,可采取的措施为▲。
A.增大悬浊液中ZnO的量
B.适当提高单位时间内烟气的循环次数
C.调节溶液的pH至6.0以下
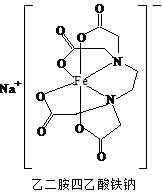
21、乙二胺四乙酸可由乙二胺(H2NCH2CH2NH2)、氰化钠(NaCN)和甲醛水溶液作用制得,能和Fe3+形成稳定的水溶性配合物乙二胺四乙酸铁钠,原理如下:

(1)Fe3+基态核外电子排布式为▲。
(2)与CN-互为等电子体的一种非极性分子为▲(填化学式)。
(3)乙二胺四乙酸中C原子的轨道杂化类型是▲;C、N、O三种元素的电负性由大到小的顺序是▲。
(4)乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是▲。
(5)请在乙二胺四乙酸铁钠结构图中用“箭头”表示出配位键。
班级 姓名 学号 ……………………………………线………………………………………封………………………………………………密…………………………………
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | |||||
16(1)
(2)
(3)
(4)
(5) (6)
17(1) 、 (2)
(3) 、 (4)
(5)
18(1)
(2)
(3)
19(1) 、
(2);
(3) ;
;
(4)
20(1)
(2) ,
(3)① ② ③
21(1) (2)
(3) 、
(4)
(5)
2015届高三化学模拟试卷答案
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C | C | A | D | B | D | D | C | A | C |
| 11 | 12 | 13 | 14 | 15 | |||||
| BD | B | C | AD | AC | |||||
16.(12分,每空2分)
(1)氧化剂 (2)Mn2+ + HCO3- + NH3 = MnCO3↓+ NH4+
(3)减压有利于气体逸出。
(4)2NaCl+Na2SO3+2CuSO4+H2O=2CuCl+2Na2SO4+H2SO4
17.(14分)
(1)醚键、氨基(每空1分) (2)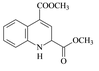 (3分)
(3分)
(3)加成反应,氧化反应(每空1分) (4)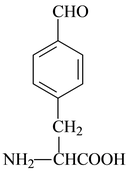 或
或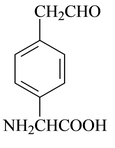 (3分)
(3分)
(5) 或
或
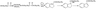 (4分)
(4分)
18.(12分)
(1)氨水(或写“NH3·H2O”)(2分)
(2)用洁净的铂丝(或铁丝)蘸取滤液在酒精灯火焰上灼烧,透过蓝色的钴玻璃观察(1分),若火焰呈紫色,则存在K+(1分)
19.(16分)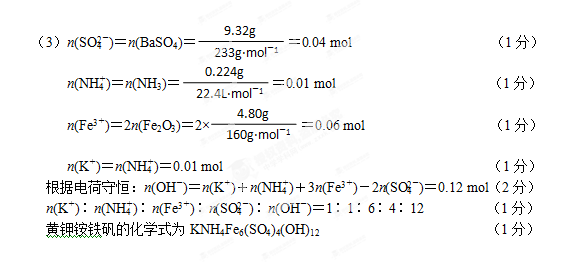 (1)提高软锰矿中锰的浸出率 作还原剂
(1)提高软锰矿中锰的浸出率 作还原剂
(2)增加MnCO3的产量(或不引入新的杂质等) MnO2 + H2O2 + 2H+=Mn2+ + 2H2O +O2↑
(3)减少碳酸氢铵的分解,提高原料利用率;
MnSO4 + 2NH4HCO3![]() MnCO3 + (NH4)2SO4 + CO2↑+ H2O;
MnCO3 + (NH4)2SO4 + CO2↑+ H2O;
取最后一次的洗涤滤液1~2 mL 于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净。
(4)Ksp (MnCO3)=c(Mn2+)·c(CO32-) ,当Mn2+沉淀完全时,c(CO32-)=1.8×10-11/1.0×10-5=1.8×10-6mol·L-1,若Mg2+也能形成沉淀,则要求Mg2+>2.6×10-5/1.8×10-6=14.4 mol·L-1, Mg2+的浓度0.01mol/L远小于14.4 mol·L-1。
20.(14分)(1)2CO(g) + SO2(g) = S(g) + 2CO2(g) ΔH=+8.0 kJ·mol-1(3分)
(2)SO2+4H++4e-=S+2H2O(或H2SO3+4H++4e-=S+3H2O)(3分),O2
(3)①ΔH<0 ②AC ③AB
21.(12分)
(1)[Ar]3d5或1s22s22p63s23p63d5(2)N2
(3)sp2、sp3;O>N>C (4)乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键。
(5)